将标准状况下一定体积的CO2缓缓通入体积为VLNaOH溶液中,充分反应后,在减压低温的条件下蒸发溶液,得到白色固体。
(1)由于CO2通入量不同,所得到的白色固体的组成不同,推断并写出各种可能组成的化学式:(可以不填满,也可以添加序号)
①________ ;②________ ;③________ ;④________ ;⑤________ ;⑥________ 。
(2)按反应的先后顺序,写出各步反应的离子方程式:________ 。
(3)若反应中CO2和NaOH均无剩余,反应后向溶液中加入过量的澄清石灰水生成m1g白色沉淀。
①根据以上数据,能否推理计算出标准状况下CO2的体积?若能,用代数式表示CO2的体积V(CO2)=________ .若不能,理由是________ 。
②根据以上数据,能否推理计算出NaOH溶液的浓度?若能,用代数式表示NaOH溶液的浓度c(NaOH)=________ 。若不能,理由是________ 。
(1)由于CO2通入量不同,所得到的白色固体的组成不同,推断并写出各种可能组成的化学式:(可以不填满,也可以添加序号)
①
(2)按反应的先后顺序,写出各步反应的离子方程式:
(3)若反应中CO2和NaOH均无剩余,反应后向溶液中加入过量的澄清石灰水生成m1g白色沉淀。
①根据以上数据,能否推理计算出标准状况下CO2的体积?若能,用代数式表示CO2的体积V(CO2)=
②根据以上数据,能否推理计算出NaOH溶液的浓度?若能,用代数式表示NaOH溶液的浓度c(NaOH)=
更新时间:2020-07-23 00:42:02
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】化工生产中锂是高能电池的主要原材料。工业上以 为锂源制备
为锂源制备 ,从盐湖水(含有NaCl、LiCl、
,从盐湖水(含有NaCl、LiCl、 、Na2B4O7等物质)中提炼
、Na2B4O7等物质)中提炼 的工艺流程如图所示。
的工艺流程如图所示。
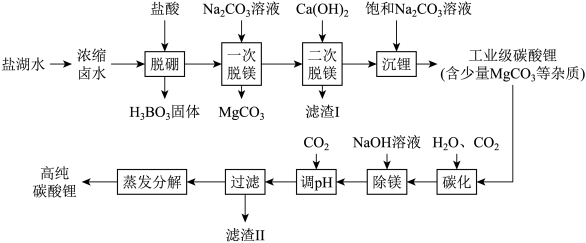
(1)“脱硼”的离子方程式是___________
(2)已知 与足量NaOH溶液反应生成Na[B(OH)4],则
与足量NaOH溶液反应生成Na[B(OH)4],则 为
为___________ 元酸。
(3)滤渣I的成分是___________ (填化学式)
(4)“碳化”中碳酸锂转化为___________ (填化学式)
(5)已知在不同温度下“蒸发分解”,碳酸锂的产率、碳酸锂溶解度与温度的关系如图:

90℃以下,随温度升高,碳酸锂产率升高的原因可能是___________ 。
 为锂源制备
为锂源制备 ,从盐湖水(含有NaCl、LiCl、
,从盐湖水(含有NaCl、LiCl、 、Na2B4O7等物质)中提炼
、Na2B4O7等物质)中提炼 的工艺流程如图所示。
的工艺流程如图所示。
(1)“脱硼”的离子方程式是
(2)已知
 与足量NaOH溶液反应生成Na[B(OH)4],则
与足量NaOH溶液反应生成Na[B(OH)4],则 为
为(3)滤渣I的成分是
(4)“碳化”中碳酸锂转化为
(5)已知在不同温度下“蒸发分解”,碳酸锂的产率、碳酸锂溶解度与温度的关系如图:

90℃以下,随温度升高,碳酸锂产率升高的原因可能是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
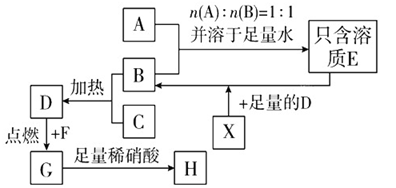
【推荐2】已知A~H均为中学化学常见的物质,A、B、C、E的焰色反应均为黄色。其中B常做食品的膨化剂;A与C按任意比例混合,溶于足量的水中,得到的溶质也只含有一种,并有无色无味的气体D地放出;X为一种黑色固体单质,有多种同素异形体,其氧化性参与大气循环,为温室气体;G为冶炼铁的原料,G溶于盐酸中得到两种化合物。A~H之间有如下的转化关系(部分物质未写出):
(1)写出该物质的化学式:C:_______ ;E:_____ 。
(2)B+C→D的反应中,每生成标准状况下11.2 L D,转移电子的物质的量为_____ mol。
(3)已知F与高温水蒸气也能反应生成G,该反应中,还原剂与还原产物的物质的量之比为_____ 。
(4)写出G与足量稀硝酸反应的离子方程式_______________ 。
(5)G在高温下与铝反应的化学方程式为:___________ 。
(1)写出该物质的化学式:C:
(2)B+C→D的反应中,每生成标准状况下11.2 L D,转移电子的物质的量为
(3)已知F与高温水蒸气也能反应生成G,该反应中,还原剂与还原产物的物质的量之比为
(4)写出G与足量稀硝酸反应的离子方程式
(5)G在高温下与铝反应的化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A~H为中学化学中常见的物质,转化关系如下图所示,其中圆圈“○”内物质是化合物,方框“□”内的物质是单质,A为医学上治疗胃酸过多的一种药剂,G为淡黄色固体,C在通常状况下为无色液体。
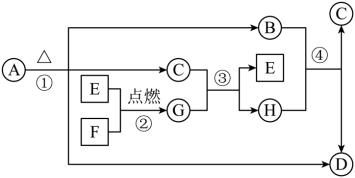
请回答下列问题:
(1)H的化学式为_______ 。
(2)反应①②③④中_______ (填序号)属于氧化还原反应。
(3)在反应③中,每生成1个E,该反应转移电子_______ 个;列举G物质的一个用途_______ 。
(4)检验H中阳离子的常用方法:_______ 和现象:_______ 。
(5)写出下列反应的离子方程式:A与少量澄清石灰水反应:_______ 。
(6)若固体D中混有少量的A,请用化学方程式表示提纯D的方法:_______ 。

请回答下列问题:
(1)H的化学式为
(2)反应①②③④中
(3)在反应③中,每生成1个E,该反应转移电子
(4)检验H中阳离子的常用方法:
(5)写出下列反应的离子方程式:A与少量澄清石灰水反应:
(6)若固体D中混有少量的A,请用化学方程式表示提纯D的方法:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某学校化学兴趣小组从文献资料上获得如下信息: 在潮湿空气中会缓慢分解成
在潮湿空气中会缓慢分解成 、
、 和
和 。为了验证这一信息,该兴趣小组将一瓶在潮湿空气中久置的
。为了验证这一信息,该兴趣小组将一瓶在潮湿空气中久置的 样品混合均匀后,进行如下实验:
样品混合均匀后,进行如下实验:
(1)在一个质量为ag的蒸发皿中加入一些样品,称得总质量为bg。用酒精灯对其充分加热,冷却后称得其总质量为cg。残留在蒸发皿中的固体是_______ (填化学式)。
(2)另取相同质量的样品放入锥形瓶中,实验装置如下图所示。为了保证实验成功,所选用针筒的最大刻度值应大于_______ mL。(设实验在标准状况下进行)
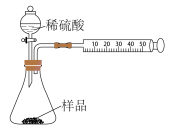
(3)打开活塞逐滴加入稀硫酸,直至没有气泡产生为止。针筒中收集到的气体体积折算成标准状况下的体积为 (滴入稀硫酸的体积及针筒活塞与内壁的摩擦力忽略不计)。该兴趣小组设称取的每份样品中
(滴入稀硫酸的体积及针筒活塞与内壁的摩擦力忽略不计)。该兴趣小组设称取的每份样品中 、
、 的物质的量分别为x、y,且没有利用化学方程式进行计算,就列出算式,
的物质的量分别为x、y,且没有利用化学方程式进行计算,就列出算式, ,他们依据的原理是
,他们依据的原理是_______ 。
 在潮湿空气中会缓慢分解成
在潮湿空气中会缓慢分解成 、
、 和
和 。为了验证这一信息,该兴趣小组将一瓶在潮湿空气中久置的
。为了验证这一信息,该兴趣小组将一瓶在潮湿空气中久置的 样品混合均匀后,进行如下实验:
样品混合均匀后,进行如下实验:(1)在一个质量为ag的蒸发皿中加入一些样品,称得总质量为bg。用酒精灯对其充分加热,冷却后称得其总质量为cg。残留在蒸发皿中的固体是
(2)另取相同质量的样品放入锥形瓶中,实验装置如下图所示。为了保证实验成功,所选用针筒的最大刻度值应大于

(3)打开活塞逐滴加入稀硫酸,直至没有气泡产生为止。针筒中收集到的气体体积折算成标准状况下的体积为
 (滴入稀硫酸的体积及针筒活塞与内壁的摩擦力忽略不计)。该兴趣小组设称取的每份样品中
(滴入稀硫酸的体积及针筒活塞与内壁的摩擦力忽略不计)。该兴趣小组设称取的每份样品中 、
、 的物质的量分别为x、y,且没有利用化学方程式进行计算,就列出算式,
的物质的量分别为x、y,且没有利用化学方程式进行计算,就列出算式, ,他们依据的原理是
,他们依据的原理是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某食品膨松剂作用物质为 ,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。

回答下列问题:
(1)A装置中 溶液的作用是除去空气中的
溶液的作用是除去空气中的______ ,C装置内所盛试剂是______ ,若没有A装置,B装置左侧用橡皮塞封闭,实验结果将______ (填“偏高”、“偏低”或“无影响”)。
(2)E装置的作用是______ ,若没有E装置,测定的结果______ (填“偏高”、“偏低”或“无影响”);
(3)分解产物 是重要化工原料,研究其性质:取少量
是重要化工原料,研究其性质:取少量 溶液,逐滴滴加盐酸,开始没有气泡,反应产生两种盐,推测两种盐的化学式
溶液,逐滴滴加盐酸,开始没有气泡,反应产生两种盐,推测两种盐的化学式______ 。
(4)取a克 与
与 混合物进行下列三组实验,其中能测定
混合物进行下列三组实验,其中能测定 质量分数的是
质量分数的是______ (填序号)。
A.充分加热,质量减少b克
B.与足量稀盐酸充分反应,加热、蒸干,灼烧,得b克固体
C.与足量稀硫酸充分反应,逸出气体用氯化钙吸收,增重b克
 ,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
回答下列问题:
(1)A装置中
 溶液的作用是除去空气中的
溶液的作用是除去空气中的(2)E装置的作用是
(3)分解产物
 是重要化工原料,研究其性质:取少量
是重要化工原料,研究其性质:取少量 溶液,逐滴滴加盐酸,开始没有气泡,反应产生两种盐,推测两种盐的化学式
溶液,逐滴滴加盐酸,开始没有气泡,反应产生两种盐,推测两种盐的化学式(4)取a克
 与
与 混合物进行下列三组实验,其中能测定
混合物进行下列三组实验,其中能测定 质量分数的是
质量分数的是A.充分加热,质量减少b克
B.与足量稀盐酸充分反应,加热、蒸干,灼烧,得b克固体
C.与足量稀硫酸充分反应,逸出气体用氯化钙吸收,增重b克
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】有一含 、
、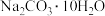 和
和 的混合物,某同学设计如图所示的实验装置,通过测量反应产生的
的混合物,某同学设计如图所示的实验装置,通过测量反应产生的 和
和 的质量,来确定该混合物中各组分的质量分数。
的质量,来确定该混合物中各组分的质量分数。
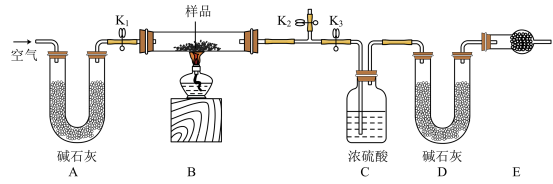
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是______ 。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开弹簧夹 、
、 ,关闭
,关闭 ,缓缓鼓入空气数分钟,其目的是
,缓缓鼓入空气数分钟,其目的是______ 。
④关闭弹簧夹 、
、 ,打开
,打开 ,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为
,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为______ (写出其中一个即可)。
⑤打开弹簧夹 ,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,会分别导致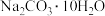 、
、 、
、 的质量分数测定结果
的质量分数测定结果______ 、______ 、______ (填“偏大”、“偏小”、“不影响”)。
②E处干燥管中盛放的药品是碱石灰,其作用是______ ,如果实验中没有该装置,则会导致测量结果 的质量分数
的质量分数______ (填“偏大”“偏小”或“无影响”)。
③若样品质量为 ,反应后C、D装置增加的质量分别为
,反应后C、D装置增加的质量分别为 、
、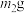 ,则混合物中
,则混合物中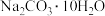 的质量分数为
的质量分数为______ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
 、
、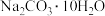 和
和 的混合物,某同学设计如图所示的实验装置,通过测量反应产生的
的混合物,某同学设计如图所示的实验装置,通过测量反应产生的 和
和 的质量,来确定该混合物中各组分的质量分数。
的质量,来确定该混合物中各组分的质量分数。
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开弹簧夹
 、
、 ,关闭
,关闭 ,缓缓鼓入空气数分钟,其目的是
,缓缓鼓入空气数分钟,其目的是④关闭弹簧夹
 、
、 ,打开
,打开 ,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为
,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为⑤打开弹簧夹
 ,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,会分别导致
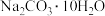 、
、 、
、 的质量分数测定结果
的质量分数测定结果②E处干燥管中盛放的药品是碱石灰,其作用是
 的质量分数
的质量分数③若样品质量为
 ,反应后C、D装置增加的质量分别为
,反应后C、D装置增加的质量分别为 、
、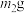 ,则混合物中
,则混合物中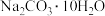 的质量分数为
的质量分数为 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】滴定实验是化学学科中重要的定量实验。
I.酸碱中和滴定——已知某NaOH试样中含有NaCl杂质,为测定试样中NaOH的质量分数,进行如下步骤实验:
①称量1.00g样品溶于水,配成250mL溶液;
②准确量取25.00mL所配溶液于锥形瓶中;
③滴加几滴甲基橙指示剂;
④用0.10mol/L的标准盐酸滴定三次,每次消耗盐酸的体积记录如下:
(1)该酸碱中和滴定(题干中②③④步)所需仪器有___________ (填字母)。
A.酸式滴定管(50mL) B.碱式滴定管(50mL) C.量筒(10mL)
D.铁架台 E.滴定管夹 F.玻璃棒
(2)排去碱式滴定管中气泡的方法应采用操作___________ 。
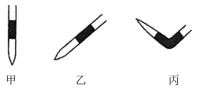
(3)滴定达到终点的现象是___________ 。
(4)试样中NaOH的质量分数为___________ 。
(5)若出现下列情况,测定结果伸高的是___________ 。
a.滴定前用蒸馏水冲洗锥形瓶
b.酸式滴定管滴至终点时,俯视读数
c.酸式滴定管用蒸馏水洗后,未用标准液润洗
d.酸式滴定管尖嘴部分有气泡,滴定后消失
Ⅱ.氧化还原滴定——取草酸( ,弱酸)溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1
,弱酸)溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1 的高锰酸钾溶液滴定。
的高锰酸钾溶液滴定。
(6)发生反应的离子方程式为___________ 。
(7)滴定时, 溶液应装在
溶液应装在___________ 滴定管中(填“酸式”或“碱式”)。
I.酸碱中和滴定——已知某NaOH试样中含有NaCl杂质,为测定试样中NaOH的质量分数,进行如下步骤实验:
①称量1.00g样品溶于水,配成250mL溶液;
②准确量取25.00mL所配溶液于锥形瓶中;
③滴加几滴甲基橙指示剂;
④用0.10mol/L的标准盐酸滴定三次,每次消耗盐酸的体积记录如下:
| 滴定序号 | 待测体积(mL) | 消耗盐酸标准的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 25.00 | 0.50 | 20.60 |
| 2 | 25.00 | 6.00 | 26.00 |
| 3 | 25.00 | 1.10 | 21.00 |
(1)该酸碱中和滴定(题干中②③④步)所需仪器有
A.酸式滴定管(50mL) B.碱式滴定管(50mL) C.量筒(10mL)
D.铁架台 E.滴定管夹 F.玻璃棒
(2)排去碱式滴定管中气泡的方法应采用操作

(3)滴定达到终点的现象是
(4)试样中NaOH的质量分数为
(5)若出现下列情况,测定结果伸高的是
a.滴定前用蒸馏水冲洗锥形瓶
b.酸式滴定管滴至终点时,俯视读数
c.酸式滴定管用蒸馏水洗后,未用标准液润洗
d.酸式滴定管尖嘴部分有气泡,滴定后消失
Ⅱ.氧化还原滴定——取草酸(
 ,弱酸)溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1
,弱酸)溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1 的高锰酸钾溶液滴定。
的高锰酸钾溶液滴定。(6)发生反应的离子方程式为
(7)滴定时,
 溶液应装在
溶液应装在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】从砷化镓废料(主要成分为GaAs,含Fe2O3、SiO2和CaCO3等杂质)中回收镓和砷的工艺流程如图所示:
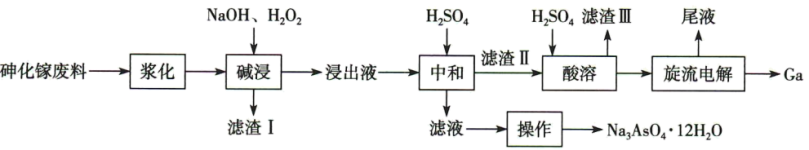
已知:镓(Ga)既能溶于酸也能溶于碱,与NaOH溶液反应生成NaGaO2和H2。
回答下列问题:
(1)“碱浸”的温度控制在70℃左右,温度不能过高的原因是___________ ;“滤渣Ⅱ”的成分为___________ (填化学式)。
(2)向浸出液中加入H2SO4进行“中和”,调节pH使镓和硅共沉淀,不同pH时沉淀率如下表所示。根据表中数据可知,“中和”的pH应调节至___________ 范围内,沉淀的效果最好。
(3)“旋流电解”时用惰性电极,则所得“尾液”的溶质主要是___________ (填化学式),可进行循环利用,提高经济效益。
(4)若用240kg含镓3%的砷化镓废料回收镓,得到纯度为99%的镓7.10kg,则镓的回收率为___________ %。(结果保留一位小数)

已知:镓(Ga)既能溶于酸也能溶于碱,与NaOH溶液反应生成NaGaO2和H2。
回答下列问题:
(1)“碱浸”的温度控制在70℃左右,温度不能过高的原因是
(2)向浸出液中加入H2SO4进行“中和”,调节pH使镓和硅共沉淀,不同pH时沉淀率如下表所示。根据表中数据可知,“中和”的pH应调节至
 | 镓沉淀率/% | 硅沉淀率/% | 砷沉淀率/% |
| 4.0 | 75.0 | 89.2 | 0.02 |
| 5.0 | 98.5 | 98.6 | 0.01 |
| 6.0 | 98.9 | 99.2 | 0.02 |
| 7.0 | 95.3 | 99.5 | 0.06 |
| 8.0 | 86.1 | 86.3 | 0.11 |
| 9.0 | 57.4 | 65.1 | 0.13 |
(3)“旋流电解”时用惰性电极,则所得“尾液”的溶质主要是
(4)若用240kg含镓3%的砷化镓废料回收镓,得到纯度为99%的镓7.10kg,则镓的回收率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】某铝合金中含有铁、铝、镁、铜、硅。为了测定该合金中铝的含量,现设计了如下实验:
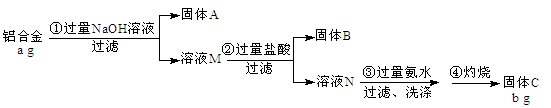
已知:Si+ 2NaOH +H2O= Na2SiO3 + 2H2↑,H2SiO3是不溶于水的弱酸。
(1)固体A的成分是:____________ ,溶液M中的阴离子有:____________________
(2)步骤③中生成沉淀的离子方程式为:_____________________________________
(3)该样品中铝的质量分数是:_______________________________ (用a、b表示)。
(4)下列因操作不当,会使测定结果偏大的是___________

已知:Si+ 2NaOH +H2O= Na2SiO3 + 2H2↑,H2SiO3是不溶于水的弱酸。
(1)固体A的成分是:
(2)步骤③中生成沉淀的离子方程式为:
(3)该样品中铝的质量分数是:
(4)下列因操作不当,会使测定结果偏大的是
| A.第①步中加入NaOH溶液不足 | B.第②步中加入盐酸不足时 |
| C.第④步中的沉淀未用蒸馏水洗涤 | D.第④步对沉淀灼烧不充分 |
您最近一年使用:0次



