以海水浓缩后的卤水为原料, 采用气态膜法提取溴单质的工艺流程如下图所示:

请回答:
(1)“氧化”时,Cl2作________ (填“氧化剂”或“还原剂”),该反应的离子方程式为______ 。
(2)“富集”时,采用了气态膜提溴技术 ,其原理是Br2在分压差的推动下通过气态膜 ,再被NaOH 溶液吸收,该操作与________ ( 填选项字母)相似。
A.过滤 B.渗析 C.分液 D.蒸馏
(3)NaOH溶液与Br2反应生成NaBr 和NaBrO3,则“酸化”时,发生的主要反应的离子方程式为_______ 。
(4)实验室模拟“蒸馏”操作时,冷却蒸气需用到的玻璃仪器为____ ;该工艺与热空气吹出法相比,优点为________

请回答:
(1)“氧化”时,Cl2作
(2)“富集”时,采用了气态膜提溴技术 ,其原理是Br2在分压差的推动下通过气态膜 ,再被NaOH 溶液吸收,该操作与
A.过滤 B.渗析 C.分液 D.蒸馏
(3)NaOH溶液与Br2反应生成NaBr 和NaBrO3,则“酸化”时,发生的主要反应的离子方程式为
(4)实验室模拟“蒸馏”操作时,冷却蒸气需用到的玻璃仪器为
更新时间:2020-07-22 20:31:48
|
相似题推荐
【推荐1】Na2S2O4(保险粉)广泛用于纺织工业的还原性染色、织物的漂白等,它既具有强还原性,又具有强氧化性。回答下列问题:
(1)Ventron公司研发了现场制取保险粉的方法,发生的主要反应为NaBH4 + 8NaHSO3=NaBO2+ 4Na2S2O4+6H2O。该反应属于________ (填“氧化还原反应”或“非氧化还原反应”)。
(2)德国BASF等企业曾用氯碱工业得到的钠汞剂生产保险粉,其反应原理如下:2Na[Hg]+2Na2SO3+2H2O=4NaOH+Na2S2O4+2Hg。该方法得到的产的品中会含有较多Cl-,从环境保护等角度考虑,另一缺点是____________ 。
(3)甲酸钠(HCOONa)法生产保险粉的主要工艺流程如下:

①用甲醇作溶剂的原因除SO2、HCOONa均易溶于甲醇外,还有_________ 。
②“反应釜”中发生反应的化学方程式为____________ 。
③测定产品中Na2S2O4质量分数的主要步骤如下:
称取a g样品,将其加入盛有一定体积的甲醛(HCHO)的烧杯中(Na2S2O4+2HCHO+H2O=NaHSO3·CH2O+NaHSO2·CH2O),溶解后转移到250 mL容量瓶中,用水稀释至刻度线。准确移取25. 00 mL溶液于锥形瓶中,酸化后加入淀粉指示剂并用c mol·L-1的碘标准液滴定(此时只发生反应:NaHSO2·CH2O+2I2+2H2O=NaHSO4 + HCHO+4HI),滴定终点时消耗V mL碘标准溶液。滴定终点的判断依据是______ 样品中Na2S2O4的质量分数为__________ (列出计算表达式即可)。
(1)Ventron公司研发了现场制取保险粉的方法,发生的主要反应为NaBH4 + 8NaHSO3=NaBO2+ 4Na2S2O4+6H2O。该反应属于
(2)德国BASF等企业曾用氯碱工业得到的钠汞剂生产保险粉,其反应原理如下:2Na[Hg]+2Na2SO3+2H2O=4NaOH+Na2S2O4+2Hg。该方法得到的产的品中会含有较多Cl-,从环境保护等角度考虑,另一缺点是
(3)甲酸钠(HCOONa)法生产保险粉的主要工艺流程如下:

①用甲醇作溶剂的原因除SO2、HCOONa均易溶于甲醇外,还有
②“反应釜”中发生反应的化学方程式为
③测定产品中Na2S2O4质量分数的主要步骤如下:
称取a g样品,将其加入盛有一定体积的甲醛(HCHO)的烧杯中(Na2S2O4+2HCHO+H2O=NaHSO3·CH2O+NaHSO2·CH2O),溶解后转移到250 mL容量瓶中,用水稀释至刻度线。准确移取25. 00 mL溶液于锥形瓶中,酸化后加入淀粉指示剂并用c mol·L-1的碘标准液滴定(此时只发生反应:NaHSO2·CH2O+2I2+2H2O=NaHSO4 + HCHO+4HI),滴定终点时消耗V mL碘标准溶液。滴定终点的判断依据是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
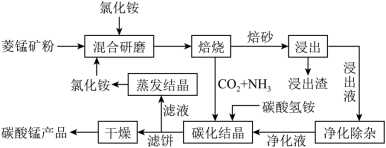
【推荐2】磁性材料产业是21世纪各国竞相发展的高科技支柱产业之一,磁性材料广泛用于电子信息、军事技术等领域。碳酸锰主要用于制备软磁铁氧体,工业上用氯化铵焙烧锰矿粉制备高纯度碳酸锰的工艺流程如下:
已知:①锰和粉的主要成分是 ,还含少量Fe、Al、Ca、Mg等元素。
,还含少量Fe、Al、Ca、Mg等元素。
②相关金属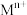 离于
离于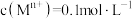 形成
形成 沉淀的pH范围如下:
沉淀的pH范围如下:
回答下列问题:
(1)“焙烧时发生的主要反应的化学方程式为_______ 。
(2)浸出液“净化除杂”过程如下:
①加入 将
将 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为_______ 。
②加入 调节溶液pH范围为
调节溶液pH范围为_______ ,将 、
、 变为沉淀除去。
变为沉淀除去。
(3)碳化结晶时,反应的离子方程式为_______ 。
(4)流程中能循环利用的物质除了氯化铵之外还有_______ 。

已知:①锰和粉的主要成分是
 ,还含少量Fe、Al、Ca、Mg等元素。
,还含少量Fe、Al、Ca、Mg等元素。②相关金属
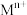 离于
离于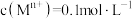 形成
形成 沉淀的pH范围如下:
沉淀的pH范围如下:| 金属离子 |  | 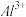 |  |  |  |  |
| 开始沉淀的pH | 1.5 | 3.8 | 6.3 | 9.6 | 10.6 | 8.8 |
| 沉淀完全的pH | 2.8 | 5.2 | 8.3 | 11.6 | 12.6 | 10.8 |
回答下列问题:
(1)“焙烧时发生的主要反应的化学方程式为
(2)浸出液“净化除杂”过程如下:
①加入
 将
将 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为②加入
 调节溶液pH范围为
调节溶液pH范围为 、
、 变为沉淀除去。
变为沉淀除去。(3)碳化结晶时,反应的离子方程式为
(4)流程中能循环利用的物质除了氯化铵之外还有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】废弃化学品循环再利用对节约资源和保护环境有重要意义。钴盐在新能源、催化、印染等领域应用广泛。利用电解工业产生的钴、镍废渣(含Fe、Cu等)制备CoCl2·6H2O,流程如下图所示:

已知:通常认为溶液中离子浓度小于10-5 mol·L-1为沉淀完全;室温下相关物质的Ksp见下表。
回答下列问题:
(1)滤渣Ⅰ的主要成分为Fe(OH)3,H2O2的作用是___________ 。
(2)操作①是___________ ;滤液III对应的溶质是___________ (填化学式);浓盐酸溶解沉淀时,加入NaCl(s)的目的是___________ 。
(3)Co(OH)2易被氧化成Co(OH)3.Co(OH)3可氧化浓盐酸,其化学方程式为___________ 。
(4)浓缩结晶后的母液V可返回___________ 工序循环利用。
(5)利用硫化物分离钴镍离子,向浓度同为0.1 mol·L-1的Ni2+和Co2+混合溶液中逐滴加入(NH4)2S溶液(忽略溶液体积变化),首先生成硫化物沉淀的离子为___________ 。

已知:通常认为溶液中离子浓度小于10-5 mol·L-1为沉淀完全;室温下相关物质的Ksp见下表。
| 物质 | Co(OH)2 | NiS | CoS |
| Ksp | 1×10-14.2 | 1×10-18.5 | 1×10-20.4 |
(1)滤渣Ⅰ的主要成分为Fe(OH)3,H2O2的作用是
(2)操作①是
(3)Co(OH)2易被氧化成Co(OH)3.Co(OH)3可氧化浓盐酸,其化学方程式为
(4)浓缩结晶后的母液V可返回
(5)利用硫化物分离钴镍离子,向浓度同为0.1 mol·L-1的Ni2+和Co2+混合溶液中逐滴加入(NH4)2S溶液(忽略溶液体积变化),首先生成硫化物沉淀的离子为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验仪器的改进和创新,便于我们更好地进行科学探究和物质制备。回答下列问题:
(1)微量实验。如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如表(气体和试剂均充分反应)。

(2)燃烧模拟。用如图装置模拟工业合成盐酸,挤压软塑瓶壁,向锥形瓶中加入溶液A,同时往燃烧管中通入气体C并点燃,可看到明显的燃烧现象(金属网用以防止气体混合爆炸)。下列试剂选择正确的是___________ (填序号)。

(3)晶体制备。
软塑瓶固体B实验室用粗锌(含ZnS杂质)和稀硫酸反应制备H2后的溶液制备皓矾(ZnSO4·7H2O)晶体。
①选择合适仪器并组装抽滤的装置从溶液中得到皓矾晶体,安装顺序为___________ (填标号)。

②抽滤也称减压过滤,下列说法不正确的是___________ (填标号)。
A.抽滤的原理是利用抽气泵使抽滤瓶中的压强降低,以达到固液分离的目的
B.抽滤的优点是过滤速度快,可得到较干燥的沉淀
C.过滤完之后,先关抽气泵,后抽掉抽滤瓶接管
(1)微量实验。如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如表(气体和试剂均充分反应)。

| 序号 | 棉球 | 棉球上滴加试剂的名称 | 实验现象 | 解释或结论 |
| ① | a | 棉球变白,微热后又恢复红色 | 该气体具有漂白性 | |
| ② | b | 含酚酞的NaOH溶液 | 棉球变为白色 | 该气体属于 |
| ③ | c | 碘与淀粉的混合溶液 | 棉球变为白色 | 该气体具有还原性化学方程式为 |
(2)燃烧模拟。用如图装置模拟工业合成盐酸,挤压软塑瓶壁,向锥形瓶中加入溶液A,同时往燃烧管中通入气体C并点燃,可看到明显的燃烧现象(金属网用以防止气体混合爆炸)。下列试剂选择正确的是

| 溶液A | 固体B | 气体C | |
| ① | 浓盐酸 | MnO2 | H2 |
| ② | 稀硝酸 | Fe | Cl2 |
| ③ | 浓盐酸 | KMnO4 | H2 |
(3)晶体制备。
软塑瓶固体B实验室用粗锌(含ZnS杂质)和稀硫酸反应制备H2后的溶液制备皓矾(ZnSO4·7H2O)晶体。
①选择合适仪器并组装抽滤的装置从溶液中得到皓矾晶体,安装顺序为

②抽滤也称减压过滤,下列说法不正确的是
A.抽滤的原理是利用抽气泵使抽滤瓶中的压强降低,以达到固液分离的目的
B.抽滤的优点是过滤速度快,可得到较干燥的沉淀
C.过滤完之后,先关抽气泵,后抽掉抽滤瓶接管
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】海水是一种重要的自然资源。以下是我市对海水资源的部分利用。
(1)从海水中获得氯化钠。将海水进行_____ 可得到粗盐;为除去粗盐中含有的SO42-、Ca2+、Mg2+等杂质,有如下操作:①溶解;②加过量的Na2CO3溶液;③加过量的BaCl2溶液;④加适量的盐酸;⑤加过量NaOH溶液;⑥蒸发结晶;⑦过滤。正确的操作顺序是_________________ 。(用序号填一种合理组合)。
 上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为
上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为__________ ,
由无水MgCl2制取Mg的化学方程式为_____________________________________ 。海
水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:___________________________________________________________ 。
(1)从海水中获得氯化钠。将海水进行
 上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为
上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为由无水MgCl2制取Mg的化学方程式为
水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】粗盐中常含有杂质MgCl2、CaCl2和Na2SO4,为将杂质除尽设计如下步骤,回答下列问题:

(1)试剂③为NaOH溶液,则试剂①是___________ ,试剂②是___________ 。
(2)试剂①的作用是___________ ,试剂②的作用是___________ 。
(3)证明加入试剂③使沉淀完全反应的方法是___________ 。
(4)在滤液中加盐酸的作用是___________ 、___________ (用化学方程式表示)。
(5)操作a的名称是___________ 。

(1)试剂③为NaOH溶液,则试剂①是
(2)试剂①的作用是
(3)证明加入试剂③使沉淀完全反应的方法是
(4)在滤液中加盐酸的作用是
(5)操作a的名称是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】能源、资源、环境日益成为人们关注的主题。
(1)近日习近平向2019世界新能源汽车大会致贺信,为发展氢能源,必须制得廉价氢气。下列可供开发又较经济的一种制氢方法是_______ (填写编号)
①电解水 ②锌和稀硫酸反应 ③利用太阳能,光解海水
(2)某同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案:
方案①:铜与浓硫酸加热直接反应,即Cu→CuSO4
方案②:铜在空气中加热再与稀硫酸反应,即Cu→CuO→CuSO4
这两种方案,你认为哪一种方案更合理并简述理由_______ 。
(3)海带中含有丰富的碘元素.从海带中提取碘单质的工业生产流程如图所示.
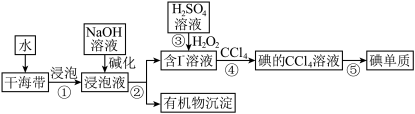
步骤③中双氧水在酸性条件下氧化碘离子的离子方程式是_______ ,步骤④除了CCl4 还可以选用的萃取剂是_______ (填序号)。
a.苯 b.乙醇 c.乙酸 d.乙烷
(1)近日习近平向2019世界新能源汽车大会致贺信,为发展氢能源,必须制得廉价氢气。下列可供开发又较经济的一种制氢方法是
①电解水 ②锌和稀硫酸反应 ③利用太阳能,光解海水
(2)某同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案:
方案①:铜与浓硫酸加热直接反应,即Cu→CuSO4
方案②:铜在空气中加热再与稀硫酸反应,即Cu→CuO→CuSO4
这两种方案,你认为哪一种方案更合理并简述理由
(3)海带中含有丰富的碘元素.从海带中提取碘单质的工业生产流程如图所示.

步骤③中双氧水在酸性条件下氧化碘离子的离子方程式是
a.苯 b.乙醇 c.乙酸 d.乙烷
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】浙江海洋经济发展示范区建设已上升为国家战略,海洋经济将成为浙江经济转型升级发展的重点。请回答下列问题:
(1)被称作海洋元素的是_________ (写元素符号)。
(2)工业上常以食盐为原料制备氯气,请写出化学方程式_______________________ 。
(3)从海水中提取食盐和溴的过程如下:
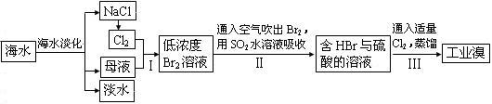
①步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br¯,其目的为富集溴元素,请写出步骤Ⅰ的离子方程式:_____________________ ,
步骤Ⅱ的化学方程式:________________________ 。
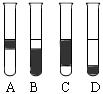
②在3mL溴水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象为图中_____________ 。
(1)被称作海洋元素的是
(2)工业上常以食盐为原料制备氯气,请写出化学方程式
(3)从海水中提取食盐和溴的过程如下:

①步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br¯,其目的为富集溴元素,请写出步骤Ⅰ的离子方程式:
步骤Ⅱ的化学方程式:
②在3mL溴水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象为图中

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】工业生产中,海水提取溴常用空气吹出法。某化学实验小组设计了如下实验装置(夹持装置略去)模拟该法从浓缩的海水中提取溴。
已知:Br2的沸点为58.78℃,密度为3.119g/cm3,微溶于水,有毒。

(1)实验步骤如下:
①关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
②关闭a、c,打开活塞b、d,向A中鼓入足量热空气;
③关闭b,打开a,再通过A向B中通入足量Cl2;
④取B中所得溶液进行蒸馏,收集液溴。
(2)步骤①A中主要反应的离子方程式为______________ 。
(3)X试剂可以是_____ (填序号),步骤②B中X试剂与Br2发生反应的离子方程式为___ 。
a.H2O b. 饱和食盐水 c.饱和Na2SO3溶液
(4)该实验中尾气处理所用的试剂可为___________ 。
(5)蒸馏时,除酒精灯、石棉网、铁架台外,还应该选择仪器_______ (填序号)。蒸馏操作中应控制温度为___________ 。

已知:Br2的沸点为58.78℃,密度为3.119g/cm3,微溶于水,有毒。

(1)实验步骤如下:
①关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
②关闭a、c,打开活塞b、d,向A中鼓入足量热空气;
③关闭b,打开a,再通过A向B中通入足量Cl2;
④取B中所得溶液进行蒸馏,收集液溴。
(2)步骤①A中主要反应的离子方程式为
(3)X试剂可以是
a.H2O b. 饱和食盐水 c.饱和Na2SO3溶液
(4)该实验中尾气处理所用的试剂可为
(5)蒸馏时,除酒精灯、石棉网、铁架台外,还应该选择仪器

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】海水中的化学资源具有巨大的开发潜力。
(1)溴及其化合物广泛用于医药、塑料阻燃剂等。苦卤(含Br-)提溴的工业流程如下:

①用离子方程式表示通入Cl2目的是___________ 。
②吸收塔中盛有Na2CO3溶液,通入足量Br2蒸气时,有BrO 和无色气体生成,反应的离子方程式是
和无色气体生成,反应的离子方程式是___________ 。
(2)用下图所示装置( 表示斜发沸石)分离海水中的K+和Na+,料液(含K+、Na+、Cl-和I-)先流过斜发沸石吸附K+和I-。然后通电,双极膜产生的H+将K+交换下来,OH-将I-交换下来,得到A溶液。
表示斜发沸石)分离海水中的K+和Na+,料液(含K+、Na+、Cl-和I-)先流过斜发沸石吸附K+和I-。然后通电,双极膜产生的H+将K+交换下来,OH-将I-交换下来,得到A溶液。

①简述A溶液中含K+不含Na+的原因:___________ 。
②海水中c(K+)>c(I-),则A溶液中的溶质是___________ 。为了提高产率并防止原料浪费,通电一段时间后,将阴、阳极的斜发沸石对调,继续通电,此时斜发沸石内主要反应的离子方程式是___________ 。
(3)KI广泛用于皮肤科、眼科等疾病的治疗。利用海水中获得的I2和(2)中获得的A溶液及Fe粉,可获得纯度较高的KI晶体,流程如下:
A溶液 溶液I(pH为6~7)
溶液I(pH为6~7) 溶液2
溶液2 KI晶体
KI晶体
已知:ⅰ.KI的溶解度
ⅱ.3I2+6KOH=5KI+KIO3+3H2O
①用化学方程式说明加入Fe粉的作用:___________ 。
②操作1是___________ ,过滤,洗涤,干燥。
(1)溴及其化合物广泛用于医药、塑料阻燃剂等。苦卤(含Br-)提溴的工业流程如下:

①用离子方程式表示通入Cl2目的是
②吸收塔中盛有Na2CO3溶液,通入足量Br2蒸气时,有BrO
 和无色气体生成,反应的离子方程式是
和无色气体生成,反应的离子方程式是(2)用下图所示装置(
 表示斜发沸石)分离海水中的K+和Na+,料液(含K+、Na+、Cl-和I-)先流过斜发沸石吸附K+和I-。然后通电,双极膜产生的H+将K+交换下来,OH-将I-交换下来,得到A溶液。
表示斜发沸石)分离海水中的K+和Na+,料液(含K+、Na+、Cl-和I-)先流过斜发沸石吸附K+和I-。然后通电,双极膜产生的H+将K+交换下来,OH-将I-交换下来,得到A溶液。
①简述A溶液中含K+不含Na+的原因:
②海水中c(K+)>c(I-),则A溶液中的溶质是
(3)KI广泛用于皮肤科、眼科等疾病的治疗。利用海水中获得的I2和(2)中获得的A溶液及Fe粉,可获得纯度较高的KI晶体,流程如下:
A溶液
 溶液I(pH为6~7)
溶液I(pH为6~7) 溶液2
溶液2 KI晶体
KI晶体已知:ⅰ.KI的溶解度
| 温度/℃ | 6 | 20 | 60 | 100 |
| KI的溶解度/g | 128 | 140 | 176 | 206 |
①用化学方程式说明加入Fe粉的作用:
②操作1是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】海洋具有十分巨大的开发潜力,人们可以从海水中获得多种物质.工业上进行海水淡化有多种方法.
(1)蒸馏法是历史悠久,技术和工艺比较成熟的海水淡化方法,如图1是海水蒸馏法装置示意图,仪器B的名称是__________ 。
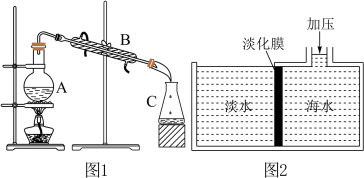
(2)图2是膜分离技术进行淡化的原理示意图,水分子可以透过淡化膜,而海水中其他各种粒子不能通过淡化膜,加压后,右侧海水中减少的是______ (填字母)。
A.溶质质量 B.溶剂质量 C.溶质的物质的量浓度
Ⅱ.从海水中提取一些重要的化工产品的工艺流程如图所示。
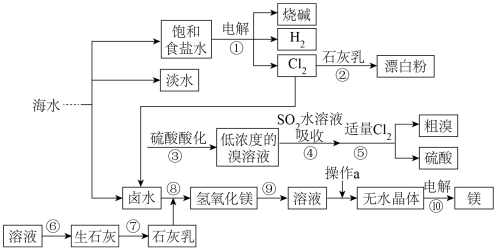
根据上述流程图回答下列问题:
(3)标准状况下22.4 L Cl2气体发生反应②,转移的电子数是________ NA。
(4)过程③到过程⑤的变化为“Br-→Br2→Br-→Br2”,其目的是_______________ 。
(5)过程⑥⑦⑧⑨⑩中没有涉及的化学反应类型是______ 。
A.分解反应 B.化合反应 C.复分解反应 D.置换反应
(6)写出反应④与⑩的化学方程式
④________________________________________________ ;
⑩________________________________________________ 。
(1)蒸馏法是历史悠久,技术和工艺比较成熟的海水淡化方法,如图1是海水蒸馏法装置示意图,仪器B的名称是

(2)图2是膜分离技术进行淡化的原理示意图,水分子可以透过淡化膜,而海水中其他各种粒子不能通过淡化膜,加压后,右侧海水中减少的是
A.溶质质量 B.溶剂质量 C.溶质的物质的量浓度
Ⅱ.从海水中提取一些重要的化工产品的工艺流程如图所示。

根据上述流程图回答下列问题:
(3)标准状况下22.4 L Cl2气体发生反应②,转移的电子数是
(4)过程③到过程⑤的变化为“Br-→Br2→Br-→Br2”,其目的是
(5)过程⑥⑦⑧⑨⑩中没有涉及的化学反应类型是
A.分解反应 B.化合反应 C.复分解反应 D.置换反应
(6)写出反应④与⑩的化学方程式
④
⑩
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】溴及其化合物在医药、农药、染料、阻燃剂等领域有广泛的用途。利用空气吹出法从海水(弱碱性)中提取溴的流程如图。

已知:溴单质的沸点为58.5℃。
(1)溴元素在元素周期表中的位置是_______ 。
(2)“吹出塔”中利用了溴的_______ 性。
(3)“吸收塔”中发生反应的离子方程式为_______ 。
(4)“蒸馏塔”中温度应控制在_______ (填序号)。
A.40~50℃
B.70~80℃
C.100℃以上
(5)物质A_______ (填化学式)可以循环利用,降低成本。
(6)探究“氧化”的适宜条件,测得不同条件下溶液中Br2的含量如图。
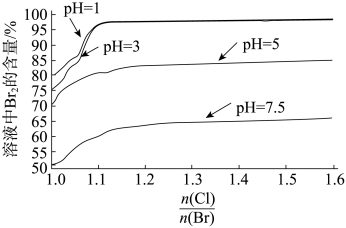
注: 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。
①“氧化”的适宜条件为_______ 。
②用离子方程式说明pH=7.5时溶液中Br2的含量较低的原因:_______ 。

已知:溴单质的沸点为58.5℃。
(1)溴元素在元素周期表中的位置是
(2)“吹出塔”中利用了溴的
(3)“吸收塔”中发生反应的离子方程式为
(4)“蒸馏塔”中温度应控制在
A.40~50℃
B.70~80℃
C.100℃以上
(5)物质A
(6)探究“氧化”的适宜条件,测得不同条件下溶液中Br2的含量如图。

注:
 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。①“氧化”的适宜条件为
②用离子方程式说明pH=7.5时溶液中Br2的含量较低的原因:
您最近一年使用:0次



