某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
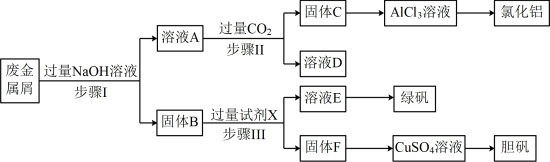
(1)写出步骤Ⅱ反应的离子方程式:________ 。
(2)试剂X是_______ ;溶液D是________ 。
(3)在步骤Ⅱ时,用如图装置制取CO2并通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是_________ 。

(4)由固体F制取硫酸铜溶液,通常有两种方案:
方案一:将固体F在加热条件下与浓硫酸反应;
方案二:将固体F投入热的稀硫酸中,然后通入氧气;
方法一的缺点为:____________ 。

(1)写出步骤Ⅱ反应的离子方程式:
(2)试剂X是
(3)在步骤Ⅱ时,用如图装置制取CO2并通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是

(4)由固体F制取硫酸铜溶液,通常有两种方案:
方案一:将固体F在加热条件下与浓硫酸反应;
方案二:将固体F投入热的稀硫酸中,然后通入氧气;
方法一的缺点为:
更新时间:2020-07-24 21:29:01
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室制取乙烯并检验乙烯性质的装置如图。
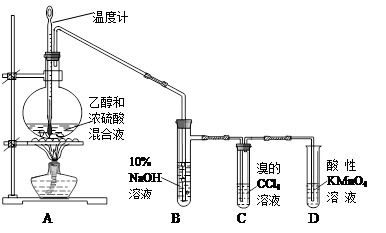
请回答有关问题:
(1)烧瓶中除反应物以外,还应放2-3块碎瓷片,目的是_______ 。
(2)烧瓶中产生乙烯的反应方程式为_______ 。
(3)反应开始后,可观察到C和D中共同的现象是_______ ;C中的反应类型为_______ 反应、D中的反应类型为_______ 反应。
(4)反应结束冷却至室温,处理烧瓶中废液发现,反应液变黑、且有强烈的刺激性气味气体,其原因是_______ ;10%的NaOH溶液起的作用是_______ 。

请回答有关问题:
(1)烧瓶中除反应物以外,还应放2-3块碎瓷片,目的是
(2)烧瓶中产生乙烯的反应方程式为
(3)反应开始后,可观察到C和D中共同的现象是
(4)反应结束冷却至室温,处理烧瓶中废液发现,反应液变黑、且有强烈的刺激性气味气体,其原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】原子序数依次增大的五种短周期元素 ,已知
,已知 同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成—种盐Y;
同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成—种盐Y;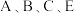 四种元素都能与D元素形成原子个数比不相同的常见化合物,回答下列问题:
四种元素都能与D元素形成原子个数比不相同的常见化合物,回答下列问题:
(1)B在周期表中的位置是___________ 。
(2)D和E形成的一种化合物与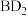 发生氧化还原反应,该反应的化学方程式
发生氧化还原反应,该反应的化学方程式___________ 。
(3)B元素的单质与浓硫酸反应的化学方程式___________ 。
(4)C元素的最高价氧化物的水化物与其氢化物反应的离子方程式________ 。
(5)写出工业制硫酸沸腾炉中进行的反应,煅烧黄铁矿(主要成分 )
)___________ 。
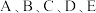 ,已知
,已知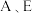 同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成—种盐Y;
同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成—种盐Y;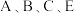 四种元素都能与D元素形成原子个数比不相同的常见化合物,回答下列问题:
四种元素都能与D元素形成原子个数比不相同的常见化合物,回答下列问题:(1)B在周期表中的位置是
(2)D和E形成的一种化合物与
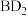 发生氧化还原反应,该反应的化学方程式
发生氧化还原反应,该反应的化学方程式(3)B元素的单质与浓硫酸反应的化学方程式
(4)C元素的最高价氧化物的水化物与其氢化物反应的离子方程式
(5)写出工业制硫酸沸腾炉中进行的反应,煅烧黄铁矿(主要成分
 )
)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2.某同学在实验室中对NH3与NO2反应进行了探究。回答下列问题:
I.某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。
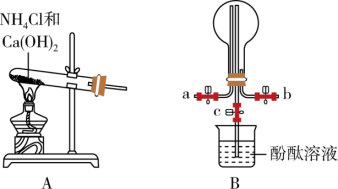
(1)实验室制备氨气的化学方程式为_______ ;B中圆底烧瓶收集氨气时,请你选择氨气的进气口_______ (填“a”或“b”)。
(2)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是_______ 。
(3)将I中收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。
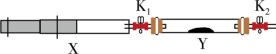
在一定温度下按图示装置进行实验。打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中,反应的化学方程式_______ 。
Ⅱ.硫酸铜可应用于电镀、颜料、医药、农药等方面。下图是探究铜与浓硫酸反应生成硫酸铜的实验装置图:

(4)写出烧瓶中发生反应的化学方程式_______ ;写出图中虚线框内NaOH溶液的作用_______ ,球形干燥管的作用_______ 。
(5)实验结束后,烧瓶中有白色固体生成。写出检验烧瓶中此白色固体是CuSO4的简便方法_______ 。
I.某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。

(1)实验室制备氨气的化学方程式为
(2)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是
(3)将I中收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。

在一定温度下按图示装置进行实验。打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中,反应的化学方程式
Ⅱ.硫酸铜可应用于电镀、颜料、医药、农药等方面。下图是探究铜与浓硫酸反应生成硫酸铜的实验装置图:

(4)写出烧瓶中发生反应的化学方程式
(5)实验结束后,烧瓶中有白色固体生成。写出检验烧瓶中此白色固体是CuSO4的简便方法
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】工业上“中温焙烧——钠化氧化法”回收电镀污泥中的铬已获技术上的突破。其工艺流程如下:
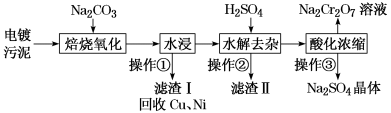
[查阅资料]①电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质;水浸后溶液中含有Na2CrO4、NaAlO2、Na2ZnO2等物质
②Na2SO4、Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表:
请回答:
(1)操作①的名称是___________ , “水浸”后的溶液呈___________ 性
(2)“焙烧氧化”过程中Cr(OH)3转化成Na2CrO4的化学方程式为___________ 。
(3)滤渣Ⅱ的主要成分有Zn(OH)2和X,生成X的离子反应方程式为___________
(4)“酸化浓缩”时,需继续加入H2SO4,使Na2CrO4转化成Na2Cr2O7,反应的离子方程式为___________

[查阅资料]①电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质;水浸后溶液中含有Na2CrO4、NaAlO2、Na2ZnO2等物质
②Na2SO4、Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表:
温度 化学式 | 20 ℃ | 60 ℃ | 100 ℃ |
| Na2SO4 | 19.5 | 45.3 | 42.5 |
| Na2Cr2O7 | 183 | 269 | 415 |
| Na2CrO4 | 84 | 115 | 126 |
(1)操作①的名称是
(2)“焙烧氧化”过程中Cr(OH)3转化成Na2CrO4的化学方程式为
(3)滤渣Ⅱ的主要成分有Zn(OH)2和X,生成X的离子反应方程式为
(4)“酸化浓缩”时,需继续加入H2SO4,使Na2CrO4转化成Na2Cr2O7,反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】某矿石中含有铁、铝、硅的氧化物,为综合开发资源,提高矿石的利用率,某化工厂采取如图所示流程制备铁红和AlCl3•6H2O。

该工艺条件下,有关金属阳离子开始沉淀和完全沉淀的pH如表:
回答下列问题:
(1)基态Fe2+的核外电子排布式为____ 。
(2)进行“酸浸”操作最适合选择的试剂为____ (填名称)。
(3)下列有关说法错误的是____ (填标号)。
(4)“氧化”步骤中,下列试剂最适宜加入的是____ (填标号)。
A.HNO3 B.KMnO4 C.H2O2
其中涉及的离子方程式为____ 。
(5)“调节pH”的范围是____ ;在实验室进行“洗涤”的操作是____ 。

该工艺条件下,有关金属阳离子开始沉淀和完全沉淀的pH如表:
| 金属阳离子 | Fe2+ | Fe3+ | Al3+ |
| 开始沉淀的pH | 9.5 | 2.2 | 3.7 |
| 完全沉淀的pH | 11.1 | 3.1 | 4.7 |
(1)基态Fe2+的核外电子排布式为
(2)进行“酸浸”操作最适合选择的试剂为
(3)下列有关说法错误的是
| A.适当增大酸的浓度可以提高酸浸效率 |
| B.滤渣①的主要成分可用作太阳能电池板 |
| C.“操作1”和“操作2”均为过滤 |
| D.“操作3”需使用的主要仪器为蒸发皿 |
A.HNO3 B.KMnO4 C.H2O2
其中涉及的离子方程式为
(5)“调节pH”的范围是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】叶蛇纹石是一种富镁硅酸盐矿物[主要成分为Mg6(Si4O10)(OH)8,还含有Al2O3、Fe2O3、FeO等杂质],利用该矿物生产铁红(Fe2O3)和碱式碳酸镁的工艺流程如图所示:
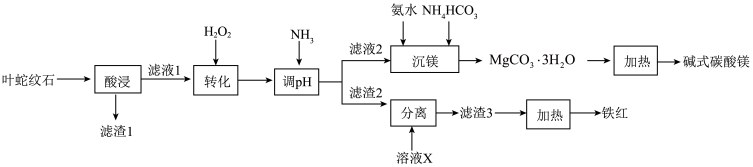
回答下列问题:
(1)“转化”步骤中,温度不能过高的原因是_______ 。“转化”时反应的离子方程式为_______ 。
(2)滤渣2的成分为_______ 。
(3)X通常选用_______ (填化学式)。
(4)“沉镁”步骤中氨水加入的量不能太多,否则MgCO3·H2O的产率会降低,其原因是_______ 。
(5)取9.1g碱式碳酸镁[xMgCO3·yMg(OH)2·zH2O],高温分解后,测得生成3.3gCO2、4.0gMgO,化学式中z=_______ 写出由MgCO3·3H2O生成产品的化学方程式:_______ 。
(6)碱式碳酸镁常用作新型阻燃剂,试分析碱式碳酸镁能够阻燃的原因:_______ 。(写出两点即可)。

回答下列问题:
(1)“转化”步骤中,温度不能过高的原因是
(2)滤渣2的成分为
(3)X通常选用
(4)“沉镁”步骤中氨水加入的量不能太多,否则MgCO3·H2O的产率会降低,其原因是
(5)取9.1g碱式碳酸镁[xMgCO3·yMg(OH)2·zH2O],高温分解后,测得生成3.3gCO2、4.0gMgO,化学式中z=
(6)碱式碳酸镁常用作新型阻燃剂,试分析碱式碳酸镁能够阻燃的原因:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】软锰矿是锰矿石的主要存在形式之一,其主要成分为MnO2,含有SiO2、Fe2O3、MgCO3、CaCO3等杂质,可用于制取在电池领域、涂料工业和农业上均有重要用途的MnSO4.某制备MnSO4的工艺流程如图:

已知:①Fe(OH)3、Mn(OH)2的Ksp分别为1×10-39、4×10-14 ②MnSO4的溶解度随温度变化的曲线如图所示

回答下列问题:
(1)“酸浸还原”发生的主要反应的化学方程式为_______ 。
(2)“酸浸还原”后铁元素的存在形式为_______ ,滤渣1的主要成分是_______ 。
(3)根据绿色化学原则,“氧化”中可替代MnO2的物质是_______ 。若“氧化”后溶液中Mn2+浓度为1 mol/L,则“调pH”时为了确保Fe3+被沉淀完全(离子浓度不超过10-6 mol/L)应控制的pH范围为_______ (已知lg2=0.3)。
(4)“滤渣2”的主要成分是_______ 。
(5)“沉锰”时加入的试剂为氨水-NH4HCO3混合溶液,写出“沉锰”的离子方程式:_______ 。
(6)采用“趁热过滤”操作的目的是_______ 。将分离出硫酸锰晶体后的母液收集起来循环使用,其意义是_______ 。

已知:①Fe(OH)3、Mn(OH)2的Ksp分别为1×10-39、4×10-14 ②MnSO4的溶解度随温度变化的曲线如图所示

回答下列问题:
(1)“酸浸还原”发生的主要反应的化学方程式为
(2)“酸浸还原”后铁元素的存在形式为
(3)根据绿色化学原则,“氧化”中可替代MnO2的物质是
(4)“滤渣2”的主要成分是
(5)“沉锰”时加入的试剂为氨水-NH4HCO3混合溶液,写出“沉锰”的离子方程式:
(6)采用“趁热过滤”操作的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】粗食盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥砂等不溶性杂质。我们食用的精盐是用粗食盐提纯而得到的。通过教材中“粗盐的提纯”及你做过的该实验回答下列问题。
(1)实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯;②固定铁圈位置;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌; ⑤停止加热。其正确的操作顺序为_______ 。
(2)如何运用最简方法检验溶液中 离子是否除尽?
离子是否除尽?________
(3)怎样洗涤沉淀?_______ 。
(4)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:溶解或蒸发时:________ ,过滤时:_______ 。
(1)实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯;②固定铁圈位置;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌; ⑤停止加热。其正确的操作顺序为
(2)如何运用最简方法检验溶液中
 离子是否除尽?
离子是否除尽?(3)怎样洗涤沉淀?
(4)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:溶解或蒸发时:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】三氯氧磷(POCl3)是一种重要的化工原料。现以 、
、 和
和 为原料,采用二级间歇式反应装置模拟联合制备POCl3和氯化亚砜(SOCl2)。实验过程中,控制
为原料,采用二级间歇式反应装置模拟联合制备POCl3和氯化亚砜(SOCl2)。实验过程中,控制 和
和 通入的体积比为1∶1,实验装置如图:
通入的体积比为1∶1,实验装置如图:

已知:
(1)A装置中盛装浓硫酸的仪器名称为___________ 。
(2)A装置的作用为___________ 、___________ 、使气体充分混合。
(3)B、C装置中发生反应的化学方程式为___________ ,分离提纯获得POCl3的实验方法是___________ 。
(4)POCl3水解的方程式为:___________ 。
(5)本实验采用的二级间歇式反应装置,在反应5~6小时后,暂停通入气体。将B瓶拆下,C瓶装在图中B瓶处,并在原C瓶处重新装上一个盛有 的圆底烧瓶。继续通气反应一段时间后重复以上步骤,这种操作的优点是
的圆底烧瓶。继续通气反应一段时间后重复以上步骤,这种操作的优点是___________ 。
(6)通过下列方法可以测定制备的三氯氧磷产品中Cl元素含量,实验步骤如下:
A.取m g产品于锥形瓶中,加入足量NaOH溶液,再加稀硝酸至酸性;
B.向锥形瓶中加入0.1000mol/L的 溶液30.00mL,使
溶液30.00mL,使 完全沉淀;
完全沉淀;
C.向其中加入3mL硝基苯,用力摇动,使沉淀表面被有机物覆盖;
D.加入指示剂,用 溶液滴定过量
溶液滴定过量 至终点,记下所用体积V mL。
至终点,记下所用体积V mL。
已知:AgSCN是白色沉淀。
①滴定选用的指示剂是___________ 。
A.淀粉 B.酚酞 C.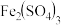 D.
D.
②根据上面实验数据计算产品中氯元素的质量分数为___________ 。(用c、V表示)
 、
、 和
和 为原料,采用二级间歇式反应装置模拟联合制备POCl3和氯化亚砜(SOCl2)。实验过程中,控制
为原料,采用二级间歇式反应装置模拟联合制备POCl3和氯化亚砜(SOCl2)。实验过程中,控制 和
和 通入的体积比为1∶1,实验装置如图:
通入的体积比为1∶1,实验装置如图:
已知:
| 物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
 | -93.6 | 76.1 | 137.5 | 遇水剧烈水解,易与 反应 反应 |
| POCl3 | 1.25 | 105.8 | 153.5 | 遇水剧烈水解,能溶于 |
| SOCl2 | -105 | 78.8 | 119 | 遇水剧烈水解,受热易分解 |
(2)A装置的作用为
(3)B、C装置中发生反应的化学方程式为
(4)POCl3水解的方程式为:
(5)本实验采用的二级间歇式反应装置,在反应5~6小时后,暂停通入气体。将B瓶拆下,C瓶装在图中B瓶处,并在原C瓶处重新装上一个盛有
 的圆底烧瓶。继续通气反应一段时间后重复以上步骤,这种操作的优点是
的圆底烧瓶。继续通气反应一段时间后重复以上步骤,这种操作的优点是(6)通过下列方法可以测定制备的三氯氧磷产品中Cl元素含量,实验步骤如下:
A.取m g产品于锥形瓶中,加入足量NaOH溶液,再加稀硝酸至酸性;
B.向锥形瓶中加入0.1000mol/L的
 溶液30.00mL,使
溶液30.00mL,使 完全沉淀;
完全沉淀;C.向其中加入3mL硝基苯,用力摇动,使沉淀表面被有机物覆盖;
D.加入指示剂,用
 溶液滴定过量
溶液滴定过量 至终点,记下所用体积V mL。
至终点,记下所用体积V mL。已知:AgSCN是白色沉淀。
①滴定选用的指示剂是
A.淀粉 B.酚酞 C.
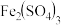 D.
D.
②根据上面实验数据计算产品中氯元素的质量分数为
您最近一年使用:0次



