该研究性学习小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略).已知:Cl2易溶于CCl4而HCl不溶于CCl4
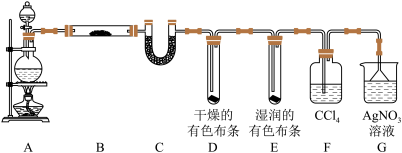
按要求回答问题:
(1)写出装置A制取Cl2的化学方程式_____ 。
(2)装置B中的试剂是__ ,现象是________ 。
(3)装置D和E中出现的不同现象说明的问题是____ 。
(4)装置F的作用是____ 。
(5)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种,为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在F和D之间再连接一个洗气瓶装置,则装置中应放入_____ (填写试剂或用品名称),改正后证明有HCl挥发出来的现象是_______ 。

按要求回答问题:
(1)写出装置A制取Cl2的化学方程式
(2)装置B中的试剂是
(3)装置D和E中出现的不同现象说明的问题是
(4)装置F的作用是
(5)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种,为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在F和D之间再连接一个洗气瓶装置,则装置中应放入
19-20高一下·河北衡水·期末 查看更多[2]
(已下线)必考点09 氯气的制取 氯离子的检验-【对点变式题】2021-2022学年高一化学上学期期中期末必考题精准练(人教版2019)河北省衡水市深州市中学2019-2020学年高一下学期期末考试化学试题
更新时间:2020-07-29 20:42:43
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】纯净干燥的氯气与熔融金属锡反应可制备SnCl4,某化学小组的同学设计了如下实验装置进行制备。
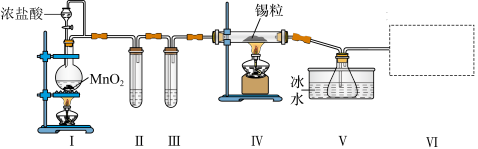
已知:①金属锡熔点为231℃,化学活泼性与铁相似;②SnCl4的沸点为114℃;③SnCl4易与水反应。
请根据上图装置回答:
(1)装置I中反应的离子方程式是________________________________________
(2)试管II中的试剂是________ ,试管III中的试剂是____________ 。
(3)装置V的作用是____________ 。
(4)装置Ⅵ 最好选用下列装置中的________ (填标号)。
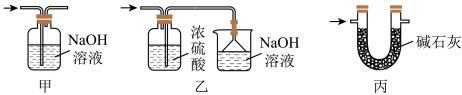
(5)实验结束后,欲回收利用装置Ⅰ中未反应完的MnO2,需要的玻璃仪器有_________ 。

已知:①金属锡熔点为231℃,化学活泼性与铁相似;②SnCl4的沸点为114℃;③SnCl4易与水反应。
请根据上图装置回答:
(1)装置I中反应的离子方程式是
(2)试管II中的试剂是
(3)装置V的作用是
(4)装置Ⅵ 最好选用下列装置中的

(5)实验结束后,欲回收利用装置Ⅰ中未反应完的MnO2,需要的玻璃仪器有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】阅读下列科普短文并填空:
海洋约占地球表面积的 ,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和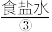 用以生产
用以生产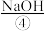 、
、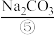 、
、 、
、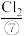 、
、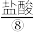 等,苦卤经过氯气氧化,热空气吹出、
等,苦卤经过氯气氧化,热空气吹出、 吸收等一系列操作可获得
吸收等一系列操作可获得 。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
(1)实验室可用_______ 、_______ (填化学式)溶液检验①中的阴离子。
(2)实验室可用MnO2与⑧的浓溶液在加热条件下制取⑦,请写出其离子方程式_______ ,100mL 12 mol·L-1的盐酸溶液与足量的MnO2反应实际生成的气体体积(标准状况下)_______ 6.72L(填“>”、“<”或“=”)。
(3)实验室需要220 mL 0.1 mol·L-1 ⑤的溶液,应该用托盘天平称取Na2CO3·10H2O晶体质量为_______ g;配制溶液所需仪器除烧杯、量筒、玻璃棒、胶头滴管外,还必须用到的一种玻璃仪器为_______ 。
(4)下列操作使配制的溶液物质的量浓度的偏低的是_______。
(5)海水提溴的过程中涉及的反应有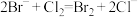 ,
, ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为_______ 。潮湿的Cl2和SO2都具有漂白性,将其混合后其漂白性_______ (填“增强”、“减弱”或“无影响”)
海洋约占地球表面积的
 ,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和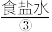 用以生产
用以生产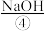 、
、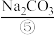 、
、 、
、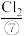 、
、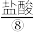 等,苦卤经过氯气氧化,热空气吹出、
等,苦卤经过氯气氧化,热空气吹出、 吸收等一系列操作可获得
吸收等一系列操作可获得 。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。(1)实验室可用
(2)实验室可用MnO2与⑧的浓溶液在加热条件下制取⑦,请写出其离子方程式
(3)实验室需要220 mL 0.1 mol·L-1 ⑤的溶液,应该用托盘天平称取Na2CO3·10H2O晶体质量为
(4)下列操作使配制的溶液物质的量浓度的偏低的是_______。
| A.定容时俯视刻度线 |
| B.转移前,容量瓶内有蒸馏水 |
| C.定容时水加多了用胶头滴管吸出 |
| D.称量是将砝码放在托盘天平的左盘(托盘天平1g以下用游码) |
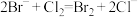 ,
, ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室用如图所示装置进行氯气性质的探究并制备无水FeCl3。查阅相关资料可知:①无水FeCl3在空气中易潮解,加热易升华;②碱石灰的主要成分是氧化钙和氢氧化钠的混合物。

(1)仪器a的名称为___________ ,实验室以二氧化锰和浓盐酸为原料制备氯气的化学方程式为 ___________ 。
(2)装置B的作用是___________ ,同时用作安全瓶(监测实验时装置C中是否发生堵塞)。
(3)装置C的作用是验证氯气是否具有漂白性,为此,实验时装置C中Ⅰ、Ⅱ、Ⅲ处依次放入的物质是___________ (填字母)。
(4)装置D中发生反应的化学方程式为___________ 。
(5)E中冷水的作用是___________ 。
(6)装置E中的导管应接虚线框中的___________ (填“e、f、g或h”),其作用是 ___________ 。

(1)仪器a的名称为
(2)装置B的作用是
(3)装置C的作用是验证氯气是否具有漂白性,为此,实验时装置C中Ⅰ、Ⅱ、Ⅲ处依次放入的物质是
| A | B | C | D | |
| Ⅰ | 干燥的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 无水氯化钙 | 无水氯化钙 | 浓硫酸 |
| Ⅲ | 湿润的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 干燥的有色布条 |
(4)装置D中发生反应的化学方程式为
(5)E中冷水的作用是
(6)装置E中的导管应接虚线框中的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除产生二氧化硫气体外,还可能产生氢气。为了验证哪位同学的判断正确,丙同学设计了如下图所示的实验装置(锌与浓硫酸共热时产生的气体为X,且该装置略去。已知C为CuO)。试回答:

(1)上述反应中能生成二氧化硫的化学方程式为___________ 。
(2)乙同学认为还可能产生氢气的理由是___________ 。
(3)A中加入的试剂可能是___________ ,作用是___________ 。B中加入的试剂可能是___________ ,作用是___________ 。
(4)可以证明气体X中含有氢气的实验现象是C中:___________ ,D中:___________ 。
(5)如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?___________ (填“能”或“不能”),原因是___________ 。
(6)下列有关硫及其化合物的叙述正确的是___________ 。
A.食品中添加适量二氧化硫可以起到防腐和抗氧化等作用
B.硫在足量空气中燃烧生成SO3
C.向SO2水溶液中滴加BaCl2溶液,会生成BaSO3白色沉淀
D.浓硫酸与蔗糖反应的实验体现了浓硫酸的脱水性和强氧化性
E.除去SO2中含有的少量HCl气体,可以使气体通过饱和Na2SO3溶液

(1)上述反应中能生成二氧化硫的化学方程式为
(2)乙同学认为还可能产生氢气的理由是
(3)A中加入的试剂可能是
(4)可以证明气体X中含有氢气的实验现象是C中:
(5)如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?
(6)下列有关硫及其化合物的叙述正确的是
A.食品中添加适量二氧化硫可以起到防腐和抗氧化等作用
B.硫在足量空气中燃烧生成SO3
C.向SO2水溶液中滴加BaCl2溶液,会生成BaSO3白色沉淀
D.浓硫酸与蔗糖反应的实验体现了浓硫酸的脱水性和强氧化性
E.除去SO2中含有的少量HCl气体,可以使气体通过饱和Na2SO3溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质。甲同学设计了如图所示的实验装置(部分支撑用的铁架台省略)。
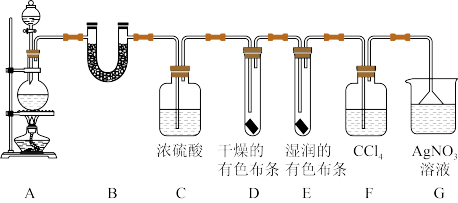
按要求回答下列问题。
(1)若用含有7.3 g HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2总是小于3.55 g的原因是__ 。
(2)①装置B中盛放的试剂名称为____ ,作用是_____ ,现象是_____ 。
②装置D和E中出现的不同现象说明的问题是_____ 。
③装置F的作用是______ 。
④写出装置G中发生反应的离子方程式_____ 。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在______ 与______ 之间(填装置标号),装置中应放入_______ (填试剂或用品名称)。

按要求回答下列问题。
(1)若用含有7.3 g HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2总是小于3.55 g的原因是
(2)①装置B中盛放的试剂名称为
②装置D和E中出现的不同现象说明的问题是
③装置F的作用是
④写出装置G中发生反应的离子方程式
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
您最近一年使用:0次
【推荐3】Ⅰ.测定 样品的纯度可用标准
样品的纯度可用标准 溶液进行滴定,取
溶液进行滴定,取 样品溶解酸化后,用
样品溶解酸化后,用 标准
标准 溶液进行滴定,标准
溶液进行滴定,标准 溶液应盛装在
溶液应盛装在________  填“酸式”或“碱式”
填“酸式”或“碱式” 滴定管中。实验中,滴定至终点时消耗
滴定管中。实验中,滴定至终点时消耗 溶液
溶液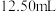 ,则该样品中
,则该样品中 的质量分数是
的质量分数是________ 。 有关离子方程式为:
有关离子方程式为:
Ⅱ.铁矿石中含铁量的测定

(1)步骤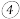 中煮沸的作用是
中煮沸的作用是________ 。
(2)步骤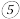 中用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还有
中用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还有________ 。
(3)下列有关步骤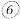 的操作中说法正确的是
的操作中说法正确的是________ 。
 因为碘水为黄色,所以滴定过程中不需加指示剂
因为碘水为黄色,所以滴定过程中不需加指示剂
 滴定过程中可利用淀粉溶液作为指示剂
滴定过程中可利用淀粉溶液作为指示剂
 滴定管用蒸馏水洗涤后可以直接装液
滴定管用蒸馏水洗涤后可以直接装液
 锥形瓶不需要用待测液润洗
锥形瓶不需要用待测液润洗
 滴定过程中,眼睛注视滴定管中液面变化
滴定过程中,眼睛注视滴定管中液面变化
 滴定结束后,
滴定结束后, 内溶液不恢复原来的颜色,再读数
内溶液不恢复原来的颜色,再读数
Ⅲ.一些食品添加剂、抗氧化剂中含有焦亚硫酸钠 ,大量的焦亚硫酸钠会损伤细胞,具有生物毒性。已知:
,大量的焦亚硫酸钠会损伤细胞,具有生物毒性。已知: 溶于水会生成
溶于水会生成 。检验
。检验 晶体在空气中已被氧化的实验方法是
晶体在空气中已被氧化的实验方法是________ 。
Ⅳ 某化学兴趣小组用铜和浓硫酸制取
某化学兴趣小组用铜和浓硫酸制取 ,并依次检验
,并依次检验 具有酸性氧化物的性质和还原性、漂白性、氧化性,所用仪器如下图所示
具有酸性氧化物的性质和还原性、漂白性、氧化性,所用仪器如下图所示 图中连接胶管、夹持和加热装置省略
图中连接胶管、夹持和加热装置省略 :
:

查阅资料可知: 的酸性强弱与
的酸性强弱与 相近。
相近。
上述装置的接口连接顺序依次是
________ 
________ 
________ 
________  填导管接口字母
填导管接口字母 。
。
 样品的纯度可用标准
样品的纯度可用标准 溶液进行滴定,取
溶液进行滴定,取 样品溶解酸化后,用
样品溶解酸化后,用 标准
标准 溶液进行滴定,标准
溶液进行滴定,标准 溶液应盛装在
溶液应盛装在 填“酸式”或“碱式”
填“酸式”或“碱式” 滴定管中。实验中,滴定至终点时消耗
滴定管中。实验中,滴定至终点时消耗 溶液
溶液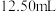 ,则该样品中
,则该样品中 的质量分数是
的质量分数是 有关离子方程式为:
有关离子方程式为:
Ⅱ.铁矿石中含铁量的测定

(1)步骤
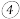 中煮沸的作用是
中煮沸的作用是(2)步骤
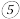 中用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还有
中用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还有(3)下列有关步骤
 的操作中说法正确的是
的操作中说法正确的是 因为碘水为黄色,所以滴定过程中不需加指示剂
因为碘水为黄色,所以滴定过程中不需加指示剂 滴定过程中可利用淀粉溶液作为指示剂
滴定过程中可利用淀粉溶液作为指示剂 滴定管用蒸馏水洗涤后可以直接装液
滴定管用蒸馏水洗涤后可以直接装液 锥形瓶不需要用待测液润洗
锥形瓶不需要用待测液润洗 滴定过程中,眼睛注视滴定管中液面变化
滴定过程中,眼睛注视滴定管中液面变化 滴定结束后,
滴定结束后, 内溶液不恢复原来的颜色,再读数
内溶液不恢复原来的颜色,再读数Ⅲ.一些食品添加剂、抗氧化剂中含有焦亚硫酸钠
 ,大量的焦亚硫酸钠会损伤细胞,具有生物毒性。已知:
,大量的焦亚硫酸钠会损伤细胞,具有生物毒性。已知: 溶于水会生成
溶于水会生成 。检验
。检验 晶体在空气中已被氧化的实验方法是
晶体在空气中已被氧化的实验方法是Ⅳ
 某化学兴趣小组用铜和浓硫酸制取
某化学兴趣小组用铜和浓硫酸制取 ,并依次检验
,并依次检验 具有酸性氧化物的性质和还原性、漂白性、氧化性,所用仪器如下图所示
具有酸性氧化物的性质和还原性、漂白性、氧化性,所用仪器如下图所示 图中连接胶管、夹持和加热装置省略
图中连接胶管、夹持和加热装置省略 :
:
查阅资料可知:
 的酸性强弱与
的酸性强弱与 相近。
相近。上述装置的接口连接顺序依次是




 填导管接口字母
填导管接口字母 。
。
您最近一年使用:0次



