现有 与
与 的混合溶液,为了分析混合溶液中
的混合溶液,为了分析混合溶液中 与
与 的质量分数,设计如下实验方案:取四份混合溶液各
的质量分数,设计如下实验方案:取四份混合溶液各 ,分别缓慢加入到
,分别缓慢加入到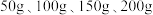 某
某 溶液中,测得四组实验数据如表:
溶液中,测得四组实验数据如表:
(1) 混合溶液与
混合溶液与 溶液完全反应生成沉淀的质量为
溶液完全反应生成沉淀的质量为______ g。
(2)试求出混合溶液中 的溶质质量分数是
的溶质质量分数是______ ?(写出计算过程)
(3)混合溶液中 的溶质质量分数为
的溶质质量分数为______ 。
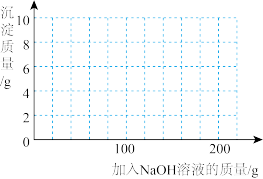
(4)若在 混合溶液中不断加入上述
混合溶液中不断加入上述 的溶液,请画出加入
的溶液,请画出加入 溶液的质量与所产生沉淀质量的关系图
溶液的质量与所产生沉淀质量的关系图______ 。(在答题卡的坐标图中作图)
 与
与 的混合溶液,为了分析混合溶液中
的混合溶液,为了分析混合溶液中 与
与 的质量分数,设计如下实验方案:取四份混合溶液各
的质量分数,设计如下实验方案:取四份混合溶液各 ,分别缓慢加入到
,分别缓慢加入到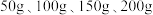 某
某 溶液中,测得四组实验数据如表:
溶液中,测得四组实验数据如表: | 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | 第Ⅳ组 | |
 溶液的质量 溶液的质量 | 50 | 100 | 150 | 200 |
生成沉淀的质量 | 0 | 2.45 | 7.35 | 9.8 |
(1)
 混合溶液与
混合溶液与 溶液完全反应生成沉淀的质量为
溶液完全反应生成沉淀的质量为(2)试求出混合溶液中
 的溶质质量分数是
的溶质质量分数是(3)混合溶液中
 的溶质质量分数为
的溶质质量分数为(4)若在
 混合溶液中不断加入上述
混合溶液中不断加入上述 的溶液,请画出加入
的溶液,请画出加入 溶液的质量与所产生沉淀质量的关系图
溶液的质量与所产生沉淀质量的关系图
更新时间:2020-08-04 19:30:50
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】为测定某一混合铵盐的成分(主要含有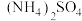 和
和 ),将不同质量的样品分别加入到
),将不同质量的样品分别加入到 浓度相同的
浓度相同的 溶液中,沸水浴加热至气体全部逸出(此温度下该铵盐不分解)。气体干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量如下表所示:
溶液中,沸水浴加热至气体全部逸出(此温度下该铵盐不分解)。气体干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量如下表所示:
(1)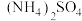 和
和 的物质的量之比
的物质的量之比______ ;
(2) 溶液的物质的量浓度为
溶液的物质的量浓度为______  ;
;
(3)第三次实验时浓硫酸增加的质量a的值为______ 。
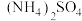 和
和 ),将不同质量的样品分别加入到
),将不同质量的样品分别加入到 浓度相同的
浓度相同的 溶液中,沸水浴加热至气体全部逸出(此温度下该铵盐不分解)。气体干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量如下表所示:
溶液中,沸水浴加热至气体全部逸出(此温度下该铵盐不分解)。气体干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量如下表所示:| 实验次数 | 1 | 2 | 3 | 4 |
铵盐质量/ | 9.05 | 18.10 | 27.15 | 36.2 |
浓硫酸增重/ | 1.7 | 1.7 |  | 0 |
(1)
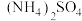 和
和 的物质的量之比
的物质的量之比(2)
 溶液的物质的量浓度为
溶液的物质的量浓度为 ;
;(3)第三次实验时浓硫酸增加的质量a的值为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】过碳酸钠是一种多用途的新型漂白剂,化学式可表示为 ,过碳酸钠溶于水分解成
,过碳酸钠溶于水分解成 和
和 。
。
测定某样品中过碳酸钠化学式的实验步骤如下(样品中杂质不参加反应):
步骤I:称取样品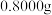 于锥形瓶中,加水溶解,用
于锥形瓶中,加水溶解,用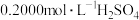 溶液与其反应,恰好反应时消耗硫酸
溶液与其反应,恰好反应时消耗硫酸 。
。
步骤II:另称取样品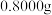 于锥形瓶中,加水溶解,加稀
于锥形瓶中,加水溶解,加稀 酸化,用
酸化,用 溶液与其反应,恰好反应时消耗
溶液与其反应,恰好反应时消耗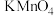 溶液
溶液 。
。
已知 与
与 反应的化学方程式如下:
反应的化学方程式如下: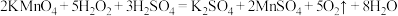
(1)步骤II中,若样品溶于水酸化后放置一段时间,然后再进行反应,则过碳酸钠化学式中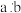 的测定结果将
的测定结果将_______ (填“偏大”或“偏小”或“无影响”)。
(2)通过计算确定该过碳酸钠化学式(写出计算过程)_______ 。
 ,过碳酸钠溶于水分解成
,过碳酸钠溶于水分解成 和
和 。
。测定某样品中过碳酸钠化学式的实验步骤如下(样品中杂质不参加反应):
步骤I:称取样品
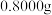 于锥形瓶中,加水溶解,用
于锥形瓶中,加水溶解,用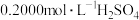 溶液与其反应,恰好反应时消耗硫酸
溶液与其反应,恰好反应时消耗硫酸 。
。步骤II:另称取样品
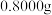 于锥形瓶中,加水溶解,加稀
于锥形瓶中,加水溶解,加稀 酸化,用
酸化,用 溶液与其反应,恰好反应时消耗
溶液与其反应,恰好反应时消耗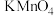 溶液
溶液 。
。已知
 与
与 反应的化学方程式如下:
反应的化学方程式如下: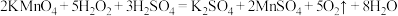
(1)步骤II中,若样品溶于水酸化后放置一段时间,然后再进行反应,则过碳酸钠化学式中
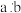 的测定结果将
的测定结果将(2)通过计算确定该过碳酸钠化学式(写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】铁粉和氧化亚铁粉末的混合物共9.2克,加入到150毫升的稀硫酸中,恰好完全反应,得到氢气2.24升(标准状况)。试求:
(1)混合物中铁和氧化亚铁的质量。
(2)原稀硫酸的物质的量浓度。
(1)混合物中铁和氧化亚铁的质量。
(2)原稀硫酸的物质的量浓度。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】硫酸亚铁与氢氧化钠制备氢氧化亚铁的过程中会出现一种绿色物质A(只含Fe、S、O、H四种元素)。称取此物质32.200g,用稀盐酸溶液恰好完全溶解后,配成250mL样品溶液待用。
(1)硫酸亚铁片可以用于治疗缺铁性贫血症,每片含铁元素0.111g,则一瓶60片的药品中硫酸亚铁的质量为___ g。
(2)移取样品溶液50.00mL,加入0.560g铁粉正好完全反应,得到溶液B(假设溶液体积不变)。根据以上数据可计算出32.200gA物质中铁离子的物质的量为___ mol。
(3)将B溶液稀释成500mL后取出20.00mL,用0.0250mol.L-1KMnO4溶液滴定至终点,消耗KMnO4溶液22.40mL。试计算:
①B溶液中Fe2+的物质的量浓度___ 。
②32.200gA物质中亚铁离子的物质的量___ 。
(4)移取样品溶液100.00mL,加入足量BaCl2溶液,过滤、烘干、冷却,得固体9.320g。根据计算结果写出A的化学式___ 。
(1)硫酸亚铁片可以用于治疗缺铁性贫血症,每片含铁元素0.111g,则一瓶60片的药品中硫酸亚铁的质量为
(2)移取样品溶液50.00mL,加入0.560g铁粉正好完全反应,得到溶液B(假设溶液体积不变)。根据以上数据可计算出32.200gA物质中铁离子的物质的量为
(3)将B溶液稀释成500mL后取出20.00mL,用0.0250mol.L-1KMnO4溶液滴定至终点,消耗KMnO4溶液22.40mL。试计算:
①B溶液中Fe2+的物质的量浓度
②32.200gA物质中亚铁离子的物质的量
(4)移取样品溶液100.00mL,加入足量BaCl2溶液,过滤、烘干、冷却,得固体9.320g。根据计算结果写出A的化学式
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】某校课外活动小组为测定已部分脱水的生石膏的组成(xCaSO4·yH2O),做如下实验:将固体加热,测量剩余固体的质量随时间的变化关系,如图所示。
(1)t5~ t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色的气体物质的量是___ ;
(2)x∶y=______ 。

(1)t5~ t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色的气体物质的量是
(2)x∶y=
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】质量、物质的量、物质的量浓度等是用于化学计算的常见物理量。
(1)质量之比为16:7:6的三种气体 、CO、NO。分子个数之比为
、CO、NO。分子个数之比为_______ ;氧原子个数之比为_______ ;相同条件下的体积之比为_______ 。
(2)标准状况下,17g 的体积为
的体积为_______ ,含有氢原子个数为_______ ,它与标准状况下_______ L  含有相同数目的氢原子。
含有相同数目的氢原子。
(3)某气体氧化物的化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为_______ ,R的相对原子质量为_______ 。
(4)同温同压下, 气体与
气体与 气体等体积化合,生成
气体等体积化合,生成 气体,已知反应前后气体的密度不变,则
气体,已知反应前后气体的密度不变,则 的分子式为
的分子式为_______ 。
(5)在t℃时将a g 完全溶于水得到V mL溶液,该溶液的密度为
完全溶于水得到V mL溶液,该溶液的密度为 ;质量分数为w,物质的量浓度为c
;质量分数为w,物质的量浓度为c  。下列计算结果正确的是
。下列计算结果正确的是
(6)将a L  和
和 的混合溶液分成两等份,一份加入b mol
的混合溶液分成两等份,一份加入b mol  溶液使溶液中的
溶液使溶液中的 刚好完全沉定,另一份加入足量NaOH溶液并加热可得到c mol
刚好完全沉定,另一份加入足量NaOH溶液并加热可得到c mol ,则原溶液中
,则原溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(7)将0.24g Mg和0.27g Al的混合物投入到100mL 1mol/L的盐酸中,充分反应后固体完全溶解。向所得溶液中加入2mol/L的NaOH溶液,恰好使金属离子全部沉淀完全。写出加入NaOH溶液发生的相关离子方程式_______ ,需要NaOH溶液的体积为_______ mL。
(8)常温下A和B两种气体组成的混合物(A的摩尔质量大于B的摩尔质量),经分析混合气体中只含有C、O元素:
①当混合物中C、O的质量比总是小于3:8时,混合气体中A和B分别是_______ 、_______ 。
②当混合物中C、O的质量比为1:2时,混合气体中A的体积百分数为_______ 。
(1)质量之比为16:7:6的三种气体
 、CO、NO。分子个数之比为
、CO、NO。分子个数之比为(2)标准状况下,17g
 的体积为
的体积为 含有相同数目的氢原子。
含有相同数目的氢原子。(3)某气体氧化物的化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为(4)同温同压下,
 气体与
气体与 气体等体积化合,生成
气体等体积化合,生成 气体,已知反应前后气体的密度不变,则
气体,已知反应前后气体的密度不变,则 的分子式为
的分子式为(5)在t℃时将a g
 完全溶于水得到V mL溶液,该溶液的密度为
完全溶于水得到V mL溶液,该溶液的密度为 ;质量分数为w,物质的量浓度为c
;质量分数为w,物质的量浓度为c  。下列计算结果正确的是
。下列计算结果正确的是A.溶质的质量分数 |
B.溶质的物质的量浓度 |
C.溶液密度 可表示为 可表示为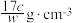 |
| D.上述溶液中再加入V mL水,所得溶液溶质的质量分数小于0.5w |
 和
和 的混合溶液分成两等份,一份加入b mol
的混合溶液分成两等份,一份加入b mol  溶液使溶液中的
溶液使溶液中的 刚好完全沉定,另一份加入足量NaOH溶液并加热可得到c mol
刚好完全沉定,另一份加入足量NaOH溶液并加热可得到c mol ,则原溶液中
,则原溶液中 的物质的量浓度为
的物质的量浓度为(7)将0.24g Mg和0.27g Al的混合物投入到100mL 1mol/L的盐酸中,充分反应后固体完全溶解。向所得溶液中加入2mol/L的NaOH溶液,恰好使金属离子全部沉淀完全。写出加入NaOH溶液发生的相关离子方程式
(8)常温下A和B两种气体组成的混合物(A的摩尔质量大于B的摩尔质量),经分析混合气体中只含有C、O元素:
①当混合物中C、O的质量比总是小于3:8时,混合气体中A和B分别是
②当混合物中C、O的质量比为1:2时,混合气体中A的体积百分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】某硫酸厂用接触法制硫酸:
(1)在煅烧黄铁矿时损失硫5%(质量分数,下同);在SO2的催化氧化时,SO3的产率为92%;在吸收塔中损失SO3 0.6%。现有含FeS295%的黄铁矿(杂质不含硫元素)100t,可制得98%的浓硫酸_____________ t。
(2)若该厂每小时生产at 98%(质量分数)硫酸。为使硫充分燃烧,且在下一步催化氧化时不再补充空气,要求燃烧后的混合气体中含氧气的体积分数为b%。若空气中氧气的体积分数为21%,且不考虑各生产阶段的物料损失,则该厂每小时消耗标准状况下空气的体积为_________ m3,b%的下限等于__________ 。
(3)接触法制硫酸排放的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2(循环利用)和混合铵盐。为测定此铵盐中氮元素的质量分数,将不同质量的铵盐样品分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。部分测定结果如下:
①铵盐质量为10.000 g和20.000 g时,浓硫酸增加的质量相同;
②铵盐质量为30.000 g时,浓硫酸质量增重0.680 g;
③铵盐质量为40.000 g时,浓硫酸的质量不变。
通过计算推理求解该铵盐的成分和铵盐样品中氮元素的质量分数_____ 。(写出计算推理过程,计算结果用小数表示,并保留3位小数)
(1)在煅烧黄铁矿时损失硫5%(质量分数,下同);在SO2的催化氧化时,SO3的产率为92%;在吸收塔中损失SO3 0.6%。现有含FeS295%的黄铁矿(杂质不含硫元素)100t,可制得98%的浓硫酸
(2)若该厂每小时生产at 98%(质量分数)硫酸。为使硫充分燃烧,且在下一步催化氧化时不再补充空气,要求燃烧后的混合气体中含氧气的体积分数为b%。若空气中氧气的体积分数为21%,且不考虑各生产阶段的物料损失,则该厂每小时消耗标准状况下空气的体积为
(3)接触法制硫酸排放的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2(循环利用)和混合铵盐。为测定此铵盐中氮元素的质量分数,将不同质量的铵盐样品分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。部分测定结果如下:
①铵盐质量为10.000 g和20.000 g时,浓硫酸增加的质量相同;
②铵盐质量为30.000 g时,浓硫酸质量增重0.680 g;
③铵盐质量为40.000 g时,浓硫酸的质量不变。
通过计算推理求解该铵盐的成分和铵盐样品中氮元素的质量分数
您最近一年使用:0次




