将一定量的氯气通入30 mL浓度为10.00 mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断不正确的是
| A.与NaOH反应的氯气一定为0.15 mol |
| B.n(Na+)∶n(Cl-) 可能为7∶3 |
| C.若反应中转移的电子为n mol,则n一定大于0.15 mol |
| D.n(NaCl)∶n(NaClO)∶n(NaClO3)可能为7∶2∶1 |
11-12高三下·上海浦东新·阶段练习 查看更多[5]
浙江省宁波中学2021-2022学年高一上学期期中考试化学试题(已下线)【新东方】2020-90(已下线)【新东方】2020-89(已下线)2013-2014浙江省宁波效实中学高一下学期期末考试化学试卷(已下线)2012届上海市浦东新区高三下学期4月质量抽测化学试卷
更新时间:2016-12-09 03:08:24
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】将1.52 g铜镁合金完全溶解于50 mL密度为1.40 g·mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL (标准状况),向反应后的溶液中加入浓度为1.0 mol·L-1的 NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀,下列说法不正确的是
| A.该合金中铜与镁的物质的量之比是16∶3 |
| B.该浓硝酸中HNO3的物质的量浓度是14.0 mol·L-1 |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.反应中转移电子的物质的量为0.06 mol |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】取铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生0.896L.NO2气体和0.672 L N2O4的气体(气体体积都已折算到标准状况),在反应后的溶液中加足量的氢氧化钠溶液,生成沉淀质量为3.7g。则合金中铜与镁的物质的量之比等于
| A.1 :1 | B.2 :1 | C.2 :3 | D.3 :2 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】做实验时不小心使皮肤上沾上了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸(乙二酸)的稀溶液洗涤,黑斑可以迅速褪去,其离子方程式为:MnO4-+H2C2O4+H+=CO2↑+Mn2++ 。下列有关叙述正确的是
| A.发生还原反应的是H2C2O4 |
| B.该离子方程式右侧横线上的产物是OH- |
| C.10molH+参加反应时,电子转移5mol |
| D.该反应的氧化剂为KMnO4 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4反应中,被氧化的P原子与被还原的P原子个数比是
| A.11:5 | B.5:6 | C.6:5 | D.11:6 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列离子方程式书写正确的是
A.将氯气通入冷的石灰乳中: |
B. 与稀硫酸的反应: 与稀硫酸的反应: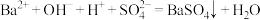 |
C.澄清石灰水与过量的小苏打溶液反应: |
D.将碳酸氢钠溶液和硫酸氢钠溶液混合: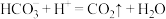 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
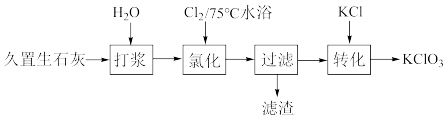
【推荐2】用久置于空气中的生石灰【主要成分为CaO,还含有 和
和 】制取
】制取 的流程如下图所示。下列有关说法不正确的是
的流程如下图所示。下列有关说法不正确的是
 和
和 】制取
】制取 的流程如下图所示。下列有关说法不正确的是
的流程如下图所示。下列有关说法不正确的是
| A.“打浆”的目的是为了提高“氯化”时的反应速率 |
B.“氯化”中主要发生的反应为: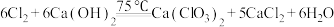 |
C.“过滤”后的滤渣中含有 |
D.“转化”时发生的化学反应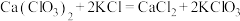 属于氧化还原反应 属于氧化还原反应 |
您最近半年使用:0次

 溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是
溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是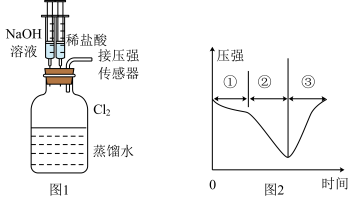
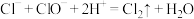
 换成
换成 ,则压强变化不会出现图2趋势
,则压强变化不会出现图2趋势

