元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的离子半径逐渐减小;化合物XN常温下为气体。据此回答:
(1)M在周期表的位置__________ ;X、Y、Z三种元素组成化合物的电子式为__________ ;
(2)N的最高价氧化物对应水化物的化学式为:__________ 。
(3)M与Fe与氢氧化钠溶液构成原电池,其负极反应式为:__________ ;
(4)Z的最高价氧化物的水化物和M的最高价氧化物反应的离子方程为__________
(1)M在周期表的位置
(2)N的最高价氧化物对应水化物的化学式为:
(3)M与Fe与氢氧化钠溶液构成原电池,其负极反应式为:
(4)Z的最高价氧化物的水化物和M的最高价氧化物反应的离子方程为
更新时间:2020-08-11 12:48:02
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】有关物质的转化关系如下图所示(部分物质和条件已略去)。A是金属单质,D是非金属单质,B、F是气体且B无色无味,G是最常见的无色液体。
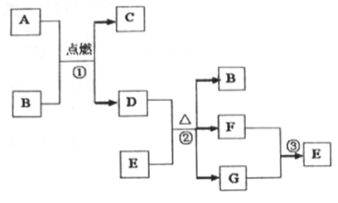
请回答下列问题:
(1)C的化学式为:______________ 。
(2)B的电子式为:______________ 。
(3)写出③的离子方程式:__________________ 。
(4)写出②的化学方程式,并用“单线桥”标出电子转移的方向和数目________________ 。

请回答下列问题:
(1)C的化学式为:
(2)B的电子式为:
(3)写出③的离子方程式:
(4)写出②的化学方程式,并用“单线桥”标出电子转移的方向和数目
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z、W、R、T为核电荷数依次增大的前4周期主族元素,X与Y、Z与W均为同周期相邻元素,W、T同主族;Y元素最外层电子数是内层电子数的3倍,Z元素形成的简单离子半径在同周期中最小,R元素最外层电子数等于X的质子数。回答下列问题:
(1)W的元素符号为_______ ,Z元素的离子结构示意图为_______ 。
(2)X元素原子的得电子能力_______ (填“强”或“弱”)于Y,请用原子结构的知识解释原因_______ 。
(3)实验室制备R元素单质的离子方程式为_______ 。
(4)X的气态氢化物与R的气态氢化物可以发生反应,其反应产物的电子式为_______ 。
(5)T在元素周期表中的位置为_______ ,W、T的简单气态氢化物的稳定性较强的是_______ (填氢化物化学式)。
(1)W的元素符号为
(2)X元素原子的得电子能力
(3)实验室制备R元素单质的离子方程式为
(4)X的气态氢化物与R的气态氢化物可以发生反应,其反应产物的电子式为
(5)T在元素周期表中的位置为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。

(1)元素Ga在元素周期表中的位置为_______ (写出周期和族)。
(2)Sn的最高正价为_______ ,As的气态氢化物的化学式为_______ 。
(3)根据元素周期律推断,P、S、Cl三种元素的原子半径由小到大的顺序是_______ (填元素符号);阴影部分元素氢化物热稳定性最高的是_______ (填化学式): 、
、 的酸性强弱:
的酸性强弱:
_______ (填“>”“<”或“=”) 。
。
(4)可在图中分界线(虚线部分)附近寻找_______(填字母)。
(5)① 常用作分析试剂,分子中各原子都满足8电子结构,两个Se原子之间直接形成共价键,其电子式为
常用作分析试剂,分子中各原子都满足8电子结构,两个Se原子之间直接形成共价键,其电子式为_______ 。
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是_______ (填字母,可多选)。
A.原子半径: B.In的金属性比Se强
B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为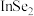
③工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气, 被溶液中的
被溶液中的 氧化为
氧化为 及
及 ,反应中
,反应中 与
与 的物质的量之比为
的物质的量之比为_______ 。

(1)元素Ga在元素周期表中的位置为
(2)Sn的最高正价为
(3)根据元素周期律推断,P、S、Cl三种元素的原子半径由小到大的顺序是
 、
、 的酸性强弱:
的酸性强弱:
 。
。(4)可在图中分界线(虚线部分)附近寻找_______(填字母)。
| A.优良的催化剂 | B.半导体材料 | C.合金材料 | D.农药 |
 常用作分析试剂,分子中各原子都满足8电子结构,两个Se原子之间直接形成共价键,其电子式为
常用作分析试剂,分子中各原子都满足8电子结构,两个Se原子之间直接形成共价键,其电子式为②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是
A.原子半径:
 B.In的金属性比Se强
B.In的金属性比Se强C.In的金属性比Al弱 D.硒化铟的化学式为
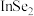
③工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,
 被溶液中的
被溶液中的 氧化为
氧化为 及
及 ,反应中
,反应中 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
【推荐1】CO、SO2是主要的大气污染气体,利用化学反应原理是治理污染的重要方法。
I.甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产。工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g) CH3OH(g) △H1=-116kJ·mol-1
CH3OH(g) △H1=-116kJ·mol-1
(1)下列措施中有利于增大该反应的反应速率的是___ ;
A.随时将CH3OH与反应混合物分离 B.降低反应温度
C.增大体系压强 D.使用高效催化剂
(2)已知:CO(g)+2H2(g) CH3OH(g) △H1=-116kJ·mol-1
CH3OH(g) △H1=-116kJ·mol-1
CO(g)+ O2(g)=CO2(g) △H2=-283kJ·mol-1
O2(g)=CO2(g) △H2=-283kJ·mol-1
H2(g)+ O2(g)=H2O(g) △H3
O2(g)=H2O(g) △H3
则△H3=___ ,表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式为___ ;
Ⅱ.当温度高于500 K时,科学家成功利用二氧化碳和氢气合成了乙醇,2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g)。这在节能减排、降低碳排放方面具有重大意义。回答下列问题:
C2H5OH(g)+3H2O(g)。这在节能减排、降低碳排放方面具有重大意义。回答下列问题:
(1)其平衡常数表达式为K=____ 。
(2)在恒容密闭容器中,判断上述反应达到平衡状态的依据是___ 。
a.体系压强不再改变 b.H2的浓度不再改变
c.气体的密度不随时间改变 d.单位时间内消耗H2和CO2的物质的量之比为3∶1
(3)在一定压强下,测得由CO2制取CH3CH2OH的实验数据中,起始投料比、温度与CO2的转化率的关系如图。根据图中数据分析:
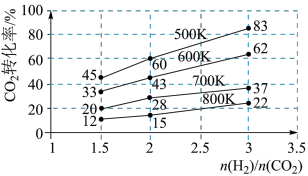
①降低温度,平衡向____ 方向移动。
②在700K、起始投料比 =1.5时,H2的转化率为
=1.5时,H2的转化率为___ 。
③在500K、起始投料比 =2时,达到平衡后H2的浓度为amol·L-1,则达到平衡时CH3CH2OH的浓度为
=2时,达到平衡后H2的浓度为amol·L-1,则达到平衡时CH3CH2OH的浓度为___ 。
Ⅲ.某学习小组以SO2为原料,采用原电池法制取硫酸。该小组设计的原电池原理如图所示。该电池中右侧为___ 极,写出该电池负极的电极反应式___ 。
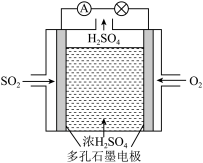
I.甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产。工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)
 CH3OH(g) △H1=-116kJ·mol-1
CH3OH(g) △H1=-116kJ·mol-1(1)下列措施中有利于增大该反应的反应速率的是
A.随时将CH3OH与反应混合物分离 B.降低反应温度
C.增大体系压强 D.使用高效催化剂
(2)已知:CO(g)+2H2(g)
 CH3OH(g) △H1=-116kJ·mol-1
CH3OH(g) △H1=-116kJ·mol-1CO(g)+
 O2(g)=CO2(g) △H2=-283kJ·mol-1
O2(g)=CO2(g) △H2=-283kJ·mol-1H2(g)+
 O2(g)=H2O(g) △H3
O2(g)=H2O(g) △H3| 化学键 | H—H | O=O | O—H |
| 键能/KJ▪mol-1 | 436 | 498 | 463.5 |
则△H3=
Ⅱ.当温度高于500 K时,科学家成功利用二氧化碳和氢气合成了乙醇,2CO2(g)+6H2(g)
 C2H5OH(g)+3H2O(g)。这在节能减排、降低碳排放方面具有重大意义。回答下列问题:
C2H5OH(g)+3H2O(g)。这在节能减排、降低碳排放方面具有重大意义。回答下列问题:(1)其平衡常数表达式为K=
(2)在恒容密闭容器中,判断上述反应达到平衡状态的依据是
a.体系压强不再改变 b.H2的浓度不再改变
c.气体的密度不随时间改变 d.单位时间内消耗H2和CO2的物质的量之比为3∶1
(3)在一定压强下,测得由CO2制取CH3CH2OH的实验数据中,起始投料比、温度与CO2的转化率的关系如图。根据图中数据分析:

①降低温度,平衡向
②在700K、起始投料比
 =1.5时,H2的转化率为
=1.5时,H2的转化率为③在500K、起始投料比
 =2时,达到平衡后H2的浓度为amol·L-1,则达到平衡时CH3CH2OH的浓度为
=2时,达到平衡后H2的浓度为amol·L-1,则达到平衡时CH3CH2OH的浓度为Ⅲ.某学习小组以SO2为原料,采用原电池法制取硫酸。该小组设计的原电池原理如图所示。该电池中右侧为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示:

(图中的ΔH表示生成1mol产物的数据)。
①P和Cl2反应生成PCl3的热化学方程式是___ 。
②PCl5分解成PCl3和Cl2的热化学方程式是___ 。
(2)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700oC的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g) ΔH=-1591.2kJ/mol,则该反应每转移1mole-,可放出的热量为
Si3N4(s)+6CO(g) ΔH=-1591.2kJ/mol,则该反应每转移1mole-,可放出的热量为___ kJ。
(3)高温时,用CO还原MgSO4可制备高纯MgO。
①750℃时,测得气体中含等物质的量的SO2和SO3,此时反应的化学方程式是:___ 。
②由MgO制成的Mg可构成“镁—次氯酸盐”电池,其装置示意图如图,该电池的正极反应式为___ 。


(图中的ΔH表示生成1mol产物的数据)。
①P和Cl2反应生成PCl3的热化学方程式是
②PCl5分解成PCl3和Cl2的热化学方程式是
(2)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700oC的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g)
 Si3N4(s)+6CO(g) ΔH=-1591.2kJ/mol,则该反应每转移1mole-,可放出的热量为
Si3N4(s)+6CO(g) ΔH=-1591.2kJ/mol,则该反应每转移1mole-,可放出的热量为(3)高温时,用CO还原MgSO4可制备高纯MgO。
①750℃时,测得气体中含等物质的量的SO2和SO3,此时反应的化学方程式是:
②由MgO制成的Mg可构成“镁—次氯酸盐”电池,其装置示意图如图,该电池的正极反应式为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】资料显示,水溶液中 与
与 发生互促水解生成蓝色沉淀
发生互促水解生成蓝色沉淀 。某小组同学设计实验探究水溶液中
。某小组同学设计实验探究水溶液中 与
与 反应的产物。
反应的产物。
实验记录如下:将 溶液逐滴加入盐酸酸化的
溶液逐滴加入盐酸酸化的 溶液中,溶液蓝色变浅,有白色沉淀生成。
溶液中,溶液蓝色变浅,有白色沉淀生成。
(1) 溶液用盐酸酸化的目的是
溶液用盐酸酸化的目的是___________ 。
(2)查阅资料得知,该白色沉淀是 。写出产生
。写出产生 的离子方程式:
的离子方程式:___________ 。
(3)甲同学认为:要证明 氧化了
氧化了 ,可检验溶液中含有
,可检验溶液中含有 。操作为:取少量上层清液于试管中,
。操作为:取少量上层清液于试管中,___________ (将操作和现象补充完整)。
(4)乙同学认为:溶液中存在 不一定是
不一定是 氧化的,体系中存在的
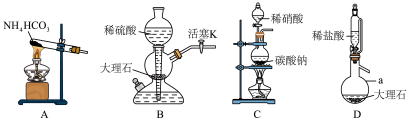
氧化的,体系中存在的 会干扰实验,于是设计了如下4个装置排除体系中的
会干扰实验,于是设计了如下4个装置排除体系中的 。其中合理的是
。其中合理的是___________ (填字母),仪器a的名称是___________ 。
(5)丙同学认为: 的还原性大
的还原性大 ,也可与盐酸酸化的
,也可与盐酸酸化的 溶液反应生成
溶液反应生成 沉淀,你认为是否合理,如果合理,简述你的实验方案,如果不合理,说明理由:
沉淀,你认为是否合理,如果合理,简述你的实验方案,如果不合理,说明理由:___________ 。
(6)称取沉淀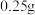 与过量氯化铁溶液反应,待样品完全溶解后,加水
与过量氯化铁溶液反应,待样品完全溶解后,加水 、邻菲啰啉溶液2滴,用
、邻菲啰啉溶液2滴,用 硫酸铈
硫酸铈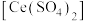 标准溶液滴定,滴定终点时消耗标准溶液
标准溶液滴定,滴定终点时消耗标准溶液 (已知:
(已知:
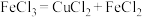 ,
, )。邻菲啰啉溶液的作用是
)。邻菲啰啉溶液的作用是___________ ,沉淀中 的质量分数为
的质量分数为___________ 。
 与
与 发生互促水解生成蓝色沉淀
发生互促水解生成蓝色沉淀 。某小组同学设计实验探究水溶液中
。某小组同学设计实验探究水溶液中 与
与 反应的产物。
反应的产物。实验记录如下:将
 溶液逐滴加入盐酸酸化的
溶液逐滴加入盐酸酸化的 溶液中,溶液蓝色变浅,有白色沉淀生成。
溶液中,溶液蓝色变浅,有白色沉淀生成。(1)
 溶液用盐酸酸化的目的是
溶液用盐酸酸化的目的是(2)查阅资料得知,该白色沉淀是
 。写出产生
。写出产生 的离子方程式:
的离子方程式:(3)甲同学认为:要证明
 氧化了
氧化了 ,可检验溶液中含有
,可检验溶液中含有 。操作为:取少量上层清液于试管中,
。操作为:取少量上层清液于试管中,(4)乙同学认为:溶液中存在
 不一定是
不一定是 氧化的,体系中存在的
氧化的,体系中存在的 会干扰实验,于是设计了如下4个装置排除体系中的
会干扰实验,于是设计了如下4个装置排除体系中的 。其中合理的是
。其中合理的是
(5)丙同学认为:
 的还原性大
的还原性大 ,也可与盐酸酸化的
,也可与盐酸酸化的 溶液反应生成
溶液反应生成 沉淀,你认为是否合理,如果合理,简述你的实验方案,如果不合理,说明理由:
沉淀,你认为是否合理,如果合理,简述你的实验方案,如果不合理,说明理由:(6)称取沉淀
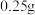 与过量氯化铁溶液反应,待样品完全溶解后,加水
与过量氯化铁溶液反应,待样品完全溶解后,加水 、邻菲啰啉溶液2滴,用
、邻菲啰啉溶液2滴,用 硫酸铈
硫酸铈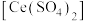 标准溶液滴定,滴定终点时消耗标准溶液
标准溶液滴定,滴定终点时消耗标准溶液 (已知:
(已知:
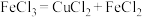 ,
, )。邻菲啰啉溶液的作用是
)。邻菲啰啉溶液的作用是 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、C同周期,A、D同主族,A、C常温下能形成两种液态化合物A2C和A2C2,E元素的周期序数与主族序数相等。请用化学用语回答下列问题:
(1)E元素在周期表中的位置为___________ ,请写出E的最高价氧化物对应水化物的电离方程式:___________ 。
(2)C、D、E三种元素对应简单离子半径从大到小的顺序为(用离子符号表示) ___________>___________>___________,___________ ;由A、B、C三种元素组成的18电子微粒的分子式 为___________ 。
(3)用电子式表示BC2的形成过程:___________ 。
(4)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出该反应的离子方程式:___________ 。
(1)E元素在周期表中的位置为
(2)C、D、E三种元素对应简单离子半径从大到小的顺序为(用离子符号表示) ___________>___________>___________,
(3)用电子式表示BC2的形成过程:
(4)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出该反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下图为短周期表的一部分,其中E为地壳中含量最高的元素。

请完成下列问题:
(1)D元素在元素周期表中的位置:_______ 。
(2)A、E简单离子的半径由大到小顺序为_______ (用具体的微粒符号表示,下同) 。
(3)写出A和F两种元素的最高价氧化物的水化物相互反应的离子方程式_______ 。
(4)工业用C的单质与 B的最高价氧化物制备B单质的化学方程式_______ 。
(5)证明元素F和G的非金属性强弱(用化学方程式表示)_______ 。

请完成下列问题:
(1)D元素在元素周期表中的位置:
(2)A、E简单离子的半径由大到小顺序为
(3)写出A和F两种元素的最高价氧化物的水化物相互反应的离子方程式
(4)工业用C的单质与 B的最高价氧化物制备B单质的化学方程式
(5)证明元素F和G的非金属性强弱(用化学方程式表示)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】短周期元素X、Y、Z、W的原子序数依次增大,Z的一种常见氧化物是形成酸雨的罪魁祸首。X、Y、W可组成化合物I,I和Ca(OH)2共热的关系图如图:
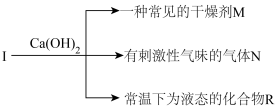
(1)W的元素符号为_______ ;Z原子的结构示意图为_______ 。
(2)I、N的电子式分别为_______ 、_______ 。
(3)I和Ca(OH)2共热的化学方程式为_______ 。
(4)I、M、N、R中离子化合物有_______ ;共价化合物有_______ 。

(1)W的元素符号为
(2)I、N的电子式分别为
(3)I和Ca(OH)2共热的化学方程式为
(4)I、M、N、R中离子化合物有
您最近一年使用:0次



