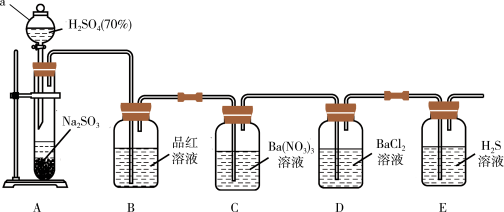
利用下图所示装置制取SO2并验证其部分性质(夹持装置已省略)。
已知: Na2SO3+ H2SO4(浓)=Na2SO4+ SO2↑+H2O
回答下列问题:
(1)仪器a的名称为______ ;装置B中品红溶液褪色,说明SO2具有______ 性。
(2)装置C中有白色沉淀生成,则该白色沉淀为_________ (填化学式) 。
(3)装置D中无白色沉淀产生,再向其中通入______ (填标号) 气体仍不会产生沉淀。
a.Cl2 b.NH3 c.O2 d.CO2
(4)装置E中有淡黄色沉淀生成,则该反应的化学方程式为_____________ 。
(5)该实验装置的缺陷是________________ 。
已知: Na2SO3+ H2SO4(浓)=Na2SO4+ SO2↑+H2O

回答下列问题:
(1)仪器a的名称为
(2)装置C中有白色沉淀生成,则该白色沉淀为
(3)装置D中无白色沉淀产生,再向其中通入
a.Cl2 b.NH3 c.O2 d.CO2
(4)装置E中有淡黄色沉淀生成,则该反应的化学方程式为
(5)该实验装置的缺陷是
更新时间:2020-08-17 17:16:23
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】SO2可用作漂白剂、食品添加剂等。某兴趣小组用如下装置制取SO2,并验证其性质:

(1)盛放 的仪器名称为
的仪器名称为___________ 。
(2)D装置用于吸收尾气。在答题卡虚线框内画出D装置图,并注明所用试剂___________ 。
(3)进行实验,观察并记录现象,做出相应解释。

(1)盛放
 的仪器名称为
的仪器名称为(2)D装置用于吸收尾气。在答题卡虚线框内画出D装置图,并注明所用试剂
(3)进行实验,观察并记录现象,做出相应解释。
| 实验操作 | 实验现象 | 分析与解释 |
| 打开装置A中的漏斗活塞 | A装置中有气泡产生 | 化学方程式为 |
| B装置中浸润过品红溶液的滤纸a的颜色 |  具有 具有 | |
B装置中浸润过酸性 溶液的滤纸b褪色 溶液的滤纸b褪色 |  具有 具有 | |
| C装置中的现象是 |  具有氧化性 具有氧化性 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如下图所示的实验。请据此回答下列问题:
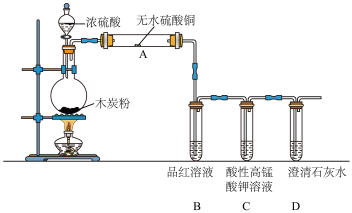
(1)连接好装置后(未加试剂),检验该装置的气密性的操作是:_____ 。
(2)实验过程中圆底烧瓶内发生反应的化学方程式为_____ 。
(3)A装置现象是_____ ,证明产物中_____ 生成(填写化学式,下同)。
(4)B装置现象是_____ ,证明产物中有_____ 生成。
(5)D装置现象是_____ ,证明产物中有_____ 生成。
(6)C装置的作用是_____ ,发生反应的离子方程式是_____ 。

(1)连接好装置后(未加试剂),检验该装置的气密性的操作是:
(2)实验过程中圆底烧瓶内发生反应的化学方程式为
(3)A装置现象是
(4)B装置现象是
(5)D装置现象是
(6)C装置的作用是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】二氧化硫具有漂白性,工业上常用二氧化硫来漂白纸浆、毛、丝、草帽等。此外二氧化硫还能够抑制霉菌和细菌的滋生,可用作防腐剂。
Ⅰ.甲组同学拟利用 粉与浓硫酸反应制取
粉与浓硫酸反应制取 (标准状况下)
(标准状况下) 。实验方案设计如下:取
。实验方案设计如下:取 粉与
粉与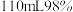 的浓硫酸(含
的浓硫酸(含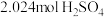 )混合,加热充分反应,待
)混合,加热充分反应,待 粉全部溶解后,干燥并收集气体。
粉全部溶解后,干燥并收集气体。
(1)写出 粉与浓硫酸反应制备
粉与浓硫酸反应制备 的化学方程式:
的化学方程式:__________________ 。
(2)乙组同学认为:按甲组同学实验方案无法达到实验目的,并且制得气体应该含有杂质,该杂质为_________ (填化学式)。
(3)为了检验甲组同学所制气体的成分,乙组同学按甲组同学的实验方案制备气体,并设计了如图所示的实验装置进行检验。(已知酸性高锰酸钾溶液及B中试剂均过量)
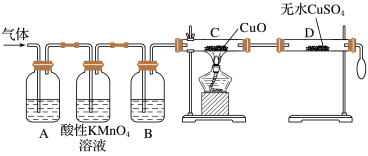
①A中试剂是品红溶液,作用是____________ 。
②B中所装试剂为____________ 。
③证明气体中混有杂质气体的实验现象是:________ 。
Ⅱ. 是常见的大气污染物,燃煤是产生
是常见的大气污染物,燃煤是产生 的主要原因。
的主要原因。
(4)工业上有多种方法可以减少 的排放。往煤中添加一些石灰石,可使燃煤过程中产生的
的排放。往煤中添加一些石灰石,可使燃煤过程中产生的 转化成硫酸钙,该反应的化学方程式是
转化成硫酸钙,该反应的化学方程式是___________ 。
(5)丙组同学认为 溶液可以做
溶液可以做 的吸收液,从而减少实验室
的吸收液,从而减少实验室 的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
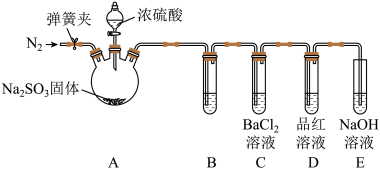
已知: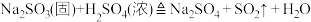
反应开始后,B、C试管中除了有气泡外,未见其他现象;D中红色褪去。通过乙组同学的实验,得出的结论是___________ 。
Ⅰ.甲组同学拟利用
 粉与浓硫酸反应制取
粉与浓硫酸反应制取 (标准状况下)
(标准状况下) 。实验方案设计如下:取
。实验方案设计如下:取 粉与
粉与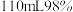 的浓硫酸(含
的浓硫酸(含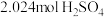 )混合,加热充分反应,待
)混合,加热充分反应,待 粉全部溶解后,干燥并收集气体。
粉全部溶解后,干燥并收集气体。(1)写出
 粉与浓硫酸反应制备
粉与浓硫酸反应制备 的化学方程式:
的化学方程式:(2)乙组同学认为:按甲组同学实验方案无法达到实验目的,并且制得气体应该含有杂质,该杂质为
(3)为了检验甲组同学所制气体的成分,乙组同学按甲组同学的实验方案制备气体,并设计了如图所示的实验装置进行检验。(已知酸性高锰酸钾溶液及B中试剂均过量)

①A中试剂是品红溶液,作用是
②B中所装试剂为
③证明气体中混有杂质气体的实验现象是:
Ⅱ.
 是常见的大气污染物,燃煤是产生
是常见的大气污染物,燃煤是产生 的主要原因。
的主要原因。(4)工业上有多种方法可以减少
 的排放。往煤中添加一些石灰石,可使燃煤过程中产生的
的排放。往煤中添加一些石灰石,可使燃煤过程中产生的 转化成硫酸钙,该反应的化学方程式是
转化成硫酸钙,该反应的化学方程式是(5)丙组同学认为
 溶液可以做
溶液可以做 的吸收液,从而减少实验室
的吸收液,从而减少实验室 的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
已知:
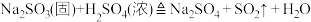
反应开始后,B、C试管中除了有气泡外,未见其他现象;D中红色褪去。通过乙组同学的实验,得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某校化学兴趣小组按如图所示装置进行实验,验证木炭与浓硫酸反应放出的气体是 、
、 和少量CO。回答下列问题:
和少量CO。回答下列问题:
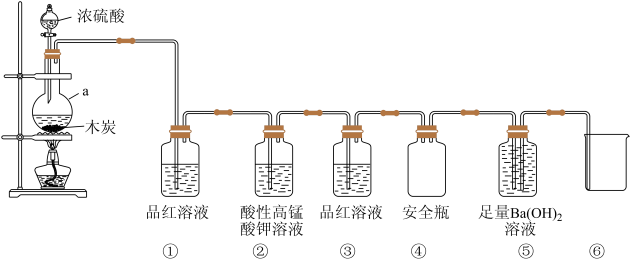
(1)仪器a的名称为_______ 。
(2)洗气瓶①②中溶液褪色,体现的二氧化硫的性质依次为_______(填序号)
(3)上述实验证明木炭与浓硫酸反应放出的气体中有少量CO的实验现象是_______ 。
 、
、 和少量CO。回答下列问题:
和少量CO。回答下列问题:
(1)仪器a的名称为
(2)洗气瓶①②中溶液褪色,体现的二氧化硫的性质依次为_______(填序号)
| A.氧化性、还原性 | B.漂白性、还原性 |
| C.漂白性、氧化性 | D.还原性、漂白性 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】已知实验室可通过反应HCOOH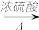 CO↑+H2O来制取一氧化碳。装置如图所示:
CO↑+H2O来制取一氧化碳。装置如图所示:
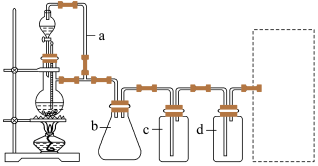
(1)用如图装置制备干燥纯净的 CO,装置中 a 和 b 的作用分别是________ ,________ ;c 和 d 中盛装的试剂分别是________ ,________ 。若用该装置制备 H2,气体发生装置中必需的玻璃仪器名称是________ ;在虚线框内画出收集干燥 H2的装置图_________ 。
(2)实验室制得的丙烯中含有 SO2、CO2及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是__ (填序号)。
①饱和 Na2SO3溶液 ②酸性 KMnO4溶液③石灰水 ④无水 CuSO4 ⑤品红溶液
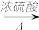 CO↑+H2O来制取一氧化碳。装置如图所示:
CO↑+H2O来制取一氧化碳。装置如图所示:
(1)用如图装置制备干燥纯净的 CO,装置中 a 和 b 的作用分别是
(2)实验室制得的丙烯中含有 SO2、CO2及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是
①饱和 Na2SO3溶液 ②酸性 KMnO4溶液③石灰水 ④无水 CuSO4 ⑤品红溶液
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】 及铵盐都是重要的化工原料,在工业生产和生活中有广泛的应用。
及铵盐都是重要的化工原料,在工业生产和生活中有广泛的应用。
(1)氨气的制备_______ 。反应的化学方程式为_______ 。
②欲收集一瓶干燥的氨气,选择图中的装置,其连接顺序为:发生装置→_______ (按气流方向,用小写字母表示)。
(2)按如图装置进行 性质实验。
性质实验。_______ ,原因是_______ 。稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是_______ 。
(3)氯的氧化物( )是大气污染物之一,工业上在一定温度和催化剂条件下
)是大气污染物之一,工业上在一定温度和催化剂条件下 将
将 转化为无污染的
转化为无污染的 ,写出其反应的化学方程式
,写出其反应的化学方程式_______ 。
 及铵盐都是重要的化工原料,在工业生产和生活中有广泛的应用。
及铵盐都是重要的化工原料,在工业生产和生活中有广泛的应用。(1)氨气的制备

②欲收集一瓶干燥的氨气,选择图中的装置,其连接顺序为:发生装置→
(2)按如图装置进行
 性质实验。
性质实验。
②再打开旋塞2,B瓶中的现象是
(3)氯的氧化物(
 )是大气污染物之一,工业上在一定温度和催化剂条件下
)是大气污染物之一,工业上在一定温度和催化剂条件下 将
将 转化为无污染的
转化为无污染的 ,写出其反应的化学方程式
,写出其反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】如图是一组探究氯气性质的装置。
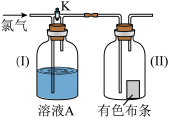
(1)现关闭活塞K,若有色布条是干燥的,溶液A为浓硫酸,则有色布条________ ;若溶液A为水,则有色布条________ ;若溶液A为饱和的NaHCO3溶液,则有色布条________ 。
(2)现打开K,溶液A为氢氧化钠溶液,通入的氯气是湿润的,布条是干燥的,则有色布条________ 。

(1)现关闭活塞K,若有色布条是干燥的,溶液A为浓硫酸,则有色布条
(2)现打开K,溶液A为氢氧化钠溶液,通入的氯气是湿润的,布条是干燥的,则有色布条
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】Ⅰ.如图是某学校实验室从化学试剂商店买回来的NaOH试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
标签上的有关数据回答下列问题:
(1)该NaOH溶液的物质的量浓度为___________ (保留两位小数);现在要配制480mL该浓度的NaOH溶液,应用托盘天平称取NaOH的质量为___________ 。
(2)配制上述溶液的过程中需要用到的主要玻璃仪器除了量筒、烧杯、玻璃棒外,还缺少的必要玻璃仪器为___________ 、___________ (填仪器名称)。
(3)若取5mL该溶液用水稀释到100mL,所得溶液 的物质的量浓度为
的物质的量浓度为___________ 。
(4)下列操作能使NaOH溶液的物质的量浓度偏高的有___________ (填字母)。
a.摇匀后发现液面低于刻度线再加水
b.NaOH溶解后未恢复至室温就注入容量瓶中
c.转移时没有洗涤烧杯、玻璃棒
d.定容时俯视刻度线
e.容量瓶未烘干
Ⅱ.某同学发现上个月做实验用的NaOH溶液忘记盖瓶塞。对于该溶液是否变质,该同学对此进行了探究。请你一起完成下列实验报告。
【提出问题1】该溶液是否变质?
【实验探究1】
(5)完成下列表格
【提出问题2】该溶液变质程度怎样?
【提出猜想】
(6)猜想一:已完全变质,该溶液中溶质只含 。
。
猜想二:部分变质,该溶液中溶质含有___________ 。
该同学探究该溶液是否完全变质,准备了两种试剂:①酚酞试液,②足量的 溶液(
溶液( 溶液为中性溶液),若加入顺序为②①,当出现
溶液为中性溶液),若加入顺序为②①,当出现___________ 现象时,说明NaOH溶液已完全变质,其中加入②时发生反应的化学方程式为___________ 。
| 氢氧化钠溶液 化学式:NaOH 相对分子质量:40 密度: 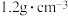 质量分数:20% |
(1)该NaOH溶液的物质的量浓度为
(2)配制上述溶液的过程中需要用到的主要玻璃仪器除了量筒、烧杯、玻璃棒外,还缺少的必要玻璃仪器为
(3)若取5mL该溶液用水稀释到100mL,所得溶液
 的物质的量浓度为
的物质的量浓度为(4)下列操作能使NaOH溶液的物质的量浓度偏高的有
a.摇匀后发现液面低于刻度线再加水
b.NaOH溶解后未恢复至室温就注入容量瓶中
c.转移时没有洗涤烧杯、玻璃棒
d.定容时俯视刻度线
e.容量瓶未烘干
Ⅱ.某同学发现上个月做实验用的NaOH溶液忘记盖瓶塞。对于该溶液是否变质,该同学对此进行了探究。请你一起完成下列实验报告。
【提出问题1】该溶液是否变质?
【实验探究1】
(5)完成下列表格
| 实验步骤 | 实验现象 | 解释与结论 |
| 取少量该溶液于试管中,滴加足量稀盐酸 | 有 | 说明该溶液已变质。变质的原因是 |
【提出问题2】该溶液变质程度怎样?
【提出猜想】
(6)猜想一:已完全变质,该溶液中溶质只含
 。
。猜想二:部分变质,该溶液中溶质含有
该同学探究该溶液是否完全变质,准备了两种试剂:①酚酞试液,②足量的
 溶液(
溶液( 溶液为中性溶液),若加入顺序为②①,当出现
溶液为中性溶液),若加入顺序为②①,当出现
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】工业上常利用含硫废水生产 ,实验室可用如图所示装置(略去部分夹持仪器)模拟生产过程。
,实验室可用如图所示装置(略去部分夹持仪器)模拟生产过程。
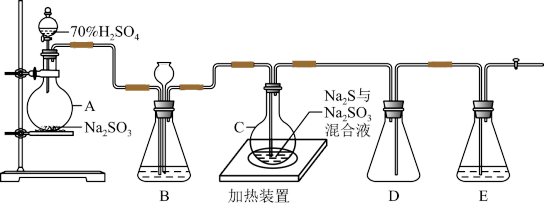
烧瓶C中发生反应如下:
 (Ⅰ)
(Ⅰ)
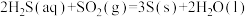 (Ⅱ)
(Ⅱ)
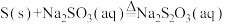 (Ⅲ)
(Ⅲ)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若____________ ,则整个装置气密性良好。装置D的作用是____________ 。装置E中为____________ 溶液。
(2)装置B的作用之一是观察 的生成速率,其中的液体最好选择
的生成速率,其中的液体最好选择____________ 。
a 蒸馏水 b 饱和 溶液
溶液
c 饱和 溶液 d 饱和
溶液 d 饱和 溶液
溶液
实验中,为使 缓慢进入烧瓶C,采用的操作是
缓慢进入烧瓶C,采用的操作是____________ 。
(3)反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出 ,其中可能含有
,其中可能含有 、
、 等杂质。利用所给试剂设计实验,检测产品中是否存在
等杂质。利用所给试剂设计实验,检测产品中是否存在 ,简要说明实验操作、现象和结论:
,简要说明实验操作、现象和结论:__________________ 。
已知 遇酸易分解:
遇酸易分解: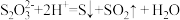 供选择的试剂:稀盐酸、稀硫酸、稀硝酸、
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、 溶液、
溶液、 溶液
溶液
 ,实验室可用如图所示装置(略去部分夹持仪器)模拟生产过程。
,实验室可用如图所示装置(略去部分夹持仪器)模拟生产过程。
烧瓶C中发生反应如下:
 (Ⅰ)
(Ⅰ)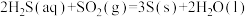 (Ⅱ)
(Ⅱ)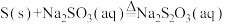 (Ⅲ)
(Ⅲ)(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若
(2)装置B的作用之一是观察
 的生成速率,其中的液体最好选择
的生成速率,其中的液体最好选择a 蒸馏水 b 饱和
 溶液
溶液c 饱和
 溶液 d 饱和
溶液 d 饱和 溶液
溶液实验中,为使
 缓慢进入烧瓶C,采用的操作是
缓慢进入烧瓶C,采用的操作是(3)反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出
 ,其中可能含有
,其中可能含有 、
、 等杂质。利用所给试剂设计实验,检测产品中是否存在
等杂质。利用所给试剂设计实验,检测产品中是否存在 ,简要说明实验操作、现象和结论:
,简要说明实验操作、现象和结论:已知
 遇酸易分解:
遇酸易分解: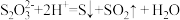 供选择的试剂:稀盐酸、稀硫酸、稀硝酸、
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、 溶液、
溶液、 溶液
溶液
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】亚硝酸钠 可用作建筑钢材的缓蚀剂;也可用作食品添加剂,抑制微生物的生长,保持肉制品的结构和营养价值,但是过量摄入会导致中毒。
可用作建筑钢材的缓蚀剂;也可用作食品添加剂,抑制微生物的生长,保持肉制品的结构和营养价值,但是过量摄入会导致中毒。
Ⅰ.某工厂以浓 、
、 、
、 溶液等为原料生产
溶液等为原料生产 ,其流程如图:
,其流程如图:

(1)在“分解塔”中,按一定比例通入 和喷入浓
和喷入浓 ,产生
,产生 和
和 。操作时将
。操作时将 从塔底通入,浓
从塔底通入,浓 从塔顶向下喷淋,这种加料操作的目的是
从塔顶向下喷淋,这种加料操作的目的是_____ 。
(2)“分解塔”中的温度不宜过高,其主要原因是_____ 。
(3)“吸收塔”中主要发生的反应为 、
、 与
与 溶液反应生成
溶液反应生成 。写出
。写出 、
、 按物质的量之比
按物质的量之比 与
与 反应生成
反应生成 的化学方程式:
的化学方程式:_____ 。
Ⅱ.某化学研究小组在实验室用稀硝酸、 、
、 为原料制备
为原料制备 ,实验装置如图(夹持装置已省略)。
,实验装置如图(夹持装置已省略)。

已知:① ,
, ;
;
②酸性条件下, 、
、 或
或 都能与
都能与 反应生成
反应生成 和
和 。
。
(4)向三颈烧瓶中加入稀 前,需要先打开止水夹
前,需要先打开止水夹 ,向装置中通入一段时间
,向装置中通入一段时间 ,目的是
,目的是_____ 。
(5)装置 中发生反应的离子方程式为
中发生反应的离子方程式为_____ 。
(6)装置 、
、 不可省去,否则会导致产品中混有
不可省去,否则会导致产品中混有_____ (填化学式)杂质。
 可用作建筑钢材的缓蚀剂;也可用作食品添加剂,抑制微生物的生长,保持肉制品的结构和营养价值,但是过量摄入会导致中毒。
可用作建筑钢材的缓蚀剂;也可用作食品添加剂,抑制微生物的生长,保持肉制品的结构和营养价值,但是过量摄入会导致中毒。Ⅰ.某工厂以浓
 、
、 、
、 溶液等为原料生产
溶液等为原料生产 ,其流程如图:
,其流程如图:
(1)在“分解塔”中,按一定比例通入
 和喷入浓
和喷入浓 ,产生
,产生 和
和 。操作时将
。操作时将 从塔底通入,浓
从塔底通入,浓 从塔顶向下喷淋,这种加料操作的目的是
从塔顶向下喷淋,这种加料操作的目的是(2)“分解塔”中的温度不宜过高,其主要原因是
(3)“吸收塔”中主要发生的反应为
 、
、 与
与 溶液反应生成
溶液反应生成 。写出
。写出 、
、 按物质的量之比
按物质的量之比 与
与 反应生成
反应生成 的化学方程式:
的化学方程式:Ⅱ.某化学研究小组在实验室用稀硝酸、
 、
、 为原料制备
为原料制备 ,实验装置如图(夹持装置已省略)。
,实验装置如图(夹持装置已省略)。
已知:①
 ,
, ;
;②酸性条件下,
 、
、 或
或 都能与
都能与 反应生成
反应生成 和
和 。
。(4)向三颈烧瓶中加入稀
 前,需要先打开止水夹
前,需要先打开止水夹 ,向装置中通入一段时间
,向装置中通入一段时间 ,目的是
,目的是(5)装置
 中发生反应的离子方程式为
中发生反应的离子方程式为(6)装置
 、
、 不可省去,否则会导致产品中混有
不可省去,否则会导致产品中混有
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】硫酸铜是一种常见的化工产品,它在纺织、印染、医药、化工、电镀以及木材和纸张的防腐等方面有极其广泛的用途。实验室制备硫酸铜的步骤如下:
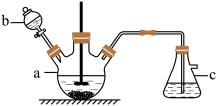
①在仪器a中先加入20g铜片、60 mL水,再缓缓加入17 mL浓硫酸:在仪器b中加入39 mL浓硝酸;在仪器c中加入20%的石灰乳150 mL。
②从仪器b中放出约5mL浓硝酸,开动搅拌器然后采用滴加的方式逐渐将浓硝酸加到仪器a中,搅拌器间歇开动。当最后滴浓硝酸加完以后,完全开动搅拌器,等反应基本停止下来时,开始用电炉加热直至仪器a中的红棕色气体完全消失,立即将导气管从仪器c中取出,再停止加热。
③将仪器a中的液体倒出,取出未反应完的铜片溶液冷却至室温.析出蓝色晶体.回答下列问题:
(1)将仪器b中液体滴入仪器a中的具体操作是__________ 。
(2)写出装置a中生成CuSO4的化学方程式:_______ 。
(3)步骤②电炉加热直至仪器a中的红棕色气体完全消失,此时会产生的气体是______ ,该气体无法直接被石灰乳吸收,为防止空气污染,请画出该气体的吸收装置(标明所用试剂及气流方向)______ 。
(4)通过本实验制取的硫酸铜晶体中常含有少量Cu(NO3)2,可来用重结晶法进行提纯,检验Cu(NO3)2是否被除净的方法是_______ 。
(5)工业上也常采用将铜在450 °C左右焙烧,再与一定浓度的硫酸反应制取硫酸铜的方法,对比分析本实验采用的硝酸氧化法制取CuSO4的优点是_______ 。
(6)用滴定法测定蓝色晶体中Cu2+的含量。取a g试样配成100 mL溶液,每次取20.00 mL用c mol·L-1EDTA(H2Y )标准溶液滴定至终点,平行滴定3次,平均消耗EDTA溶液b mL,滴定反应为Cu2++H2Y =CuY +2H+,蓝色晶体中Cu2+质量分数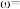
_____ %.

①在仪器a中先加入20g铜片、60 mL水,再缓缓加入17 mL浓硫酸:在仪器b中加入39 mL浓硝酸;在仪器c中加入20%的石灰乳150 mL。
②从仪器b中放出约5mL浓硝酸,开动搅拌器然后采用滴加的方式逐渐将浓硝酸加到仪器a中,搅拌器间歇开动。当最后滴浓硝酸加完以后,完全开动搅拌器,等反应基本停止下来时,开始用电炉加热直至仪器a中的红棕色气体完全消失,立即将导气管从仪器c中取出,再停止加热。
③将仪器a中的液体倒出,取出未反应完的铜片溶液冷却至室温.析出蓝色晶体.回答下列问题:
(1)将仪器b中液体滴入仪器a中的具体操作是
(2)写出装置a中生成CuSO4的化学方程式:
(3)步骤②电炉加热直至仪器a中的红棕色气体完全消失,此时会产生的气体是
(4)通过本实验制取的硫酸铜晶体中常含有少量Cu(NO3)2,可来用重结晶法进行提纯,检验Cu(NO3)2是否被除净的方法是
(5)工业上也常采用将铜在450 °C左右焙烧,再与一定浓度的硫酸反应制取硫酸铜的方法,对比分析本实验采用的硝酸氧化法制取CuSO4的优点是
(6)用滴定法测定蓝色晶体中Cu2+的含量。取a g试样配成100 mL溶液,每次取20.00 mL用c mol·L-1EDTA(H2Y )标准溶液滴定至终点,平行滴定3次,平均消耗EDTA溶液b mL,滴定反应为Cu2++H2Y =CuY +2H+,蓝色晶体中Cu2+质量分数
您最近一年使用:0次




