一定温度下,向容积为2L的恒容密闭容器中加入等物质的量的H2和I2,发生反应H2(g)+I2(g)⇌2HI(g)ΔH<0。测得不同反应时间容器内H2的物质的量如表;
回答下列问题:
(1)0~20min内HI的平均反应速率为____ 。
(2)反应达到化学平衡状态时,I2的转化率为____ ,容器内HI的体积分数为____ 。
(3)该条件下,能说明上述反应达到化学平衡状态的是____ 。(填标号)
A.混合气体颜色不再改变
B.容器内压强不再改变
C.H2、I2、HI三种气体体积分数不再改变
D.混合气体密度不再改变
(4)该反应在三种不同情况下的化学反应速率分别为:①v(H2)=0.02mol·L-1·s-1,②v(I2)=0.32mol·L-1·min-1,③v(HI)=0.84mol·L-1·min-1。则反应进行的速率由快到慢的顺序为____ 。
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(H2)/mol | 1 | 0.75 | 0.65 | 0.6 | 0.6 |
回答下列问题:
(1)0~20min内HI的平均反应速率为
(2)反应达到化学平衡状态时,I2的转化率为
(3)该条件下,能说明上述反应达到化学平衡状态的是
A.混合气体颜色不再改变
B.容器内压强不再改变
C.H2、I2、HI三种气体体积分数不再改变
D.混合气体密度不再改变
(4)该反应在三种不同情况下的化学反应速率分别为:①v(H2)=0.02mol·L-1·s-1,②v(I2)=0.32mol·L-1·min-1,③v(HI)=0.84mol·L-1·min-1。则反应进行的速率由快到慢的顺序为
19-20高一下·云南昆明·期末 查看更多[4]
(已下线)第2章基础巩固测评卷-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)浙江省宁波市北仑中学2020-2021学年高一下学期期中考试化学试题(已下线)第02章 化学反应的方向、限度与速率(B卷能力提升卷)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)云南省昆明市2019-2020学年高一下学期期末质量检测化学试题
更新时间:2020-09-27 11:17:26
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】在一定条件下N2 + 3H2⇌ 2NH3 的反应中,起始N2浓度为2mol/L,H2浓度为5mol/L, 反应到2分钟时,测得 NH3 的反应速率为v(NH3 )=0.4mol/(L·min),填空:
(1) NH3 的转化浓度为c(NH3 )=___________ mol/(L·min)
(2)三段式填空:
(mol/L) N2 + 3H2 ⇌ 2NH3
起始浓度 2 5 0
转化浓度_ _ _
2min后浓度_ _ _
(3)用v(N2)表示的反应速率为:v(N2)=__________ mol/(L·min)
(4)用v(H2)表示的反应速率为:v(H2)=__________ mol/(L·min)
(1) NH3 的转化浓度为c(NH3 )=
(2)三段式填空:
(mol/L) N2 + 3H2 ⇌ 2NH3
起始浓度 2 5 0
转化浓度
2min后浓度
(3)用v(N2)表示的反应速率为:v(N2)=
(4)用v(H2)表示的反应速率为:v(H2)=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】化学在生产生活中无处不在。
I.某汽车安全气囊的气体发生剂主要含有叠氮化钠(NaN3)、三氧化二铁(Fe2O3)、硝酸铵等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)NaN3是气体发生剂,是___________ (填“离子”或“共价”)化合物。
(2)汽车受到猛烈碰撞时,点火器点火引发NaN3迅速分解,生成氮气和金属钠,同时释放大量的热。下列关于该反应过程中的能量变化示意图正确的是___________ (填字母)。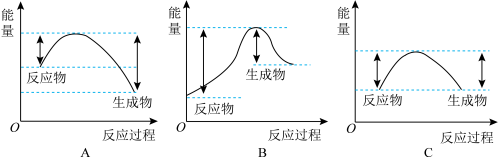
Ⅱ.CH4、CH3OH既是重要的化工原料,又是重要的能源物质。
(3)将2.0 mol CH4和4.0 mol H2O(g)通入容积为4 L的反应器,保持容器容积不变,在一定温度下发生反应CH4(g)+H2O(g) CO(g)+3H2(g),测得在5 min时,CO的物质的量为0.8 mol,则0~5 min内,用H2表示该反应的平均反应速率为
CO(g)+3H2(g),测得在5 min时,CO的物质的量为0.8 mol,则0~5 min内,用H2表示该反应的平均反应速率为___________ 。
(4)一定条件下,将1.0 mol CH4与2.0 mol H2O(g)充入密闭容器中发生反应CH4(g)+H2O(g) CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是
CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是___________ (填字母)。
a.恒容条件下充入He b.增大体积 c.升高温度 d.保持恒容投入更多的H2O(g) e.加入合适的催化剂
(5)用CH4设计燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒),电池总反应为CH4+2O2+2KOH=K2CO3+3H2O。___________ (填“A”或“B”)电极入口通甲烷。
②当消耗甲烷的体积为33.6 L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为___________ 。
I.某汽车安全气囊的气体发生剂主要含有叠氮化钠(NaN3)、三氧化二铁(Fe2O3)、硝酸铵等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)NaN3是气体发生剂,是
(2)汽车受到猛烈碰撞时,点火器点火引发NaN3迅速分解,生成氮气和金属钠,同时释放大量的热。下列关于该反应过程中的能量变化示意图正确的是

Ⅱ.CH4、CH3OH既是重要的化工原料,又是重要的能源物质。
(3)将2.0 mol CH4和4.0 mol H2O(g)通入容积为4 L的反应器,保持容器容积不变,在一定温度下发生反应CH4(g)+H2O(g)
 CO(g)+3H2(g),测得在5 min时,CO的物质的量为0.8 mol,则0~5 min内,用H2表示该反应的平均反应速率为
CO(g)+3H2(g),测得在5 min时,CO的物质的量为0.8 mol,则0~5 min内,用H2表示该反应的平均反应速率为(4)一定条件下,将1.0 mol CH4与2.0 mol H2O(g)充入密闭容器中发生反应CH4(g)+H2O(g)
 CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是
CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是a.恒容条件下充入He b.增大体积 c.升高温度 d.保持恒容投入更多的H2O(g) e.加入合适的催化剂
(5)用CH4设计燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒),电池总反应为CH4+2O2+2KOH=K2CO3+3H2O。
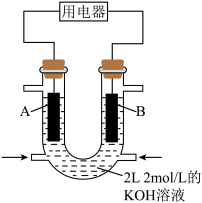
②当消耗甲烷的体积为33.6 L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】由 羟基丁酸(
羟基丁酸(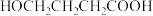 )生成
)生成 丁内酯(
丁内酯( )的反应如下:
)的反应如下:

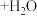
在25℃时,溶液中 羟基丁酸的初始浓度为0.180mol/L,随着反应的进行,测得
羟基丁酸的初始浓度为0.180mol/L,随着反应的进行,测得 丁内酯浓度随时间的变化如下表所示。
丁内酯浓度随时间的变化如下表所示。
请填写下列空白:
(1)在50~80min内,以 丁内酯的浓度变化表示的反应速率为
丁内酯的浓度变化表示的反应速率为___________ 。
(2)在100min时, 羟基丁酸的转化率为
羟基丁酸的转化率为___________ 。
(3)在25℃时,当生成 丁内酯与生成H2O的物质的量之比保持不变时,反应
丁内酯与生成H2O的物质的量之比保持不变时,反应___________ 达到平衡(填“一定”或“不一定”)
(4)在25℃时,该反应的平衡常数为K=___________ 。
(5)为提高平衡时 羟基丁酸的转化率,除适当控制反应温度外,还可采取的措施是
羟基丁酸的转化率,除适当控制反应温度外,还可采取的措施是___________ 。
(6)该反应达到平衡后,增大压强,平衡___________ 移动(填“正向”“不”或“逆向”)
 羟基丁酸(
羟基丁酸(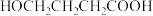 )生成
)生成 丁内酯(
丁内酯( )的反应如下:
)的反应如下:

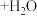
在25℃时,溶液中
 羟基丁酸的初始浓度为0.180mol/L,随着反应的进行,测得
羟基丁酸的初始浓度为0.180mol/L,随着反应的进行,测得 丁内酯浓度随时间的变化如下表所示。
丁内酯浓度随时间的变化如下表所示。| t/min | 21 | 50 | 80 | 100 | 120 | 160 | 220 |  |
| c(mol/L) | 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
(1)在50~80min内,以
 丁内酯的浓度变化表示的反应速率为
丁内酯的浓度变化表示的反应速率为(2)在100min时,
 羟基丁酸的转化率为
羟基丁酸的转化率为(3)在25℃时,当生成
 丁内酯与生成H2O的物质的量之比保持不变时,反应
丁内酯与生成H2O的物质的量之比保持不变时,反应(4)在25℃时,该反应的平衡常数为K=
(5)为提高平衡时
 羟基丁酸的转化率,除适当控制反应温度外,还可采取的措施是
羟基丁酸的转化率,除适当控制反应温度外,还可采取的措施是(6)该反应达到平衡后,增大压强,平衡
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】某工厂实验室用CO和H2制备CH3OH,其原理为:CO(g)+2H2(g)⇌CH3OH(g) ∆H<0
试回答下列问题:
(1)若该反应在298K、398K时,化学平衡常数分别为K1、K2,则K1____ K2(填“>”、“<”、“=”)
(2)在恒温恒容条件下,判断该反应达到化学平衡状态的是___
A.v正(H2)=2v正(CH3OH) B.v正(H2)=v正(CO)
C.容器内压强保持不变 D.混合气体的密度不变
(3)某温度下,向一定容积的密闭容器中充入CO和H2,浓度分别为1mol/L和2mol/L,达到平衡时CO的浓度为0.6mol/L,试求该温度下的化学平衡常数____ 。
试回答下列问题:
(1)若该反应在298K、398K时,化学平衡常数分别为K1、K2,则K1
(2)在恒温恒容条件下,判断该反应达到化学平衡状态的是
A.v正(H2)=2v正(CH3OH) B.v正(H2)=v正(CO)
C.容器内压强保持不变 D.混合气体的密度不变
(3)某温度下,向一定容积的密闭容器中充入CO和H2,浓度分别为1mol/L和2mol/L,达到平衡时CO的浓度为0.6mol/L,试求该温度下的化学平衡常数
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】利用催化技术可将汽车尾气中的CO和NO转化为 和
和 ,化学方程式:
,化学方程式: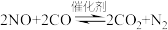
(1)某温度下,在容积不变的密闭容器中通入CO和NO,测得不同时间CO的浓度如下表:
用CO的浓度变化表示0~2s的平均反应速率为_______  。
。
(2)下列可以说明反应达到平衡状态的是_______ 。
a.CO的浓度不再改变
b.容器中的气体质量保持不变
c.NO、CO、CO2、N2的浓度之比为2︰2︰2︰1
d.相同时间内,反应消耗2molNO同时消耗1molN2
(3)在密闭容器里发生上述反应,当改变下列条件时,反应速率会减小的是_______ (填序号)。
①降低温度 ②容器体积不变,充入惰性气体Ar
③容器压强不变,充入惰性气体Ar ④再通入a mol NO(g)
(4)反应物初始浓度相同时,实验温度为280℃和360℃,进行以下实验:
【实验分析与结论】
①补全表格a._______ ,b._______ ,c._______ 。
②测得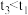 ,对比实验I、III,可得结论:催化剂的比表面积相同时,
,对比实验I、III,可得结论:催化剂的比表面积相同时,_______ 。
③通过实验可得到“温度相同时,增大催化剂的比表面积,可增大尾气的转化速率”的结论,证据是对比实验I、II,
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
 和
和 ,化学方程式:
,化学方程式: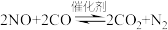
(1)某温度下,在容积不变的密闭容器中通入CO和NO,测得不同时间CO的浓度如下表:
| 时间/s | 0 | 1 | 2 | 3 | …… |
 | 3.60 | 3.05 | 2.85 | 2.75 | …… |
 。
。(2)下列可以说明反应达到平衡状态的是
a.CO的浓度不再改变
b.容器中的气体质量保持不变
c.NO、CO、CO2、N2的浓度之比为2︰2︰2︰1
d.相同时间内,反应消耗2molNO同时消耗1molN2
(3)在密闭容器里发生上述反应,当改变下列条件时,反应速率会减小的是
①降低温度 ②容器体积不变,充入惰性气体Ar
③容器压强不变,充入惰性气体Ar ④再通入a mol NO(g)
(4)反应物初始浓度相同时,实验温度为280℃和360℃,进行以下实验:
| 实验编号 | 实验目的 | T/℃ | 同种催化剂的比表面积 /g /g | 达平衡时所用的时间/s |
| I | 对照实验 | 280 | 80 |  |
| II | a | 280 | 120 |  |
| III | 研究温度对尾气转化速率的影响 | b | c |  |
①补全表格a.
②测得
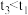 ,对比实验I、III,可得结论:催化剂的比表面积相同时,
,对比实验I、III,可得结论:催化剂的比表面积相同时,③通过实验可得到“温度相同时,增大催化剂的比表面积,可增大尾气的转化速率”的结论,证据是对比实验I、II,

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次




