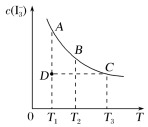
某温度时,在2L恒容密闭容器中X、Y、Z三种气体物质的量(n)随时间(t)变化的曲线如图所示。下列说法正确的是
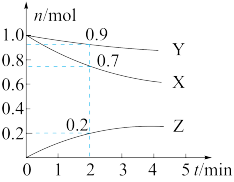

A.该反应的化学方程式为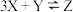 |
B.反应开始至2min时,用Z表示的平均反应速率为 |
| C.混合气体的密度不随时间的变化而变化时可以判断该反应达到平衡状态 |
| D.反应进行到2min时,X、Y、Z的化学反应速率相等 |
19-20高一下·湖北省直辖县级单位·期末 查看更多[3]
福建省南平市高级中学2020-2021学年高一下学期期中考试化学试题(已下线)练习4 化学平衡-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)湖北省仙桃、天门、潜江2019-2020学年高一下学期期末考试化学试题
更新时间:2020-08-25 18:41:55
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】在密闭容器中,A与B反应生成C(A、B、C均为气体),其反应速率分别用 表示,已知
表示,已知 ,则此反应可表示为
,则此反应可表示为
 表示,已知
表示,已知 ,则此反应可表示为
,则此反应可表示为A. | B. |
C. | D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】在 的反应中,经过一段时间后,NH3的浓度增加了0.8 mol/L,在此段时间内用H2表示的平均反应速率为0.25mol/(L·s),则此段时间是( )
的反应中,经过一段时间后,NH3的浓度增加了0.8 mol/L,在此段时间内用H2表示的平均反应速率为0.25mol/(L·s),则此段时间是( )
 的反应中,经过一段时间后,NH3的浓度增加了0.8 mol/L,在此段时间内用H2表示的平均反应速率为0.25mol/(L·s),则此段时间是( )
的反应中,经过一段时间后,NH3的浓度增加了0.8 mol/L,在此段时间内用H2表示的平均反应速率为0.25mol/(L·s),则此段时间是( )| A.2 s | B.3.2 s | C.4.8 s | D.5.6 s |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】T℃时,H2还原NO以消除氮氧化物污染的反应2NO(g)+2H2(g) N2(g)+2H2O(g)能自发进行,其正反应速率方程为
N2(g)+2H2O(g)能自发进行,其正反应速率方程为 =kca(NO)cb(H2),实验得到如下数据:
=kca(NO)cb(H2),实验得到如下数据:
下列说法正确的是
 N2(g)+2H2O(g)能自发进行,其正反应速率方程为
N2(g)+2H2O(g)能自发进行,其正反应速率方程为 =kca(NO)cb(H2),实验得到如下数据:
=kca(NO)cb(H2),实验得到如下数据:| 组别 | c(NO)起始/mol·L-1 | c(H2)起始/mol·L-1 |  (正反应)起始/mol·L-1·s-1 (正反应)起始/mol·L-1·s-1 |
| I | 6.00×10-3 | 2.00×10-3 | 2.16×10-3 |
| II | 1.20×10-2 | 2.00×10-3 | 8.64×10-3 |
| III | 6.00×10-3 | 4.00×10-3 | 4.32×10-3 |
| A.H2还原NO是熵增的反应 | B.正反应一定为吸热反应 |
| C.a=2,b=2 | D.T℃时,k的数值为3×104 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】对反应A(s)+3B(g) 2C(g)+D(g)来说,下列反应速率最快的是
2C(g)+D(g)来说,下列反应速率最快的是
 2C(g)+D(g)来说,下列反应速率最快的是
2C(g)+D(g)来说,下列反应速率最快的是| A.v(A)=0.02mol/(L•s) | B.v(B)=0.6mol/(L•min) |
| C.v(C)=1.0mol/(L•min) | D.v(D)=0.01mol/(L•s) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】对于反应 ,下列各数据表示不同条件下的反应速率,其中反应进行得最慢的是
,下列各数据表示不同条件下的反应速率,其中反应进行得最慢的是
 ,下列各数据表示不同条件下的反应速率,其中反应进行得最慢的是
,下列各数据表示不同条件下的反应速率,其中反应进行得最慢的是A. | B. |
C. | D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】以Cl2、SO2和PCl3为原料,制备POCl3和氯化亚砜(SOCl2)的原理为PCl3(g)+Cl2(g)+SO2(g) POCl3(s)+SOCl2(g);ΔH<0,下列说法正确的是
POCl3(s)+SOCl2(g);ΔH<0,下列说法正确的是
 POCl3(s)+SOCl2(g);ΔH<0,下列说法正确的是
POCl3(s)+SOCl2(g);ΔH<0,下列说法正确的是| A.使用催化剂可以同时降低正反应和逆反应的活化能 |
| B.1molCl-Cl键断裂的同时有2molS-Cl键形成,说明反应到达该条件下的平衡状态 |
C.反应平衡常数K= |
| D.上述反应中消耗3.36LCl2,转移电子数为0.3×6.02×1023 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】在一定温度下,某体积不变的密闭容器中发生如下可逆反应:A2(g)+B2(g) 2AB(g)。该反应达到平衡状态的标志是
2AB(g)。该反应达到平衡状态的标志是
 2AB(g)。该反应达到平衡状态的标志是
2AB(g)。该反应达到平衡状态的标志是| A.A2、B2、AB的反应速率的比值为1:1:2 |
| B.容器内的总压强不随时间变化而变化 |
| C.单位时间内生成2nmolAB的同时生成nmolB2 |
| D.容器内混合气体的平均相对分子质量保持不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】COCl2的分解反应为: COCl2(g)=Cl2(g)+CO(g) △H=+108 kJ•mol-1。某科研小组研究反应体系达到平衡后改变外界条件,各物质的浓度在不同条件下的变化状况,结果如图所示。下列有关判断不正确的是
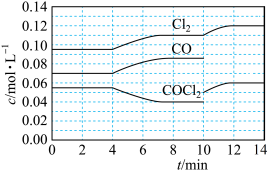

| A.第 4min 时,改变的反应条件是升高温度 |
| B.第 6min 时,V 正(COCl2)>V 逆(COCl2) |
| C.第 8min 时的平衡常数 K=2.34 |
| D.第 10min 到 14min 未标出 COCl2的浓度变化曲线 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】符合如图的反应是( )


A.X(g)+3Y(g) 2Z(g) ΔH>0 2Z(g) ΔH>0 |
B.X(g)+3Y(g) 2Z(g) ΔH<0 2Z(g) ΔH<0 |
C.X(g)+2Y(g) 3Z(g) ΔH<0 3Z(g) ΔH<0 |
D.X(g)+2Y(g) 3Z(g) ΔH>0 3Z(g) ΔH>0 |
您最近一年使用:0次

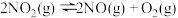 在容积固定的密闭容器中达到平衡状态的标志是
在容积固定的密闭容器中达到平衡状态的标志是 的同时生成
的同时生成
 浓度之比为2∶2∶1
浓度之比为2∶2∶1 I
I (aq),某I2、KI混合溶液中,I
(aq),某I2、KI混合溶液中,I