1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系,下图是元素周期表的一部分, 回答下列问题:
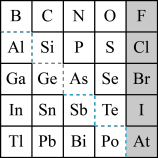
(1)元素Ga在元素周期表中的位置为:________ ;
(2)Sn的最高正价为_______ ,Cl的最高价氧化物对应水化物的化学式为______ ;
(3)根据元素周期律,推断:
①阴影部分元素形成的氢化物中热稳定性最高的是_____ ;(写化学式)
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4_______ H2SeO4 (填“>”、“<”、“=”或“无法比较”);
③氢化物的还原性:H2O_______ H2S (填“>”、“<”、“=”或“无法比较”);
④原子半径比较: N______ Si (填“>”、“<”、“=”或“无法比较”);
(4)可在图中分界线(虚线部分)附近寻找_______ (填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料 D.农药

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素形成的氢化物中热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4
③氢化物的还原性:H2O
④原子半径比较: N
(4)可在图中分界线(虚线部分)附近寻找
A.优良的催化剂 B.半导体材料 C.合金材料 D.农药
更新时间:2020-08-30 17:22:58
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】指导新元素的发现及预测它们的原子结构和性质
| “位”、“构”、“性”的关系 | 对关系图的理解 |
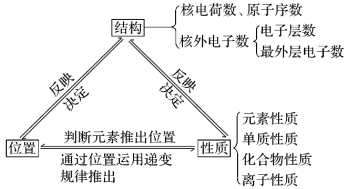 | ①结构与位置的关系:最外层电子数= ②结构与性质的关系:最外层电子数越少,电子层数越多→越易 ③元素的一些主要性质又能反映元素的原子结构和元素在周期表中的位置 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】元素周期表在指导科学研究和生产实践方面具有十分重要的意义,请将下表中A、B两栏描述的内容对应起来。_________________
A | B | A | B |
| ①制半导体的元素 | (a)IVB到VIB的过渡元素 | ① | |
| ②制催化剂的元素 | (b)F、Cl、Br、N、S三角地带 | ② | |
| ③制耐高温材料的元素 | (c)金属与非金属元素分界线附近 | ③ | |
| ④制制冷剂的元素 | (d)相对原子质量较小的元素 | ④ | |
| ⑤地壳中含量较多的元素 | (e)过渡元素 | ⑤ |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】我国科研团队成功研发“硅—石墨烯—锗晶体管”,代表着我国在这一尖端科技领域走在了世界的前列。
(1)碳元素在元素周期表中的位置是第___ 周期、第IVA族。
(2)硅元素最高价氧化物的化学式为___ 。
(3)Si的非金属性弱于S的,用原子结构解释原因:Si和S在同一周期,原子核外电子层数相同,___ ,原子半径Si大于S,得电子能力Si弱于S。
(4)在元素周期表中,锗(Ge)位于第4周期,与Si同主族。Ge—Si与Ge—Te作温差发电,可用于宇航、卫星与空间站的启动电源。下列关于Ge的推断中,正确的是__ (填字母)。
a.原子的最外层电子数为4
b.原子半径:Ge>Si
c.最高价氧化物对应的水化物酸性强于H2SiO3
(1)碳元素在元素周期表中的位置是第
(2)硅元素最高价氧化物的化学式为
(3)Si的非金属性弱于S的,用原子结构解释原因:Si和S在同一周期,原子核外电子层数相同,
(4)在元素周期表中,锗(Ge)位于第4周期,与Si同主族。Ge—Si与Ge—Te作温差发电,可用于宇航、卫星与空间站的启动电源。下列关于Ge的推断中,正确的是
a.原子的最外层电子数为4
b.原子半径:Ge>Si
c.最高价氧化物对应的水化物酸性强于H2SiO3
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下表列出了 A〜R 9种元系在周期表中的位置
(1) 这9中元素中金属性最强的是_________________ ;(填元素符号)
(2) 化学性质最不活泼的元素是_________________ ;(填元素符号)
(3) G的最高价含氧酸的化学式是_________________ ;
(4) 写出一个化学方程式证明G和H的非金属性强弱____________________ 。
族 周期 | IA | IIA | ⅢA | IVA | VA | VIA | ⅦA | 0 |
2 | E | F | ||||||
3 | A | C | D | G | R | |||
4 | B | H |
(1) 这9中元素中金属性最强的是
(2) 化学性质最不活泼的元素是
(3) G的最高价含氧酸的化学式是
(4) 写出一个化学方程式证明G和H的非金属性强弱
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】元素在周期表中的位置反映了元素的原子结构和元素的性质,下图是元素周期表的一部分:
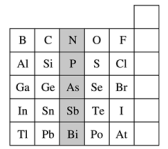
(1)根据元素周期律,请你预测,H3AsO4、H3PO4的酸性强弱:H3AsO4___________ (填“>”“<”或“=”)H3PO4。
(2)根据NaH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第___________ 族。
(3)周期表中有10多种人体所需的微量元素,其中有一种被誉为“生命元素”的主族元素R,对延长人类寿命起着重要作用。已知R元素的原子有4个电子层,其最高价氧化物的分子式为RO3,则R元素的名称为___________ 。

(1)根据元素周期律,请你预测,H3AsO4、H3PO4的酸性强弱:H3AsO4
(2)根据NaH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第
(3)周期表中有10多种人体所需的微量元素,其中有一种被誉为“生命元素”的主族元素R,对延长人类寿命起着重要作用。已知R元素的原子有4个电子层,其最高价氧化物的分子式为RO3,则R元素的名称为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】用“>”或“<”回答下列问题:
(1)酸性:H2CO3___ H2SiO3,H2SiO3___ H3PO4。
(2)碱性:Ca(OH)2___ Mg(OH)2,Mg(OH)2___ Al(OH)3。
(3)气态氢化物的稳定性:H2O___ H2S,H2S___ HCl。
(4)还原性:H2O__ H2S,H2S___ HCl。
从以上答案中可以归纳出:
①元素的非金属性越强,其最高价氧化物对应水化物的酸性越___ 。
②元素的金属性越强,其最高价氧化物对应水化物的碱性越___ 。
③元素___ 性越强,其对应气态氢化物的稳定性越强。
④元素非金属性越强,其对应气态氢化物的还原性越__ 。
(1)酸性:H2CO3
(2)碱性:Ca(OH)2
(3)气态氢化物的稳定性:H2O
(4)还原性:H2O
从以上答案中可以归纳出:
①元素的非金属性越强,其最高价氧化物对应水化物的酸性越
②元素的金属性越强,其最高价氧化物对应水化物的碱性越
③元素
④元素非金属性越强,其对应气态氢化物的还原性越
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】如表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题。
(1)地壳中含量最多的元素是____ 。
(2)氯元素位于元素周期表第____ 周期VIIA族。
(3)单质的化学性质最不活泼的是____ 。
(4)HF和HCl中,热稳定性较强的是____ 。
(5)元素最高价氧化物对应的水化物中,碱性最强的是____ (填化学式)。
(6)碳元素的最高价氧化物中碳元素与氧元素的质量比m(C):m(O)=____ 。
| 周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Al | Si | S | Cl | Ar |
(2)氯元素位于元素周期表第
(3)单质的化学性质最不活泼的是
(4)HF和HCl中,热稳定性较强的是
(5)元素最高价氧化物对应的水化物中,碱性最强的是
(6)碳元素的最高价氧化物中碳元素与氧元素的质量比m(C):m(O)=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】根据所学知识,回答下列问题:
(1)元素周期表1~20号元素中,金属性最强的元素是__________ (填元素符号,下同);属于稀有气体的是________________ ;非金属性最强的元素在周期表中的位置是_______________________ 。
(2)已知NO2和N2O4之间发生可逆反应:2NO2 (g) (红棕色) N2O4(g) (无色)。将装有NO2 和N2O4混合气体的烧瓶浸入热水中,观察到的现象是
N2O4(g) (无色)。将装有NO2 和N2O4混合气体的烧瓶浸入热水中,观察到的现象是____________________ ,产生该现象的原因是____________________________________ 。
(3)一定条件下,向2L恒容密闭容器中按体积比1:3充入4.48L(标准状况)N2和H2的混合气体,发生反应N2(g)+3H2(g) 2NH3(g),3min时反应达到平衡状态,测得c(N2)=0.02mol·L-1。
2NH3(g),3min时反应达到平衡状态,测得c(N2)=0.02mol·L-1。
① 0~3min内,v (NH3)=___________________ 。
②下列叙述可证明上述反应达到平衡状态的是_________ (填序号)。
a. v(H2)= 3 v(N2) b.容器内压强保持不变
c.每消耗1mol N2,同时生成2mol NH3
d. N2、H2和NH3的物质的量浓度不再变化
(1)元素周期表1~20号元素中,金属性最强的元素是
(2)已知NO2和N2O4之间发生可逆反应:2NO2 (g) (红棕色)
 N2O4(g) (无色)。将装有NO2 和N2O4混合气体的烧瓶浸入热水中,观察到的现象是
N2O4(g) (无色)。将装有NO2 和N2O4混合气体的烧瓶浸入热水中,观察到的现象是(3)一定条件下,向2L恒容密闭容器中按体积比1:3充入4.48L(标准状况)N2和H2的混合气体,发生反应N2(g)+3H2(g)
 2NH3(g),3min时反应达到平衡状态,测得c(N2)=0.02mol·L-1。
2NH3(g),3min时反应达到平衡状态,测得c(N2)=0.02mol·L-1。① 0~3min内,v (NH3)=
②下列叙述可证明上述反应达到平衡状态的是
a. v(H2)= 3 v(N2) b.容器内压强保持不变
c.每消耗1mol N2,同时生成2mol NH3
d. N2、H2和NH3的物质的量浓度不再变化
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】已知铷(Rb)是37号元素,其相对原子质量是85,回答下列问题:
(1)铷位于元素周期表中___________________________ (填位置)。
(2)铷单质性质活泼,写出它与氯气反应的化学方程式:________________________ ,铷单质易与水反应,反应的化学方程式为_____________________ 。实验表明,铷与水反应比钠与水反应________ (填“剧烈”或“缓慢”);反应过程中铷在水______ (填“面”或“底”)与水反应。
(3)同主族元素的同类化合物的化学性质相似,分别写出
①过氧化铷与CO2反应的化学方程式:________________________________ ;
②过量的RbOH与AlCl3反应的离子方程式:____________________ 。
(1)铷位于元素周期表中
(2)铷单质性质活泼,写出它与氯气反应的化学方程式:
(3)同主族元素的同类化合物的化学性质相似,分别写出
①过氧化铷与CO2反应的化学方程式:
②过量的RbOH与AlCl3反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H2O)3(NH4)4Cl(用R代表)。回答下列问题:
元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是__ ;氮元素的E1呈现异常的原因是__ 。

元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是

您最近一年使用:0次



