如图为相关物质间的转化关系,其中甲、丙为生活中常见的金属单质,乙、丁为非金属单质且丁为气态,E为白色沉淀,D为浅绿色溶液。请回答:
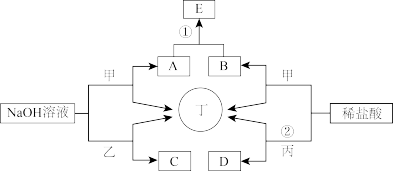
(1)组成甲的元素在元素周期表中的位置为__ ,请列举乙单质的一种用途__ ;用电子式表示丁的形成过程___ 。
(2)在C溶液中滴入2滴酚酞,再逐滴加入稀盐酸至红色消失,可得到一种胶体,该胶体的胶粒成分是__ (化学式);
(3)反应①的离子方程式为__ ;
(4)将B的稀溶液加水稀释,溶液的pH__ (填能或不能)大于7;
(5)若反应②中盐酸过量,向D溶液中滴加84消毒液,溶液的颜色发生了变化,该反应的离子方程式为__ 。

(1)组成甲的元素在元素周期表中的位置为
(2)在C溶液中滴入2滴酚酞,再逐滴加入稀盐酸至红色消失,可得到一种胶体,该胶体的胶粒成分是
(3)反应①的离子方程式为
(4)将B的稀溶液加水稀释,溶液的pH
(5)若反应②中盐酸过量,向D溶液中滴加84消毒液,溶液的颜色发生了变化,该反应的离子方程式为
更新时间:2020-08-30 20:12:26
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下图中所有物质均为中学化学常见物质,F、H是气体单质,Z是固体金属单质,Y中阳离子与阴离子个数比为2:1,化合物X、Y、A、D、E、G的焰色反应为黄色,I是白色沉淀。
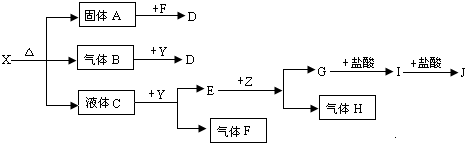
(1)写出X、E、I的化学式:X__________ 、E__________ 、I__________ ;
(2)关于Y的说法正确的是__________ ;
A.Y是氧化物 B.Y是过氧化物
C.Y是强电解质 D.Y是碱性氧化物
(3)写出E+Z的离子方程式__________ ;
(4)写出B和Y反应的化学方程式:__________ ;
(5)已知X和G的溶液反应能生成白色沉淀,试写出该反应的离子反应方程式__________ 。

(1)写出X、E、I的化学式:X
(2)关于Y的说法正确的是
A.Y是氧化物 B.Y是过氧化物
C.Y是强电解质 D.Y是碱性氧化物
(3)写出E+Z的离子方程式
(4)写出B和Y反应的化学方程式:
(5)已知X和G的溶液反应能生成白色沉淀,试写出该反应的离子反应方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下列各单质和化合物之间的转化关系如下图所示,而且各单质和化合物的组成元素的原子都不超过三个电子层。
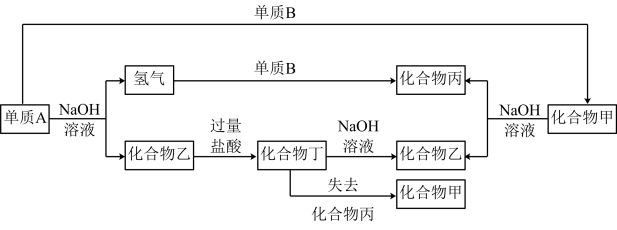
由各物质间的关系推断:
(1)单质A是___________ (写元素符号)。
(2)单质B是金属还是非金属___________ 。
(3)各化合物的化学式:甲___________ 、乙___________ 、丙___________ 、丁___________ 。

由各物质间的关系推断:
(1)单质A是
(2)单质B是金属还是非金属
(3)各化合物的化学式:甲
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D均为中学化学常见的纯净物,A是单质,B为含氧化合物。它们有如图反应关系∶
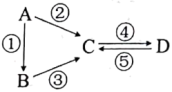
(1)若B是淡黄色固体,②③的反应物中均有同一种液态氢化物,D俗称苏打。则C的化学式为_______ 反应①的化学反应方程式为_______ A、B、C、D 均含同一种元素,检验该元素可采用_______ 法。
(2)若A是制作太阳能电池光伏材料的单质,②③的反应物中均有NaOH,D为酸。则C的水溶液俗称_______ ,反应①②③④⑤中,属于氧化还原反应的有_______ (填序号)写出C中通入过量CO2生成D的化学反应方程式_______ 。
(3)若D为两性氢氧化物。若反应②③在盐酸中完成,则C的化学式为_______ ;若反应②③在NaOH溶液中完成,则C的化学式为_______ 。反应⑤的离子方程式为_______ 。

(1)若B是淡黄色固体,②③的反应物中均有同一种液态氢化物,D俗称苏打。则C的化学式为
(2)若A是制作太阳能电池光伏材料的单质,②③的反应物中均有NaOH,D为酸。则C的水溶液俗称
(3)若D为两性氢氧化物。若反应②③在盐酸中完成,则C的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】含A元素的一种单质是一种重要的半导体材料,含 A元素的一种化合物C可用于制造高性能的现代通讯材料——光导纤维,C与烧碱反应生成含A元素的化合物D。
(1)在元素周期表中,A位于________ 族,与A同族但相对原子质量比A小的元素B的原子结构示意图为________ ,A与B在原子的电子层结构上的相同点是______________________________________ 。
(2)易与C发生化学反应的酸是________ (写名称),反应的化学方程式是__________________________ 。
(3)将C与纯碱混合高温熔融时也发生化学反应生成D,同时还生成B的最高价氧化物E;将全部的E与全部的D在足量的水中混合后,又发生化学反应生成含A的化合物F。
①写出生成D和F的化学反应方程式:______________________________________________ 。
②要将纯碱高温熔化,下列坩埚中可选用的是________ 。
A.普通玻璃坩埚 B.石英玻璃坩埚
C.氧化铝坩埚 D.铁坩埚
(4)100 g C与石灰石的混合物充分反应后,生成的气体在标准状况下的体积为11.2 L,100 g混合物中石灰石的质量分数是________ 。
(1)在元素周期表中,A位于
(2)易与C发生化学反应的酸是
(3)将C与纯碱混合高温熔融时也发生化学反应生成D,同时还生成B的最高价氧化物E;将全部的E与全部的D在足量的水中混合后,又发生化学反应生成含A的化合物F。
①写出生成D和F的化学反应方程式:
②要将纯碱高温熔化,下列坩埚中可选用的是
A.普通玻璃坩埚 B.石英玻璃坩埚
C.氧化铝坩埚 D.铁坩埚
(4)100 g C与石灰石的混合物充分反应后,生成的气体在标准状况下的体积为11.2 L,100 g混合物中石灰石的质量分数是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】单质 Z 是一种常见的半导体材料,可由 X 通过如下图所示的路线制备,其中 X 为 Z 的氧化物,Y 为氢化物,分子结构与甲烷相似,回答下列问题:
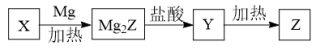
(1)能与 X 发生化学反应的酸是___________ ;在实验室中该酸保存在___________ 。
(2)由 Mg2Z 生成 Y 的化学反应方程式为___________ ,Y 分子的电子式为___________ 。
(3)晶体 Z 和 X 中熔点相对较高的是___________ (填写化学式)。

(1)能与 X 发生化学反应的酸是
(2)由 Mg2Z 生成 Y 的化学反应方程式为
(3)晶体 Z 和 X 中熔点相对较高的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
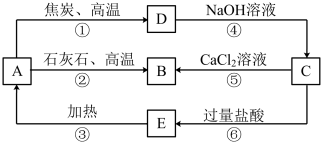
【推荐3】A、B、C、D、E五种物质中均含有同一种非金属元素,它们能发生如图所示的转化关系。若该元素用R表示,则A为R的氧化物,D为R的单质,且D与NaOH溶液反应生成C和H2。
(1)写出对应物质的化学式:A_______ ;C_______ ;E________ 。
(2)反应①的化学方程式为__________ 。
(3)反应④的离子方程式为__________ 。
(4)H2CO3的酸性强于E的酸性,请用离子方程式予以证明:________ 。
(1)写出对应物质的化学式:A
(2)反应①的化学方程式为
(3)反应④的离子方程式为
(4)H2CO3的酸性强于E的酸性,请用离子方程式予以证明:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、X均为中学常见物质,它们在一定条件下有如下转化关系(副产物已略去)。

(1)若X是氧气,则A不可能___ 。
A.C B.Si C.Na D.Mg
(2)若X是金属单质,向C的水溶液中滴入 溶液,产生了不溶于稀
溶液,产生了不溶于稀 的白色沉淀,则B的化学式为
的白色沉淀,则B的化学式为____ ;C溶液在贮存时应加入少量X,理由是(用离子方程式表示)___ 。检验B溶液中阳离子的常见试剂是____ 。
(3)若X是氢氧化钠溶液,A、B、C均为含铝元素的化合物,则反应②的离子方程式为____ 。
(4)若X为盐酸,A、B、C均不含铝元素,且反应②有无色无味气体生成,则反应①的离子方程式为___ 。

(1)若X是氧气,则A不可能
A.C B.Si C.Na D.Mg
(2)若X是金属单质,向C的水溶液中滴入
 溶液,产生了不溶于稀
溶液,产生了不溶于稀 的白色沉淀,则B的化学式为
的白色沉淀,则B的化学式为(3)若X是氢氧化钠溶液,A、B、C均为含铝元素的化合物,则反应②的离子方程式为
(4)若X为盐酸,A、B、C均不含铝元素,且反应②有无色无味气体生成,则反应①的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】据下列信息完成所需回答的问题:

其中氧化物A是白色固体;氧化物B是黑色固体;单质D为有毒的黄绿色气体,单质C不溶于冷的浓硝酸。
(1)D是_______ ;G是_______ (填化学式)
(2)写出下列反应的离子方程式:M+NaOH溶液生成G_____________________ 、G+NaOH溶液生成N______________________________________________________ 。
(3)单质C不溶于冷的浓硝酸的原因是____________________________ 。

其中氧化物A是白色固体;氧化物B是黑色固体;单质D为有毒的黄绿色气体,单质C不溶于冷的浓硝酸。
(1)D是
(2)写出下列反应的离子方程式:M+NaOH溶液生成G
(3)单质C不溶于冷的浓硝酸的原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A~I分别表示中学化学中常见的一种物质,其中A、I为常见金属,它们之间的相互关系如图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六各物质中均含同一种元素。
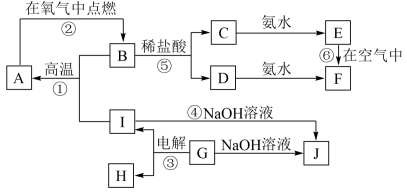
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素在元素周期表中的位置是________________________ 。
(2)检验C溶液中阳离子的方法是(写出操作,现象及结论)_____________________________________________________________________________________________ 。
(3)写出下列反应的化学方程式或离子方程式:
反应①的化学方程式:______________________________________________ ;
反应④的离子方程式:______________________________________________ ;
反应⑥的化学方程式:______________________________________________ ;
(4)从能量变化的角度看,反应①②③中,属于△H<0的反应是________ (填序号)。

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素在元素周期表中的位置是
(2)检验C溶液中阳离子的方法是(写出操作,现象及结论)
(3)写出下列反应的化学方程式或离子方程式:
反应①的化学方程式:
反应④的离子方程式:
反应⑥的化学方程式:
(4)从能量变化的角度看,反应①②③中,属于△H<0的反应是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下图所涉及的物质均为中学化学中的常见物质,其中C为气体单质一种主要成分、D在常温下是黄绿色气体、E为Fe单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。
(1)写出有关物质的化学式
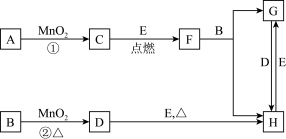
F______________ ,G_______________ ,H_________________ 。
(2)指出MnO2在相关反应中的作用,反应①中是___________ 剂,反应②中是____________ 剂。
(3)若反应①是在加热条件下进行,则A是___________ ;若反应①是在常温条件下进行,则A的电子式为______________ 。
(4)写出B与MnO2共热获得D的离子方程式________________ 。
(5)写出B与F反应的化学方程式___________________________ 。
(1)写出有关物质的化学式

F
(2)指出MnO2在相关反应中的作用,反应①中是
(3)若反应①是在加热条件下进行,则A是
(4)写出B与MnO2共热获得D的离子方程式
(5)写出B与F反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知A、E为金属单质,B为淡黄色粉末且常用于防毒面具中,回答下列问题。

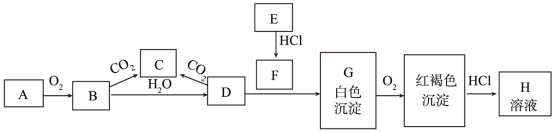
(1)实验室中A常常保存在盛有_______ 的广口瓶中,A的焰色反应为________ 色。
(2)写出B转变为C的化学方程式_______ 。该反应中氧化剂是________ ,0.1molB参与该反应,转移电子的数目为________ 。
(3)写出B转变为D的离子方程式_______ 。该反应中还原剂是________ ,该反应生成0.1molD,转移电子的数目为______ 。
(4)描述G露置在空气中的变化现象______ ,写出该过程的化学方程式________ 。
(5)写出E与水蒸气反应的化学方程式________ 。


(1)实验室中A常常保存在盛有
(2)写出B转变为C的化学方程式
(3)写出B转变为D的离子方程式
(4)描述G露置在空气中的变化现象
(5)写出E与水蒸气反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。
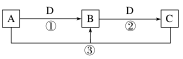
请回答下列问题:
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,则B的化学式可能是___________ ;实验室中制取A的离子方程式为___________ 。
(2)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为___________ 。某同学将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的酸性呈逐渐增强的趋势,用离子方程式解释原因:___________ 。

请回答下列问题:
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,则B的化学式可能是
(2)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为
您最近一年使用:0次



