(1)铁钉与氯气反应生成棕黄色物质 ,而铁钉在盐酸中生成浅绿色的
,而铁钉在盐酸中生成浅绿色的 溶液。则在
溶液。则在 、
、 、
、 中,具有氧化性的是
中,具有氧化性的是______ ,其中氧化性较强的是_______ 。
(2) 在不同的反应中,可以分别表现出酸性、氧化性和还原性。现有如下反应,请写出
在不同的反应中,可以分别表现出酸性、氧化性和还原性。现有如下反应,请写出 在反应中表现出的性质。
在反应中表现出的性质。
① :
:______ 。
②2HCl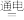 H2+Cl2:
H2+Cl2:______ 。
(3)找出第(2)小题中氧化还原反应的化学方程式,并用双线桥法标出电子转移的方向和数目:___ 。
 ,而铁钉在盐酸中生成浅绿色的
,而铁钉在盐酸中生成浅绿色的 溶液。则在
溶液。则在 、
、 、
、 中,具有氧化性的是
中,具有氧化性的是(2)
 在不同的反应中,可以分别表现出酸性、氧化性和还原性。现有如下反应,请写出
在不同的反应中,可以分别表现出酸性、氧化性和还原性。现有如下反应,请写出 在反应中表现出的性质。
在反应中表现出的性质。①
 :
:②2HCl
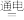 H2+Cl2:
H2+Cl2:(3)找出第(2)小题中氧化还原反应的化学方程式,并用双线桥法标出电子转移的方向和数目:
更新时间:2020/09/01 12:11:37
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)已知反应:K2Cr2O7 + 14HCl=2KCl + 2CrCl3 + 3Cl2↑+ 7H2O,用“单线桥”表示电子转移的方向和数目,并指出氧化产物和还原产物_____________ 。
(2)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气),若反应中消耗Cl2 1.5 mol,求被氧化的NH3在标准状况下的体积_________________ 。
(2)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气),若反应中消耗Cl2 1.5 mol,求被氧化的NH3在标准状况下的体积
您最近半年使用:0次
【推荐2】已知下列反应:
①CO2+H2O=H2CO3 ②C+H2O H2+CO
H2+CO
③2F2+2H2O=4HF+O2↑ ④2Na+2H2O=2NaOH+H2↑
⑤NaH+H2O=NaOH+H2↑ (NaH中H为-1价) ⑥Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
(1)上述反应中不属于氧化还原反应的有___________ (填序号,下同);反应物中H2O被还原的是___________ ;氧化产物为单质的是___________ 。
(2)用单线桥法表示反应④中电子转移的情况:___________ 。
(3)已知化学方程式:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑。上述反应中氧化产物和还原产物的质量比为___________ ;浓盐酸的作用是___________ (填字母)。
A.氧化性 B.还原性 C.酸性 D.挥发性
(4)反应NaH+H2O=NaOH+H2↑中,每生成2个H2分子,转移___________ 个电子。
①CO2+H2O=H2CO3 ②C+H2O
 H2+CO
H2+CO ③2F2+2H2O=4HF+O2↑ ④2Na+2H2O=2NaOH+H2↑
⑤NaH+H2O=NaOH+H2↑ (NaH中H为-1价) ⑥Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
(1)上述反应中不属于氧化还原反应的有
(2)用单线桥法表示反应④中电子转移的情况:
(3)已知化学方程式:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑。上述反应中氧化产物和还原产物的质量比为
A.氧化性 B.还原性 C.酸性 D.挥发性
(4)反应NaH+H2O=NaOH+H2↑中,每生成2个H2分子,转移
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2,其反应的化学方程式如下:Cu+2FeCl3=CuCl2+2FeCl2
(1)请在上式中用双线桥法标出得、失电子的情况________ 。
(2)指出上述反应中的氧化剂和还原剂。氧化剂是__________ ,还原剂是__________ 。
(3)使用过的腐蚀液会失效,但还可以回收利用,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是__________ (填序号)。
A.氯气 B.铁 C.盐酸 D.稀硫酸
(1)请在上式中用双线桥法标出得、失电子的情况
(2)指出上述反应中的氧化剂和还原剂。氧化剂是
(3)使用过的腐蚀液会失效,但还可以回收利用,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是
A.氯气 B.铁 C.盐酸 D.稀硫酸
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氧化还原反应在生活、生产与科学实验中有重要作用。
回答下列问题:
(1)亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
①误食 会导致入体血红蛋白中的
会导致入体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 发生反应
发生反应_____ (填“氧化”或“还原”,下同),服用维生素 可将
可将 转化为
转化为 从而解毒,这说明维生素
从而解毒,这说明维生素 具有
具有________ 性。
②实验室可利用反应 制备少量
制备少量 ,若反应中有
,若反应中有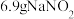 固体生成,则转移电子的物质的量为
固体生成,则转移电子的物质的量为________  。
。
(2) 、
、 是常用的氧化剂。
是常用的氧化剂。
①已知: 、
、 、
、 、
、 和一些未知物组成一个氧化还原反应,其中
和一些未知物组成一个氧化还原反应,其中 是氧化产物,则还原性:
是氧化产物,则还原性:
_________  (填“
(填“ ”或“
”或“ ”)。
”)。
②请结合①中反应,写出一个能证明氧化性 的离子方程式:
的离子方程式:___________________ 。
(3)高铁酸钾( )是一种高效多功能的新型非氯绿色消毒剂。
)是一种高效多功能的新型非氯绿色消毒剂。
①工业上可通过次氯酸盐氧化法制备 :
: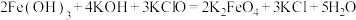 。请写出该反应的离子方程式并用双线桥法标出电子转移的方向与数目:
。请写出该反应的离子方程式并用双线桥法标出电子转移的方向与数目:___________________ 。
② 净水原理如图所示:
净水原理如图所示:

若过程 中转移
中转移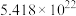 个电子,需
个电子,需____________ 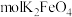 。
。
③向 溶液中加入适量的饱和
溶液中加入适量的饱和 溶液,有
溶液,有 析出,写出该反应的离子方程式:
析出,写出该反应的离子方程式:____________ 。
回答下列问题:
(1)亚硝酸钠(
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。①误食
 会导致入体血红蛋白中的
会导致入体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 发生反应
发生反应 可将
可将 转化为
转化为 从而解毒,这说明维生素
从而解毒,这说明维生素 具有
具有②实验室可利用反应
 制备少量
制备少量 ,若反应中有
,若反应中有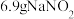 固体生成,则转移电子的物质的量为
固体生成,则转移电子的物质的量为 。
。(2)
 、
、 是常用的氧化剂。
是常用的氧化剂。①已知:
 、
、 、
、 、
、 和一些未知物组成一个氧化还原反应,其中
和一些未知物组成一个氧化还原反应,其中 是氧化产物,则还原性:
是氧化产物,则还原性:
 (填“
(填“ ”或“
”或“ ”)。
”)。②请结合①中反应,写出一个能证明氧化性
 的离子方程式:
的离子方程式:(3)高铁酸钾(
 )是一种高效多功能的新型非氯绿色消毒剂。
)是一种高效多功能的新型非氯绿色消毒剂。①工业上可通过次氯酸盐氧化法制备
 :
: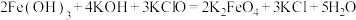 。请写出该反应的离子方程式并用双线桥法标出电子转移的方向与数目:
。请写出该反应的离子方程式并用双线桥法标出电子转移的方向与数目:②
 净水原理如图所示:
净水原理如图所示:
若过程
 中转移
中转移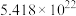 个电子,需
个电子,需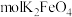 。
。③向
 溶液中加入适量的饱和
溶液中加入适量的饱和 溶液,有
溶液,有 析出,写出该反应的离子方程式:
析出,写出该反应的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据所学知识回答下列问题:
(1)H2O2是常见氧化剂,为了验证其氧化性,进行了下列实验:
①取 H2O2于试管中,通入H2S气体,溶液变浑浊,反应的化学方程式为
H2O2于试管中,通入H2S气体,溶液变浑浊,反应的化学方程式为_______ 。
②有同学认为 2
2 3也有还原性,可以选择其作为试剂验证) H2O2氧化性。该观点是否可行,说明理由:
3也有还原性,可以选择其作为试剂验证) H2O2氧化性。该观点是否可行,说明理由:_______ 。
(2)饮用水中的 对人类健康会产生危害,为了降低饮用水中)
对人类健康会产生危害,为了降低饮用水中) 的浓度,某饮用水研究人员提出两种处理方案:方案一,碱性条件下
的浓度,某饮用水研究人员提出两种处理方案:方案一,碱性条件下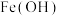 2还原
2还原 生成
生成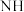 3,反应中氧化剂和还原剂物质的量之比为
3,反应中氧化剂和还原剂物质的量之比为_______ ;方案二,在碱性条件下,用铝粉处理,已知反应时Al与 为5∶3,且Al转化为
为5∶3,且Al转化为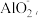 被氧化的元素是
被氧化的元素是_______ ,还原产物是_______ ,请写出反应的离子方程式:_______ 。
(3)已知 3+可以氧化
3+可以氧化 2,则向
2,则向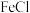 3和
3和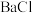 2中通入
2中通入 2会产生白色沉淀,该沉淀是
2会产生白色沉淀,该沉淀是_______ (填化学式)。
(1)H2O2是常见氧化剂,为了验证其氧化性,进行了下列实验:
①取
 H2O2于试管中,通入H2S气体,溶液变浑浊,反应的化学方程式为
H2O2于试管中,通入H2S气体,溶液变浑浊,反应的化学方程式为②有同学认为
 2
2 3也有还原性,可以选择其作为试剂验证) H2O2氧化性。该观点是否可行,说明理由:
3也有还原性,可以选择其作为试剂验证) H2O2氧化性。该观点是否可行,说明理由:(2)饮用水中的
 对人类健康会产生危害,为了降低饮用水中)
对人类健康会产生危害,为了降低饮用水中) 的浓度,某饮用水研究人员提出两种处理方案:方案一,碱性条件下
的浓度,某饮用水研究人员提出两种处理方案:方案一,碱性条件下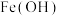 2还原
2还原 生成
生成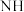 3,反应中氧化剂和还原剂物质的量之比为
3,反应中氧化剂和还原剂物质的量之比为 为5∶3,且Al转化为
为5∶3,且Al转化为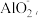 被氧化的元素是
被氧化的元素是(3)已知
 3+可以氧化
3+可以氧化 2,则向
2,则向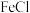 3和
3和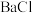 2中通入
2中通入 2会产生白色沉淀,该沉淀是
2会产生白色沉淀,该沉淀是
您最近半年使用:0次
【推荐3】Ⅰ.高铁酸钾( )是一种新型、高效、多功能绿色水处理剂,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
)是一种新型、高效、多功能绿色水处理剂,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为: ,该反应中
,该反应中 是
是___________ (填氧化剂、还原剂)。写出 与水反应的化学方程式,并用单线桥表示出电子转移方向及数目
与水反应的化学方程式,并用单线桥表示出电子转移方向及数目___________ ;将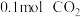 与
与 混合气体通过足量的过氧化钠固体,充分吸收后,固体质量增加了2g,则原混合气体的平均摩尔质量是
混合气体通过足量的过氧化钠固体,充分吸收后,固体质量增加了2g,则原混合气体的平均摩尔质量是___________ 。
(2)湿法制备高铁酸钾的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 。
。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:___________ 。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为___________ mol。
Ⅱ. 已知: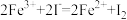 ,
,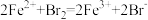 。
。
(3)含有 和
和 的混合溶液中通入少量
的混合溶液中通入少量 ,此时最先被氧化的离子是
,此时最先被氧化的离子是___________ 。
(4)若向含 和
和 的混合溶液中通入
的混合溶液中通入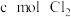 ,当
,当 、
、 、
、 完全被氧化时,c=
完全被氧化时,c=___________ (用含x、y的代数式表示)。
 )是一种新型、高效、多功能绿色水处理剂,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
)是一种新型、高效、多功能绿色水处理剂,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。(1)干法制备高铁酸钠的主要反应为:
 ,该反应中
,该反应中 是
是 与水反应的化学方程式,并用单线桥表示出电子转移方向及数目
与水反应的化学方程式,并用单线桥表示出电子转移方向及数目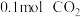 与
与 混合气体通过足量的过氧化钠固体,充分吸收后,固体质量增加了2g,则原混合气体的平均摩尔质量是
混合气体通过足量的过氧化钠固体,充分吸收后,固体质量增加了2g,则原混合气体的平均摩尔质量是(2)湿法制备高铁酸钾的反应体系中有六种微粒:
 、
、 、
、 、
、 、
、 、
、 。
。①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为
Ⅱ. 已知:
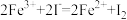 ,
,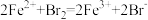 。
。(3)含有
 和
和 的混合溶液中通入少量
的混合溶液中通入少量 ,此时最先被氧化的离子是
,此时最先被氧化的离子是(4)若向含
 和
和 的混合溶液中通入
的混合溶液中通入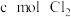 ,当
,当 、
、 、
、 完全被氧化时,c=
完全被氧化时,c=
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Cl2是一种重整的化工原料,在生产、生活和工业上均有很多用途。
(1)可与氢气化合制得盐酸。化学方程式为________________ 。
(2)可与NaOH溶液反应制得漂白液(84消毒液),离子方程式为_______________ 。
(3)可用于工业上制得高锰酸钾(KMnO4),KMnO4中Mn的化合价为_______________ 。其工业制备的部分工艺如下:
Ⅰ.将软锰矿(主要成分为MnO2)粉碎后,与KOH固体混合,通入氯气充分焙烧,生成暗绿色熔融态物质。
Ⅱ.冷却,将固体研细,用稀KOH溶液慢取,过滤,得暗绿色溶液。
Ⅲ.向暗绿色溶液中通入CO2,溶液变为紫红色,同时生成黑色固体。
Ⅳ.过滤,将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得KMnO4固体。
资料: K2MnO4为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液源中易发生歧化反应(Mn的化合价既升高又降低)。
①Ⅰ中,粉碎软锰矿的目的是_____________ 。
②Ⅰ中,生成K2MnO4的化学方程式是____________ 。
③Ⅱ中,浸取时用稀KOH溶液的原因是_____________ 。
④Ⅲ中,CO2和K2MnO4在溶液中反应的离子方程式是:MnO +CO2 +H2O→MnO
+CO2 +H2O→MnO +MnO2 +HCO
+MnO2 +HCO (未配平),氧化产物和还原产物的物质的量之比为
(未配平),氧化产物和还原产物的物质的量之比为____________ 。
(1)可与氢气化合制得盐酸。化学方程式为
(2)可与NaOH溶液反应制得漂白液(84消毒液),离子方程式为
(3)可用于工业上制得高锰酸钾(KMnO4),KMnO4中Mn的化合价为
Ⅰ.将软锰矿(主要成分为MnO2)粉碎后,与KOH固体混合,通入氯气充分焙烧,生成暗绿色熔融态物质。
Ⅱ.冷却,将固体研细,用稀KOH溶液慢取,过滤,得暗绿色溶液。
Ⅲ.向暗绿色溶液中通入CO2,溶液变为紫红色,同时生成黑色固体。
Ⅳ.过滤,将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得KMnO4固体。
资料: K2MnO4为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液源中易发生歧化反应(Mn的化合价既升高又降低)。
①Ⅰ中,粉碎软锰矿的目的是
②Ⅰ中,生成K2MnO4的化学方程式是
③Ⅱ中,浸取时用稀KOH溶液的原因是
④Ⅲ中,CO2和K2MnO4在溶液中反应的离子方程式是:MnO
 +CO2 +H2O→MnO
+CO2 +H2O→MnO +MnO2 +HCO
+MnO2 +HCO (未配平),氧化产物和还原产物的物质的量之比为
(未配平),氧化产物和还原产物的物质的量之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ。亚硫酸钠中+4价的硫,它既有氧化性又有还原性,现在有试剂:新制氯水、硫化钠溶液,NaOH溶液、氯化钡溶液、稀硫酸。要证明亚硫酸钠具有还原性,除亚硫酸钠外还应选用的试剂有______ ,看到的现象是______ ,反应的离子方程式______ ;
Ⅱ。A、B、C是三种中学常见的有色物质,摩尔质量依次增大,他们均能与水发生氧化还原反应,但水既不是氧化剂也不是还原剂,请写出A、B、C与水反应的化学方程式:
(1)A+H2O______
(2)B+H2O______
(3)C+H2O______
Ⅱ。A、B、C是三种中学常见的有色物质,摩尔质量依次增大,他们均能与水发生氧化还原反应,但水既不是氧化剂也不是还原剂,请写出A、B、C与水反应的化学方程式:
(1)A+H2O
(2)B+H2O
(3)C+H2O
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列问题。
(1)在① 、②
、② 、③
、③ 、④
、④ 、⑤S、⑥
、⑤S、⑥ 、⑦
、⑦ 中,只有氧化性的是
中,只有氧化性的是___________ (填写编号,下同),只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(2)某同学写出以下三个化学方程式(未配平):① ;②
;②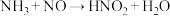 ;③
;③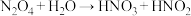 。其中你认为一定不可能实现的是
。其中你认为一定不可能实现的是___________ 。
(3)根据反应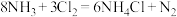 ,回答下列问题。
,回答下列问题。
①氧化性:Cl2__________ N2。(填“大于”“小于”“等于”)
②氧化剂与还原剂的分子个数之比为___________ 。
③当生成28g N2时,被氧化的物质的质量为__________ g。
(1)在①
 、②
、② 、③
、③ 、④
、④ 、⑤S、⑥
、⑤S、⑥ 、⑦
、⑦ 中,只有氧化性的是
中,只有氧化性的是(2)某同学写出以下三个化学方程式(未配平):①
 ;②
;②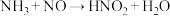 ;③
;③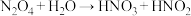 。其中你认为一定不可能实现的是
。其中你认为一定不可能实现的是(3)根据反应
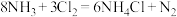 ,回答下列问题。
,回答下列问题。①氧化性:Cl2
②氧化剂与还原剂的分子个数之比为
③当生成28g N2时,被氧化的物质的质量为
您最近半年使用:0次



