如图为周期表的一小部分,A、B、C、D的位置关系如图所示。且它们均为短周期元素,其中C元素的最外层电子数是电子层数的2倍,回答下列问题:
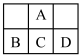
(1)在B、C、D最高价氧化物对应水化物中,酸性最强的是__ (写分子式)。
(2)在A、B、C所形成氢化物中,A的电子式:___ ,其中最稳定的是__ (写分子式)。
(3)写D的单质与C的氢化物反应的化学方程式__ 。
(4)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是__ (用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000kg该溶液需消耗氯气的质量为___ kg(保留整数)。

(1)在B、C、D最高价氧化物对应水化物中,酸性最强的是
(2)在A、B、C所形成氢化物中,A的电子式:
(3)写D的单质与C的氢化物反应的化学方程式
(4)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是
更新时间:2020-09-03 16:26:47
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】联合国大会将2019年定为“化学元素周期表国际年”,高度体现了元素周期表的重要性。部分元素在周期表中的位置如图:
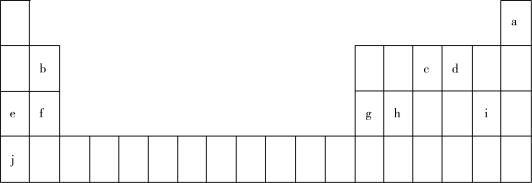
(1)2021年2月22日,嫦娥五号采样返回器带回的月壤公开亮相,对月壤中化学元素的分析有助于认识月球表面环境。
①月壤中含有较丰富的质量数为3的a,它可以作为未来核聚变的重要原料之一,a的这种核素表示为_______ 。
②经分析,月壤中含有大量的元素d和h,原子半径d_______ h(填“>”、“<”或“=”),元素h在周期表中的位置为_______ 。
(2)e和f的单质都是化学家戴维通过电解的方法首次制得。e的单质与水反应的化学方程式为_______ ,用电子式表示f原子与i原子形成化合物的形成过程:_______ 。
(3)d和i两种元素的简单氢化物中,熔沸点较高的氢化物的电子式为_______ 。
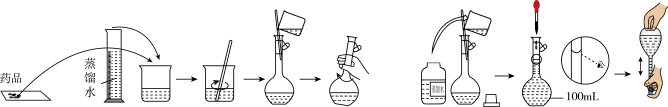
(4)《天工开物》记载,“凡火药,以硝石、硫磺为主,草木灰为辅”,由c、d、j三种元素组成的化合物是硝石的主要成分,化学式为_______ 。实验室按照如图操作配制该溶液,所得溶液浓度_______ (填“偏大”或“偏小”)。
(5)元素b与g的性质相似,可以预测b与g的单质或化合物也可能具有相似的性质。请写出b的最高价氧化物对应水化物与e的最高价氧化物对应水化物反应的化学方程式_______ 。

(1)2021年2月22日,嫦娥五号采样返回器带回的月壤公开亮相,对月壤中化学元素的分析有助于认识月球表面环境。
①月壤中含有较丰富的质量数为3的a,它可以作为未来核聚变的重要原料之一,a的这种核素表示为
②经分析,月壤中含有大量的元素d和h,原子半径d
(2)e和f的单质都是化学家戴维通过电解的方法首次制得。e的单质与水反应的化学方程式为
(3)d和i两种元素的简单氢化物中,熔沸点较高的氢化物的电子式为
(4)《天工开物》记载,“凡火药,以硝石、硫磺为主,草木灰为辅”,由c、d、j三种元素组成的化合物是硝石的主要成分,化学式为

(5)元素b与g的性质相似,可以预测b与g的单质或化合物也可能具有相似的性质。请写出b的最高价氧化物对应水化物与e的最高价氧化物对应水化物反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
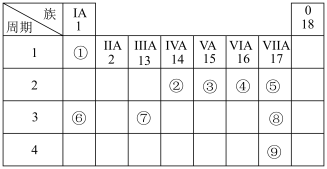
【推荐2】为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。如表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:

(1)②①4的电子式为_______ ;元素⑧在周期表中的位置是_______ 。
(2)④、⑤、⑥的原子半径的大小顺序是_______ (用元素符号表示)。④和⑨的简单气态氢化物中稳定性较强的是_______ (用化学式表示)。
(3)⑨的最高价氧化物的水化物是_______ (用化学式表示)。⑦和⑧两者的最高价氧化物的水化物之间发生反应的离子方程式是_______ 。
(4)已知②⑧2在氧气中完全燃烧,生成②③2和⑧③2,若 0.1 mol ②⑧2在 1 mol ③2中完全燃烧,所得混合气体在标准状况下的体积为_______ L。

(1)②①4的电子式为
(2)④、⑤、⑥的原子半径的大小顺序是
(3)⑨的最高价氧化物的水化物是
(4)已知②⑧2在氧气中完全燃烧,生成②③2和⑧③2,若 0.1 mol ②⑧2在 1 mol ③2中完全燃烧,所得混合气体在标准状况下的体积为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下表为元素周期表的一部分,请参考元素①~①在表中的位置,回答下列问题。
(1)元素①与元素④形成的原子个数比为2:1的化合物沸点高的原因是_____ 。
(2)考古工作者利用元素②的一种核素_____ 测定一些文物的年代。
(3)③④⑤三种元素的简单气态氢化物,热稳定性顺序是_____ (填化学式,用“>”连接)。
(4)元素⑥的最高价氧化物的水化物的电子式_____ ,该化合物中的化学键类型为_____ 。
(5)元素⑦的最高价氧化物与稀硫酸反应的化学方程式为_____ 。
(6)设计能证明元素⑧比⑨的非金属性强的实验操作及现象_____ 。

(1)元素①与元素④形成的原子个数比为2:1的化合物沸点高的原因是
(2)考古工作者利用元素②的一种核素
(3)③④⑤三种元素的简单气态氢化物,热稳定性顺序是
(4)元素⑥的最高价氧化物的水化物的电子式
(5)元素⑦的最高价氧化物与稀硫酸反应的化学方程式为
(6)设计能证明元素⑧比⑨的非金属性强的实验操作及现象
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某同学探究同周期部分元素性质递变规律时,设计实验方案并记录实验现象。
请帮助该同学整理并完成实验报告。
(1)实验目的:___________ 。
(2)实验用品:
药品:金属钠、镁条、铝条、稀盐酸、新制氯水、 溶液、NaOH溶液、酚酞溶液等;
溶液、NaOH溶液、酚酞溶液等;
仪器:___________ 、___________ 、烧杯、酒精灯、试管夹、镊子、小刀、玻璃片、砂纸等。
(3)实验内容:(填写与实验步骤标号相对应的实验现象的序号并写出相关反应的化学方程式)
(4)实验结论:___________ 。
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入沸水中,再向溶液中滴加少量酚酞溶液 | A.浮在水面上,熔成小球,做不定向运动,随后消失,溶液变成红色 |
②向 溶液中滴加NaOH溶液至过量 溶液中滴加NaOH溶液至过量 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将镁条放入盐酸中 | D.反应较快,产生无色气体 |
| ⑤将铝条放入盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
(1)实验目的:
(2)实验用品:
药品:金属钠、镁条、铝条、稀盐酸、新制氯水、
 溶液、NaOH溶液、酚酞溶液等;
溶液、NaOH溶液、酚酞溶液等;仪器:
(3)实验内容:(填写与实验步骤标号相对应的实验现象的序号并写出相关反应的化学方程式)
| 实验步骤 | 实验现象 | 相应化学方程式 |
| ① | ① | |
| ② | ② | |
| ③ | ||
| ④ | ||
| ⑤ |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,用化学用语回答下列有关问题:
(1)⑧的原子结构示意图为:___________________ ;
(2)表中某两种元素的原子形成的5核10电子分子是:______________ (写化学式);
(3)③、⑧、⑨的最高价含氧酸的酸性最强的是:___________________ (写化学式);
(4)③的气态氢化物与③的最高价氧化物对应的水化物反应生成的盐是___________ (写化学式),它属于_____________________ (选填“共价化合物”或“离子化合物”)
(5)表中分别位于三个周期的三种元素的原子能形成原子数目比为1:1:1的共价化合物,它的化学式为:______________________
(6)由⑥的单质与某物质反应生成②的单质的化学方程式为:_______________
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)⑧的原子结构示意图为:
(2)表中某两种元素的原子形成的5核10电子分子是:
(3)③、⑧、⑨的最高价含氧酸的酸性最强的是:
(4)③的气态氢化物与③的最高价氧化物对应的水化物反应生成的盐是
(5)表中分别位于三个周期的三种元素的原子能形成原子数目比为1:1:1的共价化合物,它的化学式为:
(6)由⑥的单质与某物质反应生成②的单质的化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:

(1)⑤、⑥、⑦的原子半径由大到小的顺序为_________________ ;
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_________________ ;
(3)④与⑤两元素可形成既含离子键又含非极性共价键的化合物,写出该化合物的化学式_________________ ;
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)_______ ;
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)元素⑥的氯化物溶液与稀氨水溶液反应的离子方程式_________________ ;
(6)工业上冶炼单质⑥的反应原理_________________ ;
(7)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被MnO2催化分解,写出反应的化学方程式_________________ 。

(1)⑤、⑥、⑦的原子半径由大到小的顺序为
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)④与⑤两元素可形成既含离子键又含非极性共价键的化合物,写出该化合物的化学式
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)元素⑥的氯化物溶液与稀氨水溶液反应的离子方程式
(6)工业上冶炼单质⑥的反应原理
(7)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被MnO2催化分解,写出反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】五种短周期元素X、Y、Z、L、M,原子序数依次递增。X是原子半径最小的元素,Y的最高正价和最低负价的代数和为0,Z的气态氢化物和它的最高价氧化物对应的水化物能发生化合反应,L的最外层电子数是次外层的3倍,M是地壳中含量最高的金属元素。
回答下列问题:
(1)五种元素的原子半径从大到小的顺序是______ (用元素符号表示)。
(2)X能分别与Y、Z、L形成具有相同电子数的化合物A、B、C。实验室制取B的化学方程式为______ 。
(3)Z的最高价氧化物对应水化物与M的最高价氧化物对应水化物反应的离子方程式为_______ 。
(4)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为_______ ,其最高价氧化物对应的水化物化学式为______ 。
回答下列问题:
(1)五种元素的原子半径从大到小的顺序是
(2)X能分别与Y、Z、L形成具有相同电子数的化合物A、B、C。实验室制取B的化学方程式为
(3)Z的最高价氧化物对应水化物与M的最高价氧化物对应水化物反应的离子方程式为
(4)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表为元素周期表短同期的一部分, A、B、C、D、E五种元素在周期表中的位置如下图所示。C元素的原子最外层电子数为次外层的3倍。
回答下列问题:
(1)B元素在周期表中的位置为__________ 。
(2)D的最高价氧化物对应水化物的化学式为__________ 。
(3)下列事实能说明C元素的非金属性比硫元素的非金属性强的是__________ 。
a.C单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molC单质比1molS得电子多
c.C和S两元素的简单氢化物受热分解,前者的分解温度高
d. C元素的简单氢化物沸点高于S元素的简单氢化物
(4)B与D两元素的单质反应生成化合物M,它的结构类似甲烷,写出M的电子式_____ 。
(5)A与镁形成的1mol化合物N与水反应,生成2molMg(OH)2和1mol气态烃,该烃分子中碳氢质量比为9:1,写出N与水反应的化学方程式______________________________ 。
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol/LNaOH溶液和1molO2,则两种气体的分子式及物质的量分别为__________ 。
| A | E | C | |
| B | D |
(1)B元素在周期表中的位置为
(2)D的最高价氧化物对应水化物的化学式为
(3)下列事实能说明C元素的非金属性比硫元素的非金属性强的是
a.C单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molC单质比1molS得电子多
c.C和S两元素的简单氢化物受热分解,前者的分解温度高
d. C元素的简单氢化物沸点高于S元素的简单氢化物
(4)B与D两元素的单质反应生成化合物M,它的结构类似甲烷,写出M的电子式
(5)A与镁形成的1mol化合物N与水反应,生成2molMg(OH)2和1mol气态烃,该烃分子中碳氢质量比为9:1,写出N与水反应的化学方程式
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol/LNaOH溶液和1molO2,则两种气体的分子式及物质的量分别为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10;X和 原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z在同周期元素中电负性最大。
原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z在同周期元素中电负性最大。

(1)Y位于元素周期表中第_______ 纵行,属于_______ 区;W的基态原子核外有_______ 个未成对电子。四种元素中第一电离能最小的元素是_______ (写元素符号)
(2)X的单质和Y的单质相比,熔点较高的是_______ (写化学式);Z的气态氢化物和Y的气态氢化物相比,较稳定的是_______ (写化学式),两元素对应最高价氧化物的水化物酸性更强的是_______ (写化学式)。
(3)Y单质可以与X的最高价氧化物的水化物溶液反应,该反应的化学方程式是_______ 。
 原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z在同周期元素中电负性最大。
原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z在同周期元素中电负性最大。
(1)Y位于元素周期表中第
(2)X的单质和Y的单质相比,熔点较高的是
(3)Y单质可以与X的最高价氧化物的水化物溶液反应,该反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经一百多年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
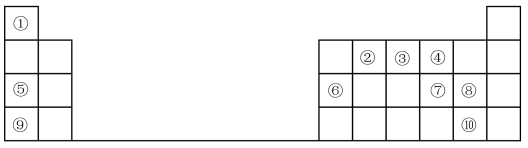
(1)元素②在周期表中的位置___________
(2)元素⑤和⑨的最高价氧化物的水化物中,碱性较强的是___________ (填化学式)。
(3)元素①与⑦可形成18电子分子,请用电子式表示该分子的形成过程:___________ 。
(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是___________ (用离子符号表示),
(5)元素⑨的最高价氧化物的水化物与元素⑥的单质反应的化学方程式为:___________ 。
(6)元素的非金属性⑩___________ ⑧(填“>”或“<”);下列事实不能 证明上述结论的是___________ 。
A.元素⑧的单质与⑩的气态氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的气态氢化物的水溶液的酸性比元素⑩的弱
C.元素⑧和⑩的气态氢化物受热分解,前者的分解温度高
D.元素⑧的最高价氧化物的水化物的酸性比元素⑩的强
E.元素⑧的气态氢化物的还原性比元素⑩的弱

(1)元素②在周期表中的位置
(2)元素⑤和⑨的最高价氧化物的水化物中,碱性较强的是
(3)元素①与⑦可形成18电子分子,请用电子式表示该分子的形成过程:
(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是
(5)元素⑨的最高价氧化物的水化物与元素⑥的单质反应的化学方程式为:
(6)元素的非金属性⑩
A.元素⑧的单质与⑩的气态氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的气态氢化物的水溶液的酸性比元素⑩的弱
C.元素⑧和⑩的气态氢化物受热分解,前者的分解温度高
D.元素⑧的最高价氧化物的水化物的酸性比元素⑩的强
E.元素⑧的气态氢化物的还原性比元素⑩的弱
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W、Q为原子序数依次增大的短周期主族元素,分别位于三个周期。Y元素原子的最外层电子数是次外层的三倍,Y元素与X、Z元素均能形成两种常见的二元化合物,其中与X形成的化合物分别为A和B,A可以用来杀菌消毒:X、Y、Z元素原子的最外层电子数之和为W元素原子所含质子数的一半。据此回答下列问题。
(1)画出Q元素简单离子的离子结构示意图___________ ,元素W在周期表中的位置为___________ 。
(2)B分子的空间结构为___________ ,A的电子式为___________ ,Z与W所形成的简单化合物中含有的化学键类型为___________ 。
(3)请写出Z的最高价氧化物对应水化物与Q的最高价氧化物对应水化物反应的离子方程式___________ 。
(4)X的单质与Q的单质能反应生成一种气体,将集满该气体的试管倒立于水槽中,产生的现象是___________ 。
a.试管中液面略有上升 b.液体几乎充满试管
c.液面升至距管口1/2处 d.无现显现象
(5)X与W组成的18电子带电微粒不能在强碱性溶液中大量共存,请写出反应的离子方程式___________ 。
(1)画出Q元素简单离子的离子结构示意图
(2)B分子的空间结构为
(3)请写出Z的最高价氧化物对应水化物与Q的最高价氧化物对应水化物反应的离子方程式
(4)X的单质与Q的单质能反应生成一种气体,将集满该气体的试管倒立于水槽中,产生的现象是
a.试管中液面略有上升 b.液体几乎充满试管
c.液面升至距管口1/2处 d.无现显现象
(5)X与W组成的18电子带电微粒不能在强碱性溶液中大量共存,请写出反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了6种元素在周期表中的位置,其中①~③代表3种元素。
(1)①的元素符号是_______ 。
(2)下列能说明 比
比 失电子能力强的事实是
失电子能力强的事实是_______ (填字母)。
 比
比 更容易与水反应置换出氢
更容易与水反应置换出氢
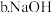 是强碱,
是强碱, 是中强碱
是中强碱
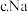 的密度比
的密度比 的小
的小
(3)非金属性②强于③,用原子结构解释原因:②和③位于同一主族,最外层电子数相同,_______ ,原子半径②小于③,得电子能力②强于③。
(4)依据元素周期律,预测气态氢化物的热稳定性: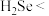
_______ (填写化学式,一种即可)。
| \ | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ||||||||
| 3 |  |  | ① | ② | ||||
| 4 |  | ③ |
(2)下列能说明
 比
比 失电子能力强的事实是
失电子能力强的事实是 比
比 更容易与水反应置换出氢
更容易与水反应置换出氢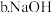 是强碱,
是强碱, 是中强碱
是中强碱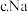 的密度比
的密度比 的小
的小(3)非金属性②强于③,用原子结构解释原因:②和③位于同一主族,最外层电子数相同,
(4)依据元素周期律,预测气态氢化物的热稳定性:
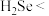
您最近一年使用:0次



