氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
 ,已知
,已知 、
、 、FeO、
、FeO、 四种物质中的一种能使上述还原过程发生。
四种物质中的一种能使上述还原过程发生。
(1)写出并配平该氧化还原反应的化学方程式:______________________________________
(2)反应过程中体现出硝酸具有_____________ (填硝酸的性质)。
(3)反应过程中若产生0.2mol气体,则转移电子的物质的量是_____________ 。

 ,已知
,已知 、
、 、FeO、
、FeO、 四种物质中的一种能使上述还原过程发生。
四种物质中的一种能使上述还原过程发生。(1)写出并配平该氧化还原反应的化学方程式:
(2)反应过程中体现出硝酸具有
(3)反应过程中若产生0.2mol气体,则转移电子的物质的量是
15-16高三上·陕西西安·阶段练习 查看更多[10]
(已下线)考点05 氧化还原反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)易错专题07 氧化还原反应电子转移的表示及方程式的书写-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)高一必修第一册(苏教2019版)专题4 第二单元 硫及其化合物的相互转化 课时2 含硫物质之间的转化 氧化还原反应方程式的配平鲁科版(2019)高一必修第一册第二章易错疑难集训(二)人教版高一化学必修1第二章《化学物质及其变化》测试卷2016-2017学年浙江省诸暨中学高一上期中化学试卷2015届陕西省西安市第83中高三上学期阶段四考试化学试卷
更新时间:2020-09-14 19:18:53
|
相似题推荐
【推荐1】(1)在反应3Cl2+6KOH(浓)=5KCl+KClO3+3H2O中,氧化产物与还原产物的物质的量之比为___ ,3molCl2参加该反应时,反应中转移___ mol电子。
(2)氧化还原反应中实际上包含氧化和还原两个过程。Cu、NO、Cu(NO3)2、HNO3下面是一个还原过程的反应式:NO3-+4H++3e-=NO↑+H2O。
①写出该氧化还原反应的化学方程式并配平:
__ ___ +__ ___ =__ ___ +__ ___ + __ H2O
②反应中硝酸体现了___ 的性质。
(2)氧化还原反应中实际上包含氧化和还原两个过程。Cu、NO、Cu(NO3)2、HNO3下面是一个还原过程的反应式:NO3-+4H++3e-=NO↑+H2O。
①写出该氧化还原反应的化学方程式并配平:
②反应中硝酸体现了
您最近半年使用:0次
【推荐2】NOx是汽车尾气中的主要污染物之一 ,能形成酸雨,主要反应为:3NO2+H2O →2HNO3+NO,完成下列填空:
(1)在化学方程式上标出电子转移的方向和数目_______________ ;
(2)被氧化与被还原的氮元素的质量比是___________ 。
(3)若反应中转移0.1mol电子,则生成硝酸的质量为____________ g。
(4)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放,当尾气中空气不足时,NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:_______________ 。
(1)在化学方程式上标出电子转移的方向和数目
(2)被氧化与被还原的氮元素的质量比是
(3)若反应中转移0.1mol电子,则生成硝酸的质量为
(4)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放,当尾气中空气不足时,NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】化学与新能源、环境保护息息相关,请回答下列问题。
(1)燃料电池的使用可降低雾霾对环境的影响,甲烷燃料电池可实现由_______ 能转化为_______ 能,甲烷可作为电池_______ (“正”或“负”)极反应物,请写出甲烷燃料电池在酸性环境下正极的电极方程式_______ 。
(2)雾霾天气的形成与汽车尾气的排放有一定的关系,目前科学家也在尝试用Cu+做催化剂,将汽车尾气中的NO用乙烯(C2H4)转化为无毒的N2。其原理如下图所示:

①该过程发生的总反应化学方程式为_______ 。
②若某辆汽车的NO排放量为0.09 g/km,则该车行驶100 km,完成上述转化时,理论上需消耗乙烯的质量为_______ g。
(1)燃料电池的使用可降低雾霾对环境的影响,甲烷燃料电池可实现由
(2)雾霾天气的形成与汽车尾气的排放有一定的关系,目前科学家也在尝试用Cu+做催化剂,将汽车尾气中的NO用乙烯(C2H4)转化为无毒的N2。其原理如下图所示:

①该过程发生的总反应化学方程式为
②若某辆汽车的NO排放量为0.09 g/km,则该车行驶100 km,完成上述转化时,理论上需消耗乙烯的质量为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】完成下列问题。
(1)无机化合物可根据其组成和性质进行分类。以下是一组对“一些物质与水反应”的分类图,请按要求填空:
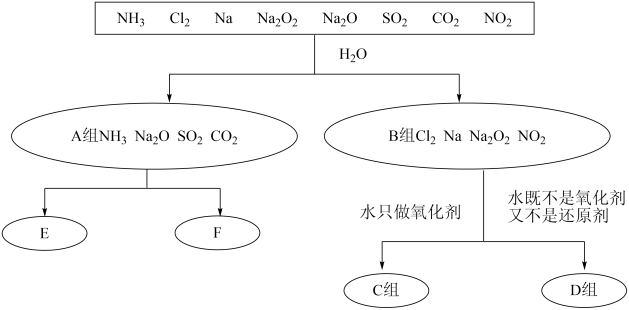
①上述分类中,分成A、B两组的依据是___________ ;
②C组物质与水反应的离子方程式为___________ ;
③D组物质与水反应中,氧化剂和还原剂物质的量之比为1∶1的物质有___________ 。
(2)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→O2
①该反应中,发生还原反应的过程是___________ →___________ 。
②写出该反应的化学方程式,___________
③H2O2可作为矿业废液消毒剂,有“绿色氧化剂”的美称,H2O2被称为绿色氧化剂的理由是_______
(1)无机化合物可根据其组成和性质进行分类。以下是一组对“一些物质与水反应”的分类图,请按要求填空:

①上述分类中,分成A、B两组的依据是
②C组物质与水反应的离子方程式为
③D组物质与水反应中,氧化剂和还原剂物质的量之比为1∶1的物质有
(2)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→O2
①该反应中,发生还原反应的过程是
②写出该反应的化学方程式,
③H2O2可作为矿业废液消毒剂,有“绿色氧化剂”的美称,H2O2被称为绿色氧化剂的理由是
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就三大酸与金属铜反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解,溶液呈现蓝色。则该反应的离子反应方程式为_______
(2)在100mL 18.4 mol∙L−1浓硫酸中加入过量铜片,加热使之反应。
①写出发生反应的化学方程式_______ 。
②生成的气体在标准状况下的实际体积为_______ (填序号) 。
a.等于20.61L b.大于20.61L c.小于20.61L
③若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为_______ 。
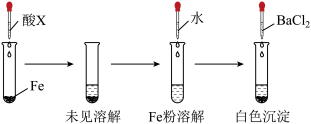
(3)根据如图操作及现象推断酸X为_______ (填序号)
a.浓盐酸 b.浓硫酸 c.浓硝酸
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解,溶液呈现蓝色。则该反应的离子反应方程式为
(2)在100mL 18.4 mol∙L−1浓硫酸中加入过量铜片,加热使之反应。
①写出发生反应的化学方程式
②生成的气体在标准状况下的实际体积为
a.等于20.61L b.大于20.61L c.小于20.61L
③若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为
(3)根据如图操作及现象推断酸X为
a.浓盐酸 b.浓硫酸 c.浓硝酸

您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】已知A是空气中含量最高的一种气体,D是种重要的无机化工原料,由A到D的转化过程如图所示(如图: 表示物质,
表示物质, 表示过程,反应条件及催化剂未标出)。
表示过程,反应条件及催化剂未标出)。
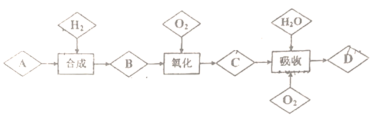
回答下列问题:
(1)物质A的电子式为___________ ,物质D的分子式为___________ 。
(2)“合成"需要在高温、高压和催化剂的条件下进行,其发生反应的化学方程式___________ 。
(3)“吸收”中通入过量O2的目的是___________ 。
(4)工业上贮存物质D的溶液可选择的罐体材料为___________ (填标号)。
a.银 b.铜 c.铝 d.锌
 表示物质,
表示物质, 表示过程,反应条件及催化剂未标出)。
表示过程,反应条件及催化剂未标出)。
回答下列问题:
(1)物质A的电子式为
(2)“合成"需要在高温、高压和催化剂的条件下进行,其发生反应的化学方程式
(3)“吸收”中通入过量O2的目的是
(4)工业上贮存物质D的溶液可选择的罐体材料为
a.银 b.铜 c.铝 d.锌
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】C和浓 的反应(写化学方程式)
的反应(写化学方程式)_______ 。
 的反应(写化学方程式)
的反应(写化学方程式)
您最近半年使用:0次

 与少量氢氧化钠溶液反应的离子方程式:
与少量氢氧化钠溶液反应的离子方程式: 溶液中无明显现象,然后再通入下列气体有沉淀生成,则该气体不可能是
溶液中无明显现象,然后再通入下列气体有沉淀生成,则该气体不可能是

