金属镓(Ga)应用广泛,在半导体和光电材料、合金、磁性材料等领域都有重要应用。镓与铝是同主族元素,性质相似。
(1)铝在元素周期表中的位置是_________________ 。
(2)GaAs是共价化合物,一种重要的半导体材料。As 与 Ga 同周期,As 与 N 同主族。
①下列事实不能用元素周期律解释的是_______________ (填字母)。
a.碱性:Ga (OH)3> Al (OH)3
b.非金属性:As>Ga
c.酸性:H3AsO4>H3AsO3
②GaAs 中,As 元素化合价为-3 价,用原子结构理论解释 As 元素显负价的原因______________________________ 。
③废弃含 GaAs 半导体材料可以用浓硝酸溶解 GaAs,生成 H3AsO4 和 Ga3+,写出该反应的化学方程式________________________________________ 。
(1)铝在元素周期表中的位置是
(2)GaAs是共价化合物,一种重要的半导体材料。As 与 Ga 同周期,As 与 N 同主族。
①下列事实不能用元素周期律解释的是
a.碱性:Ga (OH)3> Al (OH)3
b.非金属性:As>Ga
c.酸性:H3AsO4>H3AsO3
②GaAs 中,As 元素化合价为-3 价,用原子结构理论解释 As 元素显负价的原因
③废弃含 GaAs 半导体材料可以用浓硝酸溶解 GaAs,生成 H3AsO4 和 Ga3+,写出该反应的化学方程式
更新时间:2020-09-15 14:32:56
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】亚硝酸钠NaNO2主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。某小组拟利用氮氧化物制备产品NaNO2。
回答下列问题:
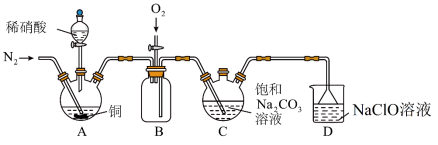
(1)实验室制取N2有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和如图装置(净化装置略去),选出一种可行的方法,写出反应的化学方程式___________ 。【可供选择的试剂:CuO(s)、NH3(g)、Cl2(g)、O2(g)、饱和NaNO2(aq)、饱和NH4Cl(aq)】___________ 。
(3)装置C中NO不能单独被纯碱溶液吸收,若要使氮的氧化物完全被纯碱溶液吸收且产品纯度最高,则n(NO):n(NO2)=___________ ;装置D中倒置漏斗的作用是___________ 。
(4)设计实验探究NaNO2的性质。实验完毕后,从装置C中分离出NaNO2固体粗产品,取少量粗产品配制成溶液,分成2份分别进行甲、乙两组实验,实验操作及现象、结论如表。
①上述实验___________ (填标号)的结论不可靠,理由是___________ 。
②经实验测得实验乙反应后的溶液中氮元素仅以NO 的形式存在,酸性KMnO4溶液与NO
的形式存在,酸性KMnO4溶液与NO 反应的离子方程式为
反应的离子方程式为___________ 。
回答下列问题:
(1)实验室制取N2有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和如图装置(净化装置略去),选出一种可行的方法,写出反应的化学方程式
(3)装置C中NO不能单独被纯碱溶液吸收,若要使氮的氧化物完全被纯碱溶液吸收且产品纯度最高,则n(NO):n(NO2)=
(4)设计实验探究NaNO2的性质。实验完毕后,从装置C中分离出NaNO2固体粗产品,取少量粗产品配制成溶液,分成2份分别进行甲、乙两组实验,实验操作及现象、结论如表。
| 实验操作及现象 | 结论 | |
| 甲 | 滴加少量酸性KI淀粉溶液,振荡,溶液变蓝 | 酸性条件下NO 具有氧化性 具有氧化性 |
| 乙 | 滴加少量酸性KMnO4溶液,振荡,紫色褪去 | 酸性条件下NO 具有还原性 具有还原性 |
②经实验测得实验乙反应后的溶液中氮元素仅以NO
 的形式存在,酸性KMnO4溶液与NO
的形式存在,酸性KMnO4溶液与NO 反应的离子方程式为
反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
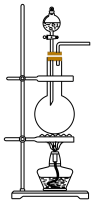
【推荐2】A、B、C、D四种物质之间有下图所示的转化关系。已知:A是空气中的主要成分,B、C、D均为化合物,且C与水反应可得到B。

请回答下列问题:
(1)写出B的名称:_______________________ 。
(2)在上图D→C的过程中,Cu在反应中________ (填“被氧化”或”被还原”)。
(3)在D的稀溶液中滴入Na2CO3溶液,其反应的离子方程式是_______________________ 。

请回答下列问题:
(1)写出B的名称:
(2)在上图D→C的过程中,Cu在反应中
(3)在D的稀溶液中滴入Na2CO3溶液,其反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】某化学小组按如图所示实验流程比较浓硝酸和稀硝酸的氧化性强弱,其中B为一种紫红色金属,C为红棕色气体。

请回答下列问题:
(1)A与B反应的离子方程式是_______ ;A与B反应迅速,实验中需要采取措施控制气体放出的快慢及多少,则装置Ⅰ可以选择的装置为_______ (填序号)。

(2)实验时在装置Ⅰ中加入B后,在加入A之前需向整套装置中通入足量的 气体,该操作的目的是
气体,该操作的目的是_______ 。
(3)装置Ⅱ中发生的反应,其氧化剂与还原剂的物质的量之比为_______ 。
(4)通过实验可得出:浓硝酸的氧化性比稀硝酸_______ (填“强”或“弱”),判断的依据是_______ 。
(5)装置Ⅴ的作用是_______ 。

请回答下列问题:
(1)A与B反应的离子方程式是

(2)实验时在装置Ⅰ中加入B后,在加入A之前需向整套装置中通入足量的
 气体,该操作的目的是
气体,该操作的目的是(3)装置Ⅱ中发生的反应,其氧化剂与还原剂的物质的量之比为
(4)通过实验可得出:浓硝酸的氧化性比稀硝酸
(5)装置Ⅴ的作用是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】如图是元素周期表的一部分,表中所列字母分别代表一种元素

回答下列问题:
(1)h元素的名称是______ ,九种元素中金属性最强的是_______ (填元素符号)。
(2)f的最高价氧化物对应的水化物的化学式____ (填化学式)。
(3)b、c、d、e的原子半径依次________ (填增大或减小)。
(4)e、h元素的氢化物中,热稳定性大的是__ (填氢化物的化学式)。
(5)化合物f2d2与化合物 a2d 反应的离子方程式__________ 。
(6)工业上冶炼g元素的单质的化学方程式__________ 。

回答下列问题:
(1)h元素的名称是
(2)f的最高价氧化物对应的水化物的化学式
(3)b、c、d、e的原子半径依次
(4)e、h元素的氢化物中,热稳定性大的是
(5)化合物f2d2与化合物 a2d 反应的离子方程式
(6)工业上冶炼g元素的单质的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】有A、B、C、D、E五种原子序数依次增大的短周期主族元素,A是短周期主族元素中原子半径最大的元素,B是地壳中含量最多的金属元素,C元素原子的最外层电子数比次外层电子数少4,D元素原子的次外层电子数比最外层电子数多3,A、B、E三种原子的最外层电子数之和为11,请回答下列问题:
(1)写出A、B、C三种元素的元素符号:A_____ 、B________ 、C________ 。
(2) C的原子结构示意图为______ 。
(3) D的最简单氢化物的化学式为____ ,E的最高价氧化物对应的水化物的化学式为_____ 。
(4) A与氧元素形成的化合物的电子式为________ 。
(5) D和E的最简单氢化物中稳定性强的是_______ (填化学式)。.
(1)写出A、B、C三种元素的元素符号:A
(2) C的原子结构示意图为
(3) D的最简单氢化物的化学式为
(4) A与氧元素形成的化合物的电子式为
(5) D和E的最简单氢化物中稳定性强的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
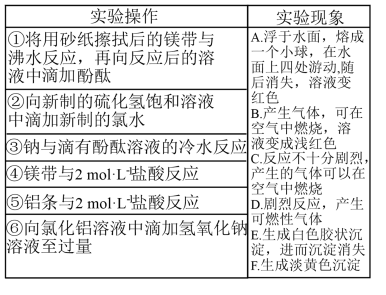
【推荐3】某化学兴趣小组的同学学习了同周期元素性质的递变规律后,设计了一套实验方案进行实验探究,并记录了有关实验现象,如下表。
请你帮助该同学整理并完成实验报告。
(1)实验目的:__________________ 。
(2)实验仪器:①________ ;②________ ;③________ ;④试管夹;⑤镊子;⑥小刀;⑦玻璃片;⑧砂纸;⑨胶头滴管等。
(3)实验药品:钠、镁带、铝条、2 mol·L-1盐酸、新制的氯水、硫化氢饱和溶液、氯化铝溶液、氢氧化钠溶液等。
(4)请你写出上述的实验操作对应的现象(用A~F表示):
①________ ;②________ ;③________ ;④________ ;⑤________ ;⑥________ 。
(5)写出实验操作②、⑥中有关反应的离子方程式:
实验②________________________ ,实验⑥______________________ 。
(6)实验结论:__________________________ 。

请你帮助该同学整理并完成实验报告。
(1)实验目的:
(2)实验仪器:①
(3)实验药品:钠、镁带、铝条、2 mol·L-1盐酸、新制的氯水、硫化氢饱和溶液、氯化铝溶液、氢氧化钠溶液等。
(4)请你写出上述的实验操作对应的现象(用A~F表示):
①
(5)写出实验操作②、⑥中有关反应的离子方程式:
实验②
(6)实验结论:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】元素周期表揭示了化学元素间的内在联系。节日燃放的五彩缤纷的烟花,就是下面周期表中一些金属元素的化合物所呈现的各种艳丽色彩。
请用相关的化学用语回答下列问题。
(1)烟花中的a、b、c三种金属元素原子的核外电子排布共同特点是_______ ,金属性最强的是_______ 。
(2)上述十种元素中,化学性质最不活泼的是_______ 。
(3)元素b、c、d按原子半径由大到小的顺序排列为_______ 。
(4)元素b的氧化物的水溶液与元素e的单质反应的离子方程式是_______ 。
(5)元素g和元素j的最高价氧化物对应的水化物的酸性强弱比较_______ 。
(6)元素c、h形成化合物的化学式是_______ ,该化合物中存在的化学键是_______ 。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | a | f | ||||||
| 3 | b | d | e | j | g | i | ||
| 4 | c | h | ||||||
(1)烟花中的a、b、c三种金属元素原子的核外电子排布共同特点是
(2)上述十种元素中,化学性质最不活泼的是
(3)元素b、c、d按原子半径由大到小的顺序排列为
(4)元素b的氧化物的水溶液与元素e的单质反应的离子方程式是
(5)元素g和元素j的最高价氧化物对应的水化物的酸性强弱比较
(6)元素c、h形成化合物的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下表所列是七种短周期元素的原子半径及主要化合价(已知铍的原子半径为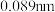 )。
)。
(1)A是___ 元素,C元素在元素周期表中的位置是________ 。
(2)B的原子结构示意图为_______ 。
(3)B、C最高价氧化物对应水化物的碱性强弱顺序为_______ (用化学式表示)。
(4)D、E、F、G的离子半径由大到小的顺序为________ (用离子符号表示)。
(5)C的最高价氧化物与氢氧化钠溶液反应的离子方程式为______ 。
(6)碲(52Te)的某种化合物是常用的VCR光盘记录材料之一,可在激光照射下发生化学或物理性能的改变而记录、储存信号。根据碲元素在周期表中的位置,推测碲元素及其化合物可能具有的性质有______ (填序号)。
A.单质碲在常温下是固体 B.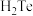 比
比 稳定
稳定
C.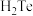 不如
不如 稳定 D.
稳定 D.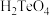 的酸性比
的酸性比 的弱
的弱
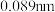 )。
)。| 元素代号 | A | B | C | D | E | F | G |
原子半径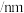 | 0.037 | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 | 0.075 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | -1 | -2 | +5、-3 |
(2)B的原子结构示意图为
(3)B、C最高价氧化物对应水化物的碱性强弱顺序为
(4)D、E、F、G的离子半径由大到小的顺序为
(5)C的最高价氧化物与氢氧化钠溶液反应的离子方程式为
(6)碲(52Te)的某种化合物是常用的VCR光盘记录材料之一,可在激光照射下发生化学或物理性能的改变而记录、储存信号。根据碲元素在周期表中的位置,推测碲元素及其化合物可能具有的性质有
A.单质碲在常温下是固体 B.
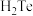 比
比 稳定
稳定C.
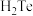 不如
不如 稳定 D.
稳定 D.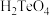 的酸性比
的酸性比 的弱
的弱
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】表中列出了第三周期几种元素的部分性质:
请按要求回答下列问题:
(1)表中元素原子半径最大的是(写元素符号)___________ 。
(2)a、b、c三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)___________ 。
(3)d、e最高价氧化物对应水化物相互反应的离子方程式为___________ 。
(4)某化学兴趣小组为探究元素性质的递变规律,设计了以下系列实验。
①甲同学为探究同主族元素金属性的递变规律,取绿豆粒大小的钠、钾分别放入到盛有水的烧杯(滴有几滴酚酞溶液)中,通过观察现象得出的结论是___________ 。
②乙同学利用现有药品: 溶液、
溶液、 固体、浓盐酸、
固体、浓盐酸、 ,设计如图装置探究第三周期部分元素非金属性的递变规律。M中所装药品为
,设计如图装置探究第三周期部分元素非金属性的递变规律。M中所装药品为___________ ,装置N中的实验现象为有淡黄色沉淀生成,离子方程式为___________ ,所得结论为___________ 。

| 元素编号 | a | b | c | d | e |
| 电负性 | 3.0 | 2.5 | 2.1 | 1.5 | 0.9 |
| 主要化合价 | -1,+7 | -2,+6 | -3,+5 | +3 | +1 |
(1)表中元素原子半径最大的是(写元素符号)
(2)a、b、c三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)
(3)d、e最高价氧化物对应水化物相互反应的离子方程式为
(4)某化学兴趣小组为探究元素性质的递变规律,设计了以下系列实验。
①甲同学为探究同主族元素金属性的递变规律,取绿豆粒大小的钠、钾分别放入到盛有水的烧杯(滴有几滴酚酞溶液)中,通过观察现象得出的结论是
②乙同学利用现有药品:
 溶液、
溶液、 固体、浓盐酸、
固体、浓盐酸、 ,设计如图装置探究第三周期部分元素非金属性的递变规律。M中所装药品为
,设计如图装置探究第三周期部分元素非金属性的递变规律。M中所装药品为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表为长式周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)写出元素⑩的一价离子的核外电子排布式:_______ 该元素属于_______ 区元素。
(2)在标号的主族元素中,电负性最大的是_______ (填元素符号,下同),第一电离能最小的是_______ 。
(3)元素④⑥⑦的气态氢化物热稳定性由强到弱的顺序为:_______ (填化学式)。
(4)已知周期表中存在对角相似规则,如②与⑤在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑨的氢氧化物反应的化学方程式_______ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑨ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
| ⑩ |
(1)写出元素⑩的一价离子的核外电子排布式:
(2)在标号的主族元素中,电负性最大的是
(3)元素④⑥⑦的气态氢化物热稳定性由强到弱的顺序为:
(4)已知周期表中存在对角相似规则,如②与⑤在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑨的氢氧化物反应的化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】下图是元素周期表的一部分,图中所列字母分别代表一种化学元素。回答下列问题:
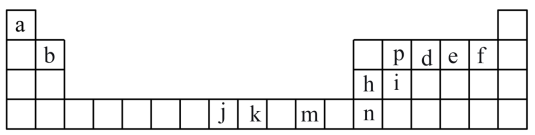
(1)下列正确的是___________。
(2)已知高温下化合物 比化合物
比化合物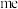 更稳定,试从
更稳定,试从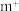 离子的核外电子排布的角度解释原因
离子的核外电子排布的角度解释原因___________ 。
(3)根据对角线规则,b与h的化学性质相似,请写出b的最高价氧化物对应的水化物与 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
(4)下图为第ⅤA族、ⅥA、ⅦA族元素简单氢化物沸点随周期数的递变趋势图。

分析上图回答下列问题:
①推测ⅣA族 与
与 的沸点大小为
的沸点大小为
___________  (填“>”或“<”)。
(填“>”或“<”)。
②接近水的沸点的水蒸气的相对分子质量测定值比按化学式 计算出的相对分子质量大一些,原因为
计算出的相对分子质量大一些,原因为___________ 。
③ 常用于制备半导体材料,
常用于制备半导体材料, 与足量的
与足量的 加热可反应得到
加热可反应得到 ,通过
,通过___________ 的实验分析方法可测出 的键长键角信息。
的键长键角信息。

(1)下列正确的是___________。
A.原子半径 | B.第一电离能 |
C.电负性 | D.最高价氧化物的水化物的酸性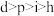 |
 比化合物
比化合物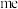 更稳定,试从
更稳定,试从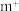 离子的核外电子排布的角度解释原因
离子的核外电子排布的角度解释原因(3)根据对角线规则,b与h的化学性质相似,请写出b的最高价氧化物对应的水化物与
 溶液反应的离子方程式
溶液反应的离子方程式(4)下图为第ⅤA族、ⅥA、ⅦA族元素简单氢化物沸点随周期数的递变趋势图。

分析上图回答下列问题:
①推测ⅣA族
 与
与 的沸点大小为
的沸点大小为
 (填“>”或“<”)。
(填“>”或“<”)。②接近水的沸点的水蒸气的相对分子质量测定值比按化学式
 计算出的相对分子质量大一些,原因为
计算出的相对分子质量大一些,原因为③
 常用于制备半导体材料,
常用于制备半导体材料, 与足量的
与足量的 加热可反应得到
加热可反应得到 ,通过
,通过 的键长键角信息。
的键长键角信息。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)②元素原子的电子式是:_______ 。
(2)硅元素在周期表中的位置是:第_______ 周期_______ 族。
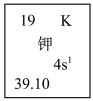
(3)如图所示钾元素的部分信息,“30.97”数值表示_______ 。______ (填元素符号)。③和⑧两种元素形成的气态氢化物稳定性强的是_______ (填化学式)。写出④的最高价氧化物对应水合物和⑧的最高价氧化物对应水合物相互反应的化学方程式_______ 。
(5)Cl元素比S元素的非金属性强,请从原子结构角度解释原因_______ 。能证明这一事实的化学反应为_______ (写一个化学方程式)。
(6)能证明O元素的非金属性强于S元素的依据是_______ 。
A.热稳定性:H2O>H2S B.SO2中O显负价 C.沸点:S>O2
(7)氧元素有三种核素:16O、17O、18O,对这三种核素的描述错误的是_______ 。
(8)元素周期表可以用于寻找新元素、发现物质的新用途。下列说法正确的是_______ 。
(9)元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”。下列叙述错误的是_______ 。
族 周期 | ⅠA | 0 | |||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ① | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)②元素原子的电子式是:
(2)硅元素在周期表中的位置是:第
(3)如图所示钾元素的部分信息,“30.97”数值表示
(5)Cl元素比S元素的非金属性强,请从原子结构角度解释原因
(6)能证明O元素的非金属性强于S元素的依据是
A.热稳定性:H2O>H2S B.SO2中O显负价 C.沸点:S>O2
(7)氧元素有三种核素:16O、17O、18O,对这三种核素的描述错误的是
| A.质子数相同 | B.质量相同 |
| C.化学性质相同 | D.位置相同(周期表中) |
(8)元素周期表可以用于寻找新元素、发现物质的新用途。下列说法正确的是
| A.在周期表中金属与非金属的分界处可以找到催化剂材料 |
| B.对氟、氯、硫、磷、砷等元素的研究,有助于制造出新品种的农药 |
| C.在过渡元素中可寻找制造半导体的元素 |
| D.可在第IA、IIA族元素中寻找制造耐高温、耐腐蚀合金的元素 |
(9)元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”。下列叙述错误的是
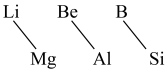
| A.Li在空气中燃烧生成Li2O、Li3N | B.硼酸是弱酸 |
| C.Be不与水反应 | D.Be(OH)2是两性氢氧化物 |
您最近一年使用:0次



