喷泉是一种常见的现象,其产生的原理是存在压强差。

试回答下列问题:
(1)实验室制取氨气的化学方程式为________ 。
①用图A装置进行喷泉实验,上部烧瓶已充满干燥的氨气,引发喷泉的操作是_______ 。
②利用图B装置引发喷泉的操作是___________ 。
(2)利用图C装置,在锥形瓶中分别加入足量的下列物质,反应后可能产生喷泉的有______ 。
A. 与稀盐酸 B.
与稀盐酸 B. 与稀硫酸
与稀硫酸
C. 与稀硝酸 D.
与稀硝酸 D. 溶液与
溶液与 溶液
溶液
(3)在图D装置的锥形瓶中加入乙醇,瓶外放一水槽,水槽中加入冷水后,再加入足量的下列物质,结果也形成了喷泉,水槽中加入的物质可能是_____ 。
A 浓硫酸 B 食盐 C 硝酸钾 D 硫酸铜
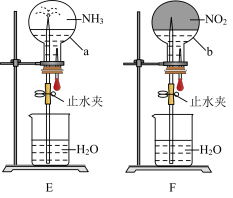
(4)同温同压下,两个等体积的干燥圆底烧瓶中分别充满 和
和 ,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有
,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有 体积的液体,则两烧瓶内溶质的物质的量浓度的关系是
体积的液体,则两烧瓶内溶质的物质的量浓度的关系是_______ 。
A.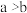 B.
B. C.
C. D.不能确定
D.不能确定

试回答下列问题:
(1)实验室制取氨气的化学方程式为
①用图A装置进行喷泉实验,上部烧瓶已充满干燥的氨气,引发喷泉的操作是
②利用图B装置引发喷泉的操作是
(2)利用图C装置,在锥形瓶中分别加入足量的下列物质,反应后可能产生喷泉的有
A.
 与稀盐酸 B.
与稀盐酸 B. 与稀硫酸
与稀硫酸C.
 与稀硝酸 D.
与稀硝酸 D. 溶液与
溶液与 溶液
溶液(3)在图D装置的锥形瓶中加入乙醇,瓶外放一水槽,水槽中加入冷水后,再加入足量的下列物质,结果也形成了喷泉,水槽中加入的物质可能是
A 浓硫酸 B 食盐 C 硝酸钾 D 硫酸铜
(4)同温同压下,两个等体积的干燥圆底烧瓶中分别充满
 和
和 ,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有
,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有 体积的液体,则两烧瓶内溶质的物质的量浓度的关系是
体积的液体,则两烧瓶内溶质的物质的量浓度的关系是
A.
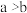 B.
B. C.
C. D.不能确定
D.不能确定
更新时间:2020-09-16 14:46:40
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某校化学兴趣小组,在实验室里模拟用N2和H2合成氨,反应的化学方程式为N2+3H2 2NH3。现用未经干燥的N2和H2按体积比V(N2)∶V(H2)=1∶3充分混合后,按如图所示的装置进行有关实验。
2NH3。现用未经干燥的N2和H2按体积比V(N2)∶V(H2)=1∶3充分混合后,按如图所示的装置进行有关实验。
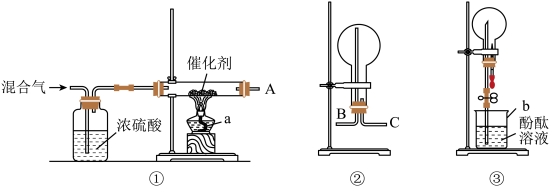
请回答下列问题:
(1)装置①中浓硫酸的作用是________ 。
(2)若用装置②收集反应生成的气体,A应连接装置中的________ (填“B”或“C”);
(3)收集满气体后,再用装置③进行实验,当烧瓶中的液面逐渐上升,溶液呈________ 色。
(4)实验结束时,溶液几乎充满了烧瓶,则溶液的物质的量浓度为________ mol/L(气体为标准状况下的体积)
 2NH3。现用未经干燥的N2和H2按体积比V(N2)∶V(H2)=1∶3充分混合后,按如图所示的装置进行有关实验。
2NH3。现用未经干燥的N2和H2按体积比V(N2)∶V(H2)=1∶3充分混合后,按如图所示的装置进行有关实验。 
请回答下列问题:
(1)装置①中浓硫酸的作用是
(2)若用装置②收集反应生成的气体,A应连接装置中的
(3)收集满气体后,再用装置③进行实验,当烧瓶中的液面逐渐上升,溶液呈
(4)实验结束时,溶液几乎充满了烧瓶,则溶液的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学小组利用装置A制取 并探究
并探究 的相关性质(部分仪器已略去)。
的相关性质(部分仪器已略去)。
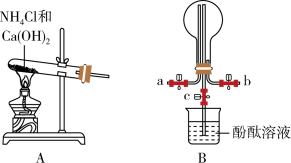
(1)B中圆底烧瓶收集氨气时,氨气的进气口________ (填“a”或“b”)。
(2)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是________ ;引发喷泉的操作应是________ 。
(3)查阅资料:氮的氧化物( )是大气污染物之一,工业上在一定温度和催化剂条件下用
)是大气污染物之一,工业上在一定温度和催化剂条件下用 将
将 还原生成无污染的物质。该小组将收集到的
还原生成无污染的物质。该小组将收集到的 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入
充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入 (两端用夹子
(两端用夹子 、
、 夹好)。
夹好)。
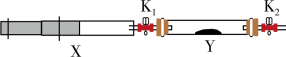
在一定温度下按图示装置进行实验,打开 ,推动注射器活塞,使X中的气体缓慢通入Y管中,反应的化学方程式为
,推动注射器活塞,使X中的气体缓慢通入Y管中,反应的化学方程式为________ 。
Ⅱ.下图是探究铜与浓硫酸反应生成硫酸铜的实验装置图:

(4)写出装置B中发生反应的离子方程式________ ,写出图中虚线框内装置的作用________ 。
Ⅲ. 如图所示, 分子呈正四面体结构。
分子呈正四面体结构。
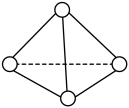
(5)已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则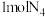 气体转化为
气体转化为 时要
时要________ (填“吸收”或“放出”)热量________ kJ。
 并探究
并探究 的相关性质(部分仪器已略去)。
的相关性质(部分仪器已略去)。
(1)B中圆底烧瓶收集氨气时,氨气的进气口
(2)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是
(3)查阅资料:氮的氧化物(
 )是大气污染物之一,工业上在一定温度和催化剂条件下用
)是大气污染物之一,工业上在一定温度和催化剂条件下用 将
将 还原生成无污染的物质。该小组将收集到的
还原生成无污染的物质。该小组将收集到的 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入
充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入 (两端用夹子
(两端用夹子 、
、 夹好)。
夹好)。
在一定温度下按图示装置进行实验,打开
 ,推动注射器活塞,使X中的气体缓慢通入Y管中,反应的化学方程式为
,推动注射器活塞,使X中的气体缓慢通入Y管中,反应的化学方程式为Ⅱ.下图是探究铜与浓硫酸反应生成硫酸铜的实验装置图:

(4)写出装置B中发生反应的离子方程式
Ⅲ. 如图所示,
 分子呈正四面体结构。
分子呈正四面体结构。
(5)已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则
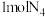 气体转化为
气体转化为 时要
时要
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】大气压强对许多物理实验和化学实验有着重要影响,制取氨气并完成喷泉实验。

(1)检验圆底烧瓶中氨气收集满的方法是_________________________________ 。
(2)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是________ ,该实验的原理是________________________________________ 。
(3)如果只提供如图2的装置,请说明引发喷泉的方法:______________________ 。

(1)检验圆底烧瓶中氨气收集满的方法是
(2)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是
(3)如果只提供如图2的装置,请说明引发喷泉的方法:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】下图为实验室制取氨气,二氧化硫气及有关性质实验的组合装置。

(1)如果A、E是气体制取装置,则按照题目要求,A中制取气体的化学反应方程式为____ ;
(2)B仪器称为_______ ,在此实验中B应加入_______ (写名称);
(3)先加热A装置,使产生气体通入烧瓶F中,此时弹簧夹a、b打开、c关闭。当F中充满A中气体后,A停止制气,关闭a,打开弹簧夹c,使E中气体通入F中;
①如何测知F中已充满大量A中气体:________ ;
②D的作用是干燥气体,D中盛的是_______ (写名称);
③E中气体进入F后,触发F中气体发生反应的操作是将烧瓶导管与塑料瓶C连接,并完成喷泉实验,F中气体发生反应的化学方程式为____ ;
(4)A、E中产生的气体都是有污染性的,吸收A尾气的试剂是____ ,吸收E尾气的离子方程式为___ 。

(1)如果A、E是气体制取装置,则按照题目要求,A中制取气体的化学反应方程式为
(2)B仪器称为
(3)先加热A装置,使产生气体通入烧瓶F中,此时弹簧夹a、b打开、c关闭。当F中充满A中气体后,A停止制气,关闭a,打开弹簧夹c,使E中气体通入F中;
①如何测知F中已充满大量A中气体:
②D的作用是干燥气体,D中盛的是
③E中气体进入F后,触发F中气体发生反应的操作是将烧瓶导管与塑料瓶C连接,并完成喷泉实验,F中气体发生反应的化学方程式为
(4)A、E中产生的气体都是有污染性的,吸收A尾气的试剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】侯德榜是我国近代化学工业的奠基人之一,他将氨碱法制取碳酸钠与合成氨联合起来,形成联合制碱法他称侯氏制碱法),该法缩短了生产流程,提高了食盐利用率。侯氏制碱法过程中首先得到的是NaHCO3,再加热分解得到碳酸钠。某化学兴趣小组在实验室模拟侯氏制碱法的装置如图所示(夹持装置已略去)。

已知:氨气极易溶于水,氨气溶于水后所得溶液呈碱性;二氧化碳在碱性溶液中的溶解度大于在饱和食盐水中的溶解度。根据所学知识回答下列问题:
(1)用于制取氨气的装置为_______ (填“甲”或“丁”)。
(2)装置乙中饱和NaHCO3溶液的作用为_______ 。
(3)装置丙中发生反应的离子方程式为_______ 。
(4)为了提高食盐的利用率应先打开_______ (填“止水夹1”或“止水夹2”)。
(5)分析装置甲中的稀盐酸能否用稀硫酸代替,并说明原因:_______ 。
(6)取一定质量制得的NaHCO3固体置于坩埚中加热分解得到固体X。为了检验固体X中是否含有NaHCO3,该组同学称取一定质量的固体X配成溶液,然后向其中滴加某浓度的稀盐酸。产生CO2的体积与加入稀盐酸的体积关系如图所示。

①同学甲通过观察图像,得出固体X中含有NaHCO3的结论,你认为该结论_______ (填“正确”或“错误”),说明理由_______ 。
②固体X中NaHCO3与Na2CO3的物质的量之比n(NaHCO3) : n(Na2CO3)=_______ 。

已知:氨气极易溶于水,氨气溶于水后所得溶液呈碱性;二氧化碳在碱性溶液中的溶解度大于在饱和食盐水中的溶解度。根据所学知识回答下列问题:
(1)用于制取氨气的装置为
(2)装置乙中饱和NaHCO3溶液的作用为
(3)装置丙中发生反应的离子方程式为
(4)为了提高食盐的利用率应先打开
(5)分析装置甲中的稀盐酸能否用稀硫酸代替,并说明原因:
(6)取一定质量制得的NaHCO3固体置于坩埚中加热分解得到固体X。为了检验固体X中是否含有NaHCO3,该组同学称取一定质量的固体X配成溶液,然后向其中滴加某浓度的稀盐酸。产生CO2的体积与加入稀盐酸的体积关系如图所示。

①同学甲通过观察图像,得出固体X中含有NaHCO3的结论,你认为该结论
②固体X中NaHCO3与Na2CO3的物质的量之比n(NaHCO3) : n(Na2CO3)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】设计了下图所示的实验装置模拟工业生产制备少量硝酸。

(1)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃以上,由此可知该反应是反应___________ (填“吸热”或“放热”),反应的化学方程式是___________ 。
(2)控制氨气和氧气的比例是制备硝酸的关键。
①当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。红棕色气体的化学式是___________ ,白烟的化学式是___________ 。
②欲使氨气尽可能完全转化为硝酸,理论上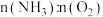 的最佳比例为
的最佳比例为___________ 。
(3)下图中制取氨气的装置和选用的试剂,合理的是(填字母)_______。

(4)实验室制备氨气的化学方程式是_______ 。
(5)下图为铵盐的受热分解装置,被加热的铂丝处发生反应的化学方程式为_______ 。

(6)B中出现的现象为_______ 。
(7)如图,将上图烧杯C中反应生成的4mol/L稀酸溶液与2mol/L稀硫酸共10mL与2.56gCu反应,实验完毕后,在标准状况下试管中收集到的气体的体积(不考虑N2O4的产生)_______ L。


(1)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃以上,由此可知该反应是反应
(2)控制氨气和氧气的比例是制备硝酸的关键。
①当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。红棕色气体的化学式是
②欲使氨气尽可能完全转化为硝酸,理论上
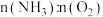 的最佳比例为
的最佳比例为(3)下图中制取氨气的装置和选用的试剂,合理的是(填字母)_______。

| A.①② | B.②③ | C.②④ | D.①③ |
(4)实验室制备氨气的化学方程式是
(5)下图为铵盐的受热分解装置,被加热的铂丝处发生反应的化学方程式为

(6)B中出现的现象为
(7)如图,将上图烧杯C中反应生成的4mol/L稀酸溶液与2mol/L稀硫酸共10mL与2.56gCu反应,实验完毕后,在标准状况下试管中收集到的气体的体积(不考虑N2O4的产生)

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C为三种单质(其中A为固体,B、C为气体),D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色,B、C反应的产物易溶于水得到无色溶液E.它们之间的转化关系如下图:

填写下列空白:
(1)物质A是________ ,B是________ ,C是________ .
(2)F中加入NaOH溶液,并在空气中放置的化学方程式是__________________________ ,______________________________________________ 。

填写下列空白:
(1)物质A是
(2)F中加入NaOH溶液,并在空气中放置的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知有以下物质的相互转化:

试回答:
(1)B的化学式为_____ ;D的化学式为_____ 。
(2)写出由E转变成F的化学方程式:______ 。
(3)常用____ (填试剂名称)检验G中的阳离子,其现象为______ 。
(4)向G溶液中加入A的有关反应的离子方程式为________ 。

试回答:
(1)B的化学式为
(2)写出由E转变成F的化学方程式:
(3)常用
(4)向G溶液中加入A的有关反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】废旧金属可回收利用,某化学兴趣小组用合金废料(含Fe、Cu和Al)制取FeSO4溶液和回收金属铜,实验流程如图所示(部分生成物已略去)。已知:2Al+2NaOH+2H2O=2NaAlO2+3H2↑。

(1)单质铁的金属活动性比铜________ (填“强”或“弱”)。
(2)操作Ⅰ的名称___________ ,操作Ⅱ用到的玻璃仪器有烧杯、玻璃棒和___________ (填仪器名称)。
(3)若取FeSO4溶液适量,滴入BaCl2溶液,发生反应的化学方程式为___________________________ ,该反应属于基本反应类型中的________ 反应。
(4)步骤B的化学方程式为_________________________________________ 。
(5)铝制品在空气中耐腐蚀的原因是_____________________________________________________ 。

(1)单质铁的金属活动性比铜
(2)操作Ⅰ的名称
(3)若取FeSO4溶液适量,滴入BaCl2溶液,发生反应的化学方程式为
(4)步骤B的化学方程式为
(5)铝制品在空气中耐腐蚀的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
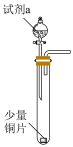
【推荐1】铜和硝酸的反应实验是体现硝酸重要性质的实验,某教师设计了如图装置进行铜和稀硝酸的反应实验,步骤如下:
步骤ⅰ.将弹簧状细铜丝放入注射器 底部并固定,注射器
底部并固定,注射器 吸入少量蒸馏水后将活塞推至最低处;注射器
吸入少量蒸馏水后将活塞推至最低处;注射器 吸取
吸取 溶液(过量),注射器
溶液(过量),注射器 于烧杯中吸取
于烧杯中吸取 稀硝酸,注射器
稀硝酸,注射器 吸取
吸取 (过量)。
(过量)。
步骤ⅱ.按图连接好装置,打开止水夹 、
、 ,关闭
,关闭 、
、 ,将注射器
,将注射器 中的稀硝酸注入
中的稀硝酸注入 中。
中。
步骤ⅲ.关闭止水夹 ,打开止水夹
,打开止水夹 ,抽动注射器
,抽动注射器 的活塞,将注射器
的活塞,将注射器 中生成的
中生成的 气体全部抽入
气体全部抽入 中。
中。
步骤ⅳ.关闭止水夹 ,打开止水夹
,打开止水夹 ,将注射器
,将注射器 中气体全部抽入
中气体全部抽入 中。
中。 、
、 的容积为
的容积为 ,注射器
,注射器 、
、 的容积为
的容积为 ;②止水夹
;②止水夹 、
、 、
、 、
、 连在四通管上;③该实验中,铜与稀硝酸反应生成的气体只有
连在四通管上;③该实验中,铜与稀硝酸反应生成的气体只有 。
。
请回答下列问题:
(1)步骤ⅰ中注射器 吸入少量蒸馏水后将活塞推至最低处的目的是
吸入少量蒸馏水后将活塞推至最低处的目的是______ ;步骤ⅱ注射器 中的稀硝酸注入
中的稀硝酸注入 中时发生反应的化学方程式为
中时发生反应的化学方程式为______ ,观察到的现象为______ ,该反应中稀硝酸体现了______ (填化学性质)。
(2)步骤ⅲ将注射器 中生成的气体全部抽入
中生成的气体全部抽入 中,注射器
中,注射器 中能观察到的现象为
中能观察到的现象为______ ;该过程中, 发生了
发生了______ (填“氧化”或“还原”)反应。
(3)步骤ⅳ将注射器 中气体全部抽入
中气体全部抽入 中,
中, 和
和 的混合气体与
的混合气体与 溶液反应生成的盐只有
溶液反应生成的盐只有 ,该反应的离子方程式为
,该反应的离子方程式为______ ,该反应中氧化剂和氧化产物的物质的量之比为______ 。
(4)若反应过程中有 铜丝参与反应,要使注射器
铜丝参与反应,要使注射器 中产生的
中产生的 最终在注射器
最终在注射器 中全部转化为
中全部转化为 ,需要消耗
,需要消耗______ 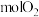 。
。
步骤ⅰ.将弹簧状细铜丝放入注射器
 底部并固定,注射器
底部并固定,注射器 吸入少量蒸馏水后将活塞推至最低处;注射器
吸入少量蒸馏水后将活塞推至最低处;注射器 吸取
吸取 溶液(过量),注射器
溶液(过量),注射器 于烧杯中吸取
于烧杯中吸取 稀硝酸,注射器
稀硝酸,注射器 吸取
吸取 (过量)。
(过量)。步骤ⅱ.按图连接好装置,打开止水夹
 、
、 ,关闭
,关闭 、
、 ,将注射器
,将注射器 中的稀硝酸注入
中的稀硝酸注入 中。
中。步骤ⅲ.关闭止水夹
 ,打开止水夹
,打开止水夹 ,抽动注射器
,抽动注射器 的活塞,将注射器
的活塞,将注射器 中生成的
中生成的 气体全部抽入
气体全部抽入 中。
中。步骤ⅳ.关闭止水夹
 ,打开止水夹
,打开止水夹 ,将注射器
,将注射器 中气体全部抽入
中气体全部抽入 中。
中。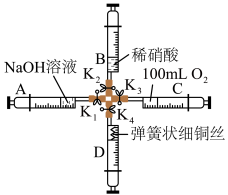
 、
、 的容积为
的容积为 ,注射器
,注射器 、
、 的容积为
的容积为 ;②止水夹
;②止水夹 、
、 、
、 、
、 连在四通管上;③该实验中,铜与稀硝酸反应生成的气体只有
连在四通管上;③该实验中,铜与稀硝酸反应生成的气体只有 。
。请回答下列问题:
(1)步骤ⅰ中注射器
 吸入少量蒸馏水后将活塞推至最低处的目的是
吸入少量蒸馏水后将活塞推至最低处的目的是 中的稀硝酸注入
中的稀硝酸注入 中时发生反应的化学方程式为
中时发生反应的化学方程式为(2)步骤ⅲ将注射器
 中生成的气体全部抽入
中生成的气体全部抽入 中,注射器
中,注射器 中能观察到的现象为
中能观察到的现象为 发生了
发生了(3)步骤ⅳ将注射器
 中气体全部抽入
中气体全部抽入 中,
中, 和
和 的混合气体与
的混合气体与 溶液反应生成的盐只有
溶液反应生成的盐只有 ,该反应的离子方程式为
,该反应的离子方程式为(4)若反应过程中有
 铜丝参与反应,要使注射器
铜丝参与反应,要使注射器 中产生的
中产生的 最终在注射器
最终在注射器 中全部转化为
中全部转化为 ,需要消耗
,需要消耗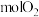 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】硝酸的化学性质
(1)酸性:在水中的电离方程式为_______ 。
(2)不稳定性:
①浓硝酸见光或受热会发生分解,化学方程式为_______ 。
②实验室中浓硝酸显黄色是浓硝酸分解生成的_______ 又溶于硝酸所致。
(3)强氧化性:
①实验探究:
②强氧化性的表现:

写出下列有关反应的化学方程式:
a.与金属反应:
稀硝酸与铜反应:_______ 。
浓硝酸与铜反应:_______ 。
b.与非金属反应:
浓硝酸与红热的碳(被氧化为CO2)的反应为_______ 。
(1)酸性:在水中的电离方程式为
(2)不稳定性:
①浓硝酸见光或受热会发生分解,化学方程式为
②实验室中浓硝酸显黄色是浓硝酸分解生成的
(3)强氧化性:
①实验探究:
| 实验装置 |  | |
| 稀硝酸 | 浓硝酸 | |
| 实验现象 | 反应缓慢,有少量气泡产生, | 反应剧烈,有 |
| 实验结论 | 铜与稀硝酸常温下缓慢反应生成 | 铜与浓硝酸常温下剧烈反应生成 |

写出下列有关反应的化学方程式:
a.与金属反应:
稀硝酸与铜反应:
浓硝酸与铜反应:
b.与非金属反应:
浓硝酸与红热的碳(被氧化为CO2)的反应为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】实验小组研究铜与过量硝酸的反应,实验如下(加持装置和尾气处理装置略)。
(1)氮在元素周期表中的位置为___________ 。
(2)实验Ⅰ、Ⅱ中的红棕色气体均是NO2.实验Ⅰ产生NO2的化学方程式是___________ 。
(3)对实验Ⅰ产生NO2,实验Ⅱ产生NO的原因提出解释。
①硝酸浓度越稀,溶液中单位体积内的NO 数目越少。被还原时,每个NO
数目越少。被还原时,每个NO 从铜片处获得较多电子的机会越
从铜片处获得较多电子的机会越___________ (填“大”或“小”),因此越易被还原为较低价态的含氮物质。
②浓硝酸具有较强的___________ 性,可将NO转化为NO2。
(4)有同学针对I中溶液呈绿色的原因,提出假设:
假设1:Cu2+的浓度较大所致;假设2:溶解了生成的NO2。
探究如下:取I中绿色溶液,分为两等份。
①取一份于如图所示装置中,向上拉动活塞a,___________ (填现象),证实I中溶解了NO2。___________ (填化学试剂),溶液变为蓝色。证实假设1不成立,假设2成立。
(5)硝酸与金属反应会产生氮氧化物。
①下列环境问题与氮的氧化物排放无关的是___________ 。
A.酸雨B.光化学烟雾C温室效应 D.白色污染
②在含有agHNO3的稀硝酸中,加入bg铁粉充分反应,铁全部溶解并生成NO,有0.25agHNO3被还原,则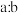 可能为
可能为___________ 。
A.2:1 B.3:1 C.4:1 D.9:2
③为避免氮氧化物污染环境,人们开发了溶液吸收法。比如用碱性的Na2CO3溶液吸收NO2,请写出相关的化学反应方程式:___________ 。
| 装置 | 编号 | 试剂a | 现象 |
| Ⅰ | 4mL浓硝酸(过量) | 铜片完全溶解,溶液变绿,出现大量红棕色气体 |
| Ⅱ | 4mL稀硝酸(过量) | 铜片完全溶解,溶液变蓝,液面上方气体呈浅红棕色 |
(1)氮在元素周期表中的位置为
(2)实验Ⅰ、Ⅱ中的红棕色气体均是NO2.实验Ⅰ产生NO2的化学方程式是
(3)对实验Ⅰ产生NO2,实验Ⅱ产生NO的原因提出解释。
①硝酸浓度越稀,溶液中单位体积内的NO
 数目越少。被还原时,每个NO
数目越少。被还原时,每个NO 从铜片处获得较多电子的机会越
从铜片处获得较多电子的机会越②浓硝酸具有较强的
(4)有同学针对I中溶液呈绿色的原因,提出假设:
假设1:Cu2+的浓度较大所致;假设2:溶解了生成的NO2。
探究如下:取I中绿色溶液,分为两等份。
①取一份于如图所示装置中,向上拉动活塞a,

(5)硝酸与金属反应会产生氮氧化物。
①下列环境问题与氮的氧化物排放无关的是
A.酸雨B.光化学烟雾C温室效应 D.白色污染
②在含有agHNO3的稀硝酸中,加入bg铁粉充分反应,铁全部溶解并生成NO,有0.25agHNO3被还原,则
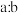 可能为
可能为A.2:1 B.3:1 C.4:1 D.9:2
③为避免氮氧化物污染环境,人们开发了溶液吸收法。比如用碱性的Na2CO3溶液吸收NO2,请写出相关的化学反应方程式:
您最近一年使用:0次