如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色,D极石墨棒上有红色的固体生成。请回答:
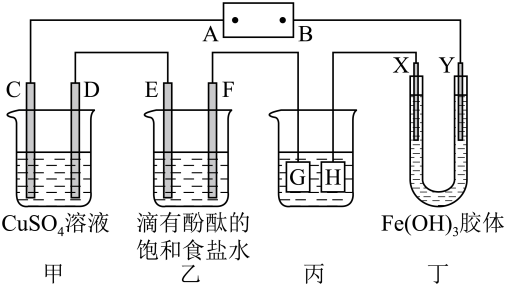
(1)B极是电源的___ 极;
(2)C电极反应式为___ ;
(3)一段时间后,丁装置中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明氢氧化铁胶体粒子带___ 电荷(填“正”或“负”)。
(4)若甲烧杯中D极石墨棒上析出红色的固体质量为6.4g时,则乙烧杯中E电极生成的气体在标况下的体积为___ ;
(5)乙烧杯中电解总反应化学方程式为___ 。

(1)B极是电源的
(2)C电极反应式为
(3)一段时间后,丁装置中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明氢氧化铁胶体粒子带
(4)若甲烧杯中D极石墨棒上析出红色的固体质量为6.4g时,则乙烧杯中E电极生成的气体在标况下的体积为
(5)乙烧杯中电解总反应化学方程式为
更新时间:2020-09-27 12:05:34
|
相似题推荐
【推荐1】Ⅰ.(1)研究和解决二氧化碳捕集和转化问题是当前科学研究的前沿领域。
已知:2CO(g) + O2(g) = 2CO2 (g) ΔH= -566kJ/mol
S(s) + O2(g) = SO2 (g) ΔH= -296kJ/mol
一定条件下,可以通过CO与SO2反应生成S(s)和一种无毒的气体,实现燃煤烟气中硫的回收,写出该反应的热化学方程式__________________
(2)向恒容密闭容器中充入 2molCO2 (g),发生反应:2CO2 (g)=2CO(g) + O2(g) ΔH= +566kJ/mol,测得温度为T℃时,容器内O2的物质的量浓度随时间的变化如图曲线Ⅱ所示,图中曲线Ⅰ是相对于曲线Ⅱ仅改变一种反应条件后c(O2)随时间的变化曲线,则改变的条件是______________________ ;a、b两点用CO浓度表示的反应速率关系为Va (CO)____ Vb(CO)

Ⅱ.某学习小祖为研究电化学相关原理,设计了如图所示装置图,A为直流电源,c、d为惰性电极,B为浸透饱和氯化钠溶液pH试纸,接通电路后,电极d附近先变红后褪色,请回答下列问题:

(1)电源A的a为___ 极;
(2)pH试纸上c处发生的电极反应为:________________ .
(3)欲在C中模拟氯碱工业,得到较纯的工业产品,可在C中增加_______ 交换膜(填“阳离子”或“阴离子”)
已知:2CO(g) + O2(g) = 2CO2 (g) ΔH= -566kJ/mol
S(s) + O2(g) = SO2 (g) ΔH= -296kJ/mol
一定条件下,可以通过CO与SO2反应生成S(s)和一种无毒的气体,实现燃煤烟气中硫的回收,写出该反应的热化学方程式
(2)向恒容密闭容器中充入 2molCO2 (g),发生反应:2CO2 (g)=2CO(g) + O2(g) ΔH= +566kJ/mol,测得温度为T℃时,容器内O2的物质的量浓度随时间的变化如图曲线Ⅱ所示,图中曲线Ⅰ是相对于曲线Ⅱ仅改变一种反应条件后c(O2)随时间的变化曲线,则改变的条件是

Ⅱ.某学习小祖为研究电化学相关原理,设计了如图所示装置图,A为直流电源,c、d为惰性电极,B为浸透饱和氯化钠溶液pH试纸,接通电路后,电极d附近先变红后褪色,请回答下列问题:

(1)电源A的a为
(2)pH试纸上c处发生的电极反应为:
(3)欲在C中模拟氯碱工业,得到较纯的工业产品,可在C中增加
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】工业上常用如下的方法从海水中提溴:

完成下列填空:
(1)上述流程中有两步都涉及到氯气。写出氯元素在周期表中的位置:___________ 。下列关于35C和37Cl原子的说法正确的是:___________
a.核外电子数相同 b.中子数相同 c.相对原子质量相同 d.互为同素异形体
(2)步骤②中体现了溴具有的性质是___________ 。
(3)写出步骤③中在水中进行的反应的化学方程式___________ ,在该反应中被氧化的元素是:___________ 。
(4)工业上利用海水还有一个重要的反应就是电解饱和食盐水,此反应中的阴极产物是:___________ (写化学式)。
(5)溴蒸汽还可以用饱和碳酸钠溶液来吸收,产物为溴化钠、溴酸钠,同时放出二氧化碳。请写出该反应的化学方程式并标明电子转移方向与数目:___________ 。

完成下列填空:
(1)上述流程中有两步都涉及到氯气。写出氯元素在周期表中的位置:
a.核外电子数相同 b.中子数相同 c.相对原子质量相同 d.互为同素异形体
(2)步骤②中体现了溴具有的性质是
(3)写出步骤③中在水中进行的反应的化学方程式
(4)工业上利用海水还有一个重要的反应就是电解饱和食盐水,此反应中的阴极产物是:
(5)溴蒸汽还可以用饱和碳酸钠溶液来吸收,产物为溴化钠、溴酸钠,同时放出二氧化碳。请写出该反应的化学方程式并标明电子转移方向与数目:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】我国由海水提取的食盐(海盐)不足四成,大部分产自内陆盐湖(湖盐)和盐矿(矿盐)。
(1)由内陆盐湖水为原料进行晒盐,有“夏天采盐(食盐)、冬天捞硝(芒硝)”的说法,下列对其化学原理的描述正确的是___ (选填编号)。
a.由夏到冬,芒硝的溶解度变小
b.由冬到夏,氯化钠的溶解度变小
c.夏天温度高,氯化钠易结晶析出
(2)芒硝型矿盐卤水中含有一定量Na2SO4和少量Ca2+、Mg2+、H2S等杂质,利用硫酸钙微溶于水的性质,用石灰-烟道气(CO2)法净化芒硝型矿盐卤水的流程如图:

脱硫工序中先吹空气,发生物理和化学变化:物理变化是氢硫酸有挥发性,部分被直接吹出,化学变化是___ (用化学方程式表示)。再加入稍过量的FeCl3溶液除去残留的硫化氢。检验FeCl3已经过量的试剂是___ (填写化学式)。
(3)加入Ca(OH)2能降低芒硝浓度并生成烧碱,同时除去Fe3+,另一目的是___ 。滤渣A的主要成分除了Fe(OH)3外,还有___ (填写化学式)。
(4)如图所示是石灰-纯碱法净化芒硝型矿盐卤水的部分流程:加入纯碱的作用是___ (选填编号)。
a.调节溶液的pH b.除去溶液中的Ca2+
c.除去溶液中的Mg2+ d.除去溶液中的SO42―
石灰-烟道气法与石灰-纯碱法相比较,石灰-烟道气法的优点是___ 。

(5)如图是离子交换膜法电解食盐水的示意图,离子交换膜只允许阳离子通过,上述精盐水需要进行二次精制后才能作为离子交换膜电解槽的原料。对盐水进行二次精制的目的是___ (选填编号)。
a.进一步降低Ca2+、Mg2+的浓度,提高烧碱纯度
b.进一步降低SO42―的浓度,提高烧碱纯度
c.防止杂质离子与碱生成的沉淀堵塞离子交换膜
d.防止溶液酸性或碱性过强,腐蚀离子交换膜
盐水中硫酸根浓度过高会使生成的氯气中混有氧气,检验氯气中是否含有少量氧气的操作是___ 。

(1)由内陆盐湖水为原料进行晒盐,有“夏天采盐(食盐)、冬天捞硝(芒硝)”的说法,下列对其化学原理的描述正确的是
a.由夏到冬,芒硝的溶解度变小
b.由冬到夏,氯化钠的溶解度变小
c.夏天温度高,氯化钠易结晶析出
(2)芒硝型矿盐卤水中含有一定量Na2SO4和少量Ca2+、Mg2+、H2S等杂质,利用硫酸钙微溶于水的性质,用石灰-烟道气(CO2)法净化芒硝型矿盐卤水的流程如图:

脱硫工序中先吹空气,发生物理和化学变化:物理变化是氢硫酸有挥发性,部分被直接吹出,化学变化是
(3)加入Ca(OH)2能降低芒硝浓度并生成烧碱,同时除去Fe3+,另一目的是
(4)如图所示是石灰-纯碱法净化芒硝型矿盐卤水的部分流程:加入纯碱的作用是
a.调节溶液的pH b.除去溶液中的Ca2+
c.除去溶液中的Mg2+ d.除去溶液中的SO42―
石灰-烟道气法与石灰-纯碱法相比较,石灰-烟道气法的优点是

(5)如图是离子交换膜法电解食盐水的示意图,离子交换膜只允许阳离子通过,上述精盐水需要进行二次精制后才能作为离子交换膜电解槽的原料。对盐水进行二次精制的目的是
a.进一步降低Ca2+、Mg2+的浓度,提高烧碱纯度
b.进一步降低SO42―的浓度,提高烧碱纯度
c.防止杂质离子与碱生成的沉淀堵塞离子交换膜
d.防止溶液酸性或碱性过强,腐蚀离子交换膜
盐水中硫酸根浓度过高会使生成的氯气中混有氧气,检验氯气中是否含有少量氧气的操作是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】请用下图所示仪器装置设计一个包括电解饱和食盐水并测定电解时产生的氢气的体积和检验氯气的氧化性的实验装置。

(1)所选仪器连接时,各接口的顺序是(填各接口的代号字母):A接,接,B接,接。_____________
(2)实验时,装置中的石墨电极接电源的_____ 极,所发生的电极反应式为_____ ;铁电极接电源的_____ 极,所发生的电极反应式为_____ ;此电解总反应方程式为_________ 。
(3)实验测得产生的氢气体积(已折算成标准状况)为5.60 mL,电解后溶液的体积恰好为50.0 mL,则溶液中OH-的浓度为_____ 。

(1)所选仪器连接时,各接口的顺序是(填各接口的代号字母):A接,接,B接,接。
(2)实验时,装置中的石墨电极接电源的
(3)实验测得产生的氢气体积(已折算成标准状况)为5.60 mL,电解后溶液的体积恰好为50.0 mL,则溶液中OH-的浓度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】锂被誉为“高能金属”。工业上用硫酸与β-锂辉矿(LiAlSi2O6和少量钙镁杂质)在250~300℃反应,生成Li2SO4以及硅铝化合物、MgSO4等,其工业生产流程如下:
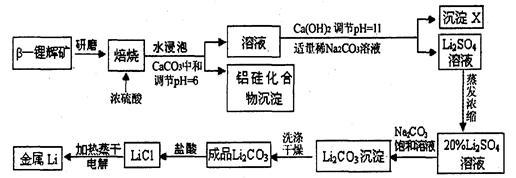
(1)用氧化物形式表示LiAlSi2O6的组成:______________ 。
(2)沉淀X的主要成分是(写化学式)______________________ 。
(3)流程中两次使用了Na2CO3溶液,试说明前后浓度不同的原因:_________________ 。
(4)锂和氢气在加热时能反应生成白色固体氢化锂,氢化锂遇到水就立即溶解并释放出大量的气体。试写出氢化锂遇水反应的化学方程式:______________ 。
(5)将盐酸与Li2CO3完全反应后的溶液,加热蒸干得到固体,再将其熔融电解生产锂。电解时产生的氯气中会混有少量氧气,原因是____________________ 。

(1)用氧化物形式表示LiAlSi2O6的组成:
(2)沉淀X的主要成分是(写化学式)
(3)流程中两次使用了Na2CO3溶液,试说明前后浓度不同的原因:
(4)锂和氢气在加热时能反应生成白色固体氢化锂,氢化锂遇到水就立即溶解并释放出大量的气体。试写出氢化锂遇水反应的化学方程式:
(5)将盐酸与Li2CO3完全反应后的溶液,加热蒸干得到固体,再将其熔融电解生产锂。电解时产生的氯气中会混有少量氧气,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】某小组以黄铜矿(主要成分为 CuFeS2,含少量SiO2等杂质)为原料制备铜化工产品CuAlO2的一种工艺如下:
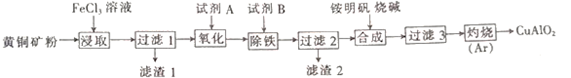
已知①过滤1所得滤液中含金属离子有:Cu2+、Fe2+和Fe3+,滤渣1的主要成分是:SiO2和S;
②Cu(OH)2+4NH3·H2O====[Cu(NH3)4]2++2OH-+4H2O。
(1)从产品纯度、环保操作方便等角度考虑,试剂A、B的最佳组合是__________ (填代号)

(2)铵明矾的化学式为NH4Al(SO4)2·12H2O,它为制备铜化工产品提供铝源。铵明矾溶液中NH4+、A13+、H+、OH-、SO42-浓度大小排序为______________________________ 。
(3)过滤3得到A1(OH)3和Cu(OH)2,写出“灼烧”发生化学反应的方程式:______________________________ 。
(4)单位时间内“浸取”Cu2+的百分率(称为浸出率)与溶液浓度、温度关系如图1所示。
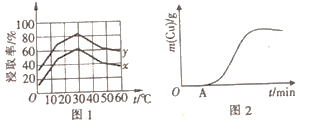
在20℃时,1L溶液中有效碰撞总次数:x_________ y(填“>”“<”或“=”)。相同浓度下,温度高于30℃,“浸出率”降低的主要原因是____________________________________ 。
(5)以铜、石墨为电极,电解“过滤1”所得溶液制备铜,铜的质量与通电时间关系如图2所示。写出OA段阴极的反应方程式:___________________________ 。
(6)常温下,Ksp[Fe(OH)3]=4.0×10-38。加入试剂B调节pH=3时c(Fe3+)=_________ mol·L-1

已知①过滤1所得滤液中含金属离子有:Cu2+、Fe2+和Fe3+,滤渣1的主要成分是:SiO2和S;
②Cu(OH)2+4NH3·H2O====[Cu(NH3)4]2++2OH-+4H2O。
(1)从产品纯度、环保操作方便等角度考虑,试剂A、B的最佳组合是

(2)铵明矾的化学式为NH4Al(SO4)2·12H2O,它为制备铜化工产品提供铝源。铵明矾溶液中NH4+、A13+、H+、OH-、SO42-浓度大小排序为
(3)过滤3得到A1(OH)3和Cu(OH)2,写出“灼烧”发生化学反应的方程式:
(4)单位时间内“浸取”Cu2+的百分率(称为浸出率)与溶液浓度、温度关系如图1所示。

在20℃时,1L溶液中有效碰撞总次数:x
(5)以铜、石墨为电极,电解“过滤1”所得溶液制备铜,铜的质量与通电时间关系如图2所示。写出OA段阴极的反应方程式:
(6)常温下,Ksp[Fe(OH)3]=4.0×10-38。加入试剂B调节pH=3时c(Fe3+)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】金秋十月,也是许多重大工程项目的攻坚时刻。在江苏滨海国家重点能源项目工程施工现场,1800多名工人正在加班加点建设,不远处的海面上,亚洲最大的重型自航绞吸船“天鲲号”正在疏浚航道。这个项目建成后,将为华东地区提供持续稳定清洁的天然气。新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液(滴有几滴酚酞)电解实验,如图所示。

回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为___________ 、___________ 。
(2)如图所示U形管中氯化钠溶液的体积为80mL。闭合K后,若每个电池甲烧用量均为0.224L(标况),且反应完全,则理论上通过电解池的电量为_______ (保留两位小数,已知法拉第常数F=9.65×104C/mol),若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为________ 。
(3)若每个电池甲烷通入量为1L(标准状况),且反应完全,则理论上最多能产生的氯气体积为______ L(标准状况)。
(4)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。

分析图可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为________ 。

回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为
(2)如图所示U形管中氯化钠溶液的体积为80mL。闭合K后,若每个电池甲烧用量均为0.224L(标况),且反应完全,则理论上通过电解池的电量为
(3)若每个电池甲烷通入量为1L(标准状况),且反应完全,则理论上最多能产生的氯气体积为
(4)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。

分析图可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)实验室由炼钢污泥 简称铁泥,主要成分为铁的氧化物
简称铁泥,主要成分为铁的氧化物 制备软磁性材料α-Fe2O3。其主要实验流程如图。
制备软磁性材料α-Fe2O3。其主要实验流程如图。

①酸浸。用一定浓度的H2SO4溶液浸取铁泥中的铁元素。若其他条件不变,实验中提高铁元素浸出率的措施有___________ (写2条)。
②还原。向“酸浸”后的滤液中加入过量铁粉,使Fe3+完全转化为 。“还原”过程中除生成
。“还原”过程中除生成 外,还会生成
外,还会生成___________ (填化学式);检验Fe3+是否还原完全的实验操作是___________ 。
③除杂。向“还原”后的滤液中加入 溶液,使
溶液,使 转化为
转化为 沉淀除去。若溶液的pH偏低,将会导致
沉淀除去。若溶液的pH偏低,将会导致 沉淀不完全,原因是
沉淀不完全,原因是___________ [ ]。
]。
(2)下图是利用甲烷燃料电池电解 的氯化铜溶液的装置示意图:
的氯化铜溶液的装置示意图:

请回答:
①甲烷燃料电池负极反应式是___________ 。
②当线路中有 电子通过时,
电子通过时,___________  填“a”或“b”
填“a”或“b” 极增重
极增重___________ 
(3)①在化学分析中采用 为指示剂,以
为指示剂,以 标准溶液滴定溶液中
标准溶液滴定溶液中 ,利用
,利用 与
与 生成砖红色沉淀,指示到达滴定终点。当溶液中
生成砖红色沉淀,指示到达滴定终点。当溶液中 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于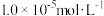 )时,溶液中
)时,溶液中 为
为___________  ,此时溶液中
,此时溶液中 等于
等于___________  (已知
(已知 、AgCl的
、AgCl的 分别为
分别为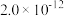 和
和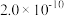 )。
)。
②+6价铬的化合物毒性较大,常用 将废液中的
将废液中的 还原成
还原成 ,该反应的离子方程式为
,该反应的离子方程式为___________
 简称铁泥,主要成分为铁的氧化物
简称铁泥,主要成分为铁的氧化物 制备软磁性材料α-Fe2O3。其主要实验流程如图。
制备软磁性材料α-Fe2O3。其主要实验流程如图。
①酸浸。用一定浓度的H2SO4溶液浸取铁泥中的铁元素。若其他条件不变,实验中提高铁元素浸出率的措施有
②还原。向“酸浸”后的滤液中加入过量铁粉,使Fe3+完全转化为
 。“还原”过程中除生成
。“还原”过程中除生成 外,还会生成
外,还会生成③除杂。向“还原”后的滤液中加入
 溶液,使
溶液,使 转化为
转化为 沉淀除去。若溶液的pH偏低,将会导致
沉淀除去。若溶液的pH偏低,将会导致 沉淀不完全,原因是
沉淀不完全,原因是 ]。
]。(2)下图是利用甲烷燃料电池电解
 的氯化铜溶液的装置示意图:
的氯化铜溶液的装置示意图:
请回答:
①甲烷燃料电池负极反应式是
②当线路中有
 电子通过时,
电子通过时, 填“a”或“b”
填“a”或“b” 极增重
极增重
(3)①在化学分析中采用
 为指示剂,以
为指示剂,以 标准溶液滴定溶液中
标准溶液滴定溶液中 ,利用
,利用 与
与 生成砖红色沉淀,指示到达滴定终点。当溶液中
生成砖红色沉淀,指示到达滴定终点。当溶液中 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于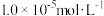 )时,溶液中
)时,溶液中 为
为 ,此时溶液中
,此时溶液中 等于
等于 (已知
(已知 、AgCl的
、AgCl的 分别为
分别为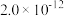 和
和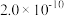 )。
)。②+6价铬的化合物毒性较大,常用
 将废液中的
将废液中的 还原成
还原成 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】如图是两种溶液进行电解的装置。电极A是由金属M制成的,M的硝酸盐的化学式为M(NO3)2,B、C、D都是铂电极,P、Q是电池的两极。

(1)电路接通后,B极上析出金属M,其电极反应为_______ ;同时C极产生____ ,电极反应为_______ ;D极产生____ ,电极反应为_______ 。
(2)电池中P是____ 极,Q是____ 极。
(3)A极上电极反应为__________ 。
(4)当电路中通过2.408×1022个电子时,B极上析出1.27 g M,则M的相对原子质量为____ 。
(5)如果将电池的正、负极交换接入原电路,当通过1.204×1022个电子时,B极上的现象是________ ,电极反应为______ ;A极上析出金属___ g,电极反应为______ (假设M为Cu)。

(1)电路接通后,B极上析出金属M,其电极反应为
(2)电池中P是
(3)A极上电极反应为
(4)当电路中通过2.408×1022个电子时,B极上析出1.27 g M,则M的相对原子质量为
(5)如果将电池的正、负极交换接入原电路,当通过1.204×1022个电子时,B极上的现象是
您最近一年使用:0次



