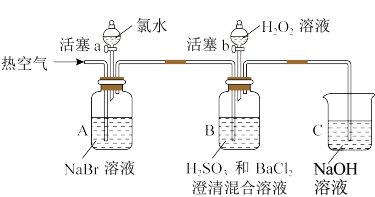
某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
实验记录如下:
完成下列填空:
(1)在进行操作①时,A中的实验现象是______ ,有关反应的离子方程式是_____________
(2)操作②吹入热空气的目的是______ 。B中产生的白色沉淀的化学式是_______________ 。
(3)装置C的作用是____________ 。
(4)由上述实验可知,在此实验条件下,H2O2、H2SO3、Br2氧化性强弱顺序为_________ 。

实验记录如下:
| 实验操作 | 实验现象 | |
| ① | 打开活塞a,滴加氯水,关闭活塞a | |
| ② | 吹入热空气一段时间后停止 | A中溶液颜色明显变浅;B中有气泡,产生大量白色沉淀,沉降后上层清液为无色 |
| ③ | 打开活塞b,逐滴加入H2O2溶液 | 开始时溶液颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成橙红色 |
(1)在进行操作①时,A中的实验现象是
(2)操作②吹入热空气的目的是
(3)装置C的作用是
(4)由上述实验可知,在此实验条件下,H2O2、H2SO3、Br2氧化性强弱顺序为
更新时间:2020-10-10 08:58:59
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学为验证同主族元素原子得电子能力强弱进行如下实验:
Ⅰ.向 溶液中滴加少量氯水,充分反应后,加1mL四氯化碳振荡,静置;
溶液中滴加少量氯水,充分反应后,加1mL四氯化碳振荡,静置;
Ⅱ.向 溶液中滴加少量氯水,充分反应后,加1mL四氯化碳振荡,静置;
溶液中滴加少量氯水,充分反应后,加1mL四氯化碳振荡,静置;
Ⅲ.在淀粉碘化钾试纸上滴加几滴溴水。
回答下列问题:
(1)实验Ⅰ的现象_______ 。
(2)根据Ⅰ、Ⅱ、Ⅲ的实验现象可得实验结论为_______ ,请用原子结构的知识解释其原因:_______ 。
(3)实验Ⅰ、Ⅱ得到的 层中含有卤素单质,可用
层中含有卤素单质,可用 浓溶液反萃取分离回收。以下是反萃取回收
浓溶液反萃取分离回收。以下是反萃取回收 的操作过程:
的操作过程:
①向装有 的
的 溶液的
溶液的_______ (填仪器名称)中加入少量浓 溶液;
溶液;
②振荡至溶液的_______ 色消失,振荡过程中仪器内压强会增大,需要打开下口活塞放气;
③静置、分层,先将 层从仪器的下口放出,再将含NaI与NaIO3的碱溶液从仪器的
层从仪器的下口放出,再将含NaI与NaIO3的碱溶液从仪器的_______ (填“上”、“下”)口倒入烧杯中;
④边搅拌边加入几滴45%的 溶液,溶液立即转为棕黄色,并析出碘晶体,写出该反应的离子方程式
溶液,溶液立即转为棕黄色,并析出碘晶体,写出该反应的离子方程式_______ 。
Ⅰ.向
 溶液中滴加少量氯水,充分反应后,加1mL四氯化碳振荡,静置;
溶液中滴加少量氯水,充分反应后,加1mL四氯化碳振荡,静置;Ⅱ.向
 溶液中滴加少量氯水,充分反应后,加1mL四氯化碳振荡,静置;
溶液中滴加少量氯水,充分反应后,加1mL四氯化碳振荡,静置;Ⅲ.在淀粉碘化钾试纸上滴加几滴溴水。
回答下列问题:
(1)实验Ⅰ的现象
(2)根据Ⅰ、Ⅱ、Ⅲ的实验现象可得实验结论为
(3)实验Ⅰ、Ⅱ得到的
 层中含有卤素单质,可用
层中含有卤素单质,可用 浓溶液反萃取分离回收。以下是反萃取回收
浓溶液反萃取分离回收。以下是反萃取回收 的操作过程:
的操作过程:①向装有
 的
的 溶液的
溶液的 溶液;
溶液;②振荡至溶液的
③静置、分层,先将
 层从仪器的下口放出,再将含NaI与NaIO3的碱溶液从仪器的
层从仪器的下口放出,再将含NaI与NaIO3的碱溶液从仪器的④边搅拌边加入几滴45%的
 溶液,溶液立即转为棕黄色,并析出碘晶体,写出该反应的离子方程式
溶液,溶液立即转为棕黄色,并析出碘晶体,写出该反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
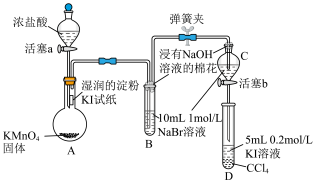
【推荐2】为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)实验过程:
①.打开弹簧夹,打开活塞a,滴加浓盐酸;
②.当B和C中的溶液都变为黄色时,夹紧弹簧夹;
③.当B中溶液由黄色变为棕红色时,关闭活塞a;
④.……
请回答问题:
(1)A中产生黄绿色气体,其与氨气反应后的产物的电子式是___________ ;实验室在加热条件下制取该气体的离子方程式为___________ ;
(2)简单设计一个验证氯气的氧化性强于碘单质的实验___________ ;
(3)过程③实验的目的:某同学经分析认为,B中溶液由黄色变为棕红色,以此说明C中___________ ,从而得出D中氧化I-的氧化剂必为Br2,因此B装置是必不可少的;
(4)过程④为:打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下试管D震荡,静置,观察到的现象是___________ ,发生反应的离子方程式为___________ ;
(5)浸有NaOH溶液的棉花的作用是___________ ;
(6)用原子结构理论解释氯、溴、碘单质的氧化性逐渐减弱的原因是:同主族元素从下到上___________ ,得电子能力逐渐减弱。
①.打开弹簧夹,打开活塞a,滴加浓盐酸;
②.当B和C中的溶液都变为黄色时,夹紧弹簧夹;
③.当B中溶液由黄色变为棕红色时,关闭活塞a;
④.……

请回答问题:
(1)A中产生黄绿色气体,其与氨气反应后的产物的电子式是
(2)简单设计一个验证氯气的氧化性强于碘单质的实验
(3)过程③实验的目的:某同学经分析认为,B中溶液由黄色变为棕红色,以此说明C中
(4)过程④为:打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下试管D震荡,静置,观察到的现象是
(5)浸有NaOH溶液的棉花的作用是
(6)用原子结构理论解释氯、溴、碘单质的氧化性逐渐减弱的原因是:同主族元素从下到上
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】氮和氧是构建化合物的常见元素。
(1)下列说法正确的是___________。
(2)①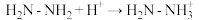 ,其中
,其中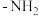 的
的 原子杂化方式为
原子杂化方式为___________ ;比较键角 中的-NH2
中的-NH2_____ H2N-NH 中的-NH
中的-NH (填“>”、“<”或“=”),请说明理由
(填“>”、“<”或“=”),请说明理由___________ 。
②将 与
与 按物质的量之比
按物质的量之比 发生化合反应生成A,测得A由2种微粒构成,其中之一是
发生化合反应生成A,测得A由2种微粒构成,其中之一是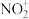 。比较氧化性强弱:NO
。比较氧化性强弱:NO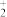
_____ HNO3(填“>”、“<”或“=”);写出A中阴离子的结构式___________ 。
已知: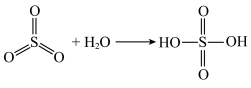
(1)下列说法正确的是___________。
A.电负性: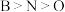 | B.离子半径: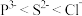 |
C.第一电离能: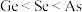 | D.基态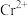 的简化电子排布式: 的简化电子排布式: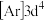 |
(2)①
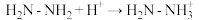 ,其中
,其中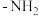 的
的 原子杂化方式为
原子杂化方式为 中的-NH2
中的-NH2 中的-NH
中的-NH (填“>”、“<”或“=”),请说明理由
(填“>”、“<”或“=”),请说明理由②将
 与
与 按物质的量之比
按物质的量之比 发生化合反应生成A,测得A由2种微粒构成,其中之一是
发生化合反应生成A,测得A由2种微粒构成,其中之一是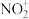 。比较氧化性强弱:NO
。比较氧化性强弱:NO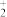
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某课外活动小组做了如下关于钠的探究实验。
探究一:钠与水反应
(1)①在通常实验中钠常会着火燃烧,并发生轻微爆炸,写出钠与水反应的离子方程式_____________________________ 。
②用如图所示的实验装置可以进行钠与水反应的实验,并可收集、检验生成的气体,煤油的密度为0.8 g/cm3液体物质添加完毕后,关闭活塞A,向煤油中加入一小块钠,立即塞好胶塞,反应开始前钠的位置在______ 处(填“a”、“b”或“c”)。
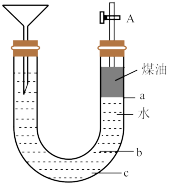
探究二:钠与氯气反应
(2)钠在氯气中燃烧的现象:剧烈燃烧,火焰呈______ 色且有______ 生成。
(3)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验。
①下列收集Cl2的正确装置是______ 。

②利用上述方法制取标准状况下11.2 LCl2,则作还原剂的HCl的物质的量是__________ 。
③将Cl2通入水中,所得溶液中具有氧化性的含氯微粒有Cl2、________ (2种)。
探究一:钠与水反应
(1)①在通常实验中钠常会着火燃烧,并发生轻微爆炸,写出钠与水反应的离子方程式
②用如图所示的实验装置可以进行钠与水反应的实验,并可收集、检验生成的气体,煤油的密度为0.8 g/cm3液体物质添加完毕后,关闭活塞A,向煤油中加入一小块钠,立即塞好胶塞,反应开始前钠的位置在

探究二:钠与氯气反应
(2)钠在氯气中燃烧的现象:剧烈燃烧,火焰呈
(3)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验。
①下列收集Cl2的正确装置是

②利用上述方法制取标准状况下11.2 LCl2,则作还原剂的HCl的物质的量是
③将Cl2通入水中,所得溶液中具有氧化性的含氯微粒有Cl2、
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】舍勒制备氯气的方法至今还在实验室使用。按照下图所示装置进行有关实验,打开玻璃活塞F,将A逐滴加入B中。若A中盛放浓盐酸,B中盛放二氧化锰。

回答下列问题:
(1)仪器A的名称是___________ 。
(2)写出当将A滴入B中并加热时发生反应的化学方程式,并用双线桥法表示电子转移的方向和数目___________
(3)当实验进行一段时间后,发现盛装铜粉的硬质玻璃管C中有棕黄色烟产生,则C中发生反应的化学方程式为___________ 。
(4)若将装置Ⅱ换成装置Ⅳ,则可观察到装置Ⅳ的现象为___________
(5)若E中盛有NaOH溶液,此溶液的作用是___________ ,D装置的作用是___________ 。
(6)通过电解饱和食盐水为基础制取氯气、烧碱等产品的工业称为氯碱工业,请写出该反应的化学方程式___________ 。

回答下列问题:
(1)仪器A的名称是
(2)写出当将A滴入B中并加热时发生反应的化学方程式,并用双线桥法表示电子转移的方向和数目
(3)当实验进行一段时间后,发现盛装铜粉的硬质玻璃管C中有棕黄色烟产生,则C中发生反应的化学方程式为
(4)若将装置Ⅱ换成装置Ⅳ,则可观察到装置Ⅳ的现象为
(5)若E中盛有NaOH溶液,此溶液的作用是
(6)通过电解饱和食盐水为基础制取氯气、烧碱等产品的工业称为氯碱工业,请写出该反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】钠及其化合物在生产生活中具有广泛的作用。
Ⅰ.化工专家侯德榜发明的侯氏制碱法,其工艺流程图如下:

已知:氯化铵在加热条件下生成氨气和氯化氢。
(1)由工艺流程图可知可以循环使用的物质有___________ (填化学式)。
(2)写出碳酸化过程中发生反应的化学方程式:___________ 。
(3)欲除去制得的碳酸钠中的碳酸氢钠可用加热的方法,用化学方程式表示其原理______ 。
(4)若在(3)中加热的时间较短, 分解不完全,取加热了
分解不完全,取加热了 的
的 样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中部分离子的物质的量的变化如图所示:
样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中部分离子的物质的量的变化如图所示:

①M点的溶质成分是___________ 。
②若N点时溶液体积为200mL,则溶液中溶质的物质的量浓度为___________ 。
Ⅱ.高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A、F为非金属单质气体,B为常见金属单质,E为生活中最常见的调味品,F在标准状况下密度为0.090 。
。

请回答下列问题:
(5)写出反应②的化学方程式:___________ 。
(6)反应④中各物质的反应比例关系如下,请填入相应的反应物和生成物的化学式,并用单线桥标明电子转移的方向和数目:_______ 。
3 +2
+2 +10NaOH =2Na2FeO4+9
+10NaOH =2Na2FeO4+9 +5H2O
+5H2O
(7)写出反应⑤的化学方程式:___________ 。
Ⅰ.化工专家侯德榜发明的侯氏制碱法,其工艺流程图如下:

已知:氯化铵在加热条件下生成氨气和氯化氢。
(1)由工艺流程图可知可以循环使用的物质有
(2)写出碳酸化过程中发生反应的化学方程式:
(3)欲除去制得的碳酸钠中的碳酸氢钠可用加热的方法,用化学方程式表示其原理
(4)若在(3)中加热的时间较短,
 分解不完全,取加热了
分解不完全,取加热了 的
的 样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中部分离子的物质的量的变化如图所示:
样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中部分离子的物质的量的变化如图所示:
①M点的溶质成分是
②若N点时溶液体积为200mL,则溶液中溶质的物质的量浓度为
Ⅱ.高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A、F为非金属单质气体,B为常见金属单质,E为生活中最常见的调味品,F在标准状况下密度为0.090
 。
。
请回答下列问题:
(5)写出反应②的化学方程式:
(6)反应④中各物质的反应比例关系如下,请填入相应的反应物和生成物的化学式,并用单线桥标明电子转移的方向和数目:
3
 +2
+2 +10NaOH =2Na2FeO4+9
+10NaOH =2Na2FeO4+9 +5H2O
+5H2O(7)写出反应⑤的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某小组拟设计实验探究影响氢氧化物 在铵盐溶液中溶解度的因素。
在铵盐溶液中溶解度的因素。
已知:①常温下,几种氢氧化物的溶度积:
②可能用到的试剂: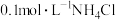 溶液、
溶液、 溶液,
溶液, 溶液和
溶液和 溶液。
溶液。
③常温下, 的电离常数
的电离常数 ,
, 的电离常数
的电离常数 。
。
实验I.比较 在不同浓度的
在不同浓度的 溶液中的溶解情况。
溶液中的溶解情况。
(1)从科学性角度考虑,还需要设计的对照实验是___________ 。
(2)针对实验i,“白色浊液”变澄清的原因,提出如下假设:
假设①: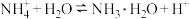 ,
,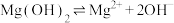 ,
, 。
。
假设②: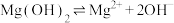 ,
,___________ (补充离子方程式)。
(3)为了验证(2)提出的假设,设计如下实验:
实验II.比较 在不同浓度的
在不同浓度的 溶液中的溶解情况。
溶液中的溶解情况。
实验结论是(2)中假设___________ 成立(填“①”或“②”)。
(4)根据上述实验,有同学认为金属氢氧化物都能溶于 溶液。为了验证他的观点,设计如下实验:
溶液。为了验证他的观点,设计如下实验:
实验III.探究 、
、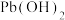 、
、 在
在 溶液中溶解情况。
溶液中溶解情况。
已知: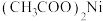 、
、 、
、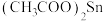 都易溶于水。
都易溶于水。
预测:实验vi现象不同的可能原因是___________ 。设计简单实验证明:___________ 。
(5)通过上述实验,影响氢氧化物的铵盐溶液中溶解度的因素主要有浓度、___________ 、___________ 。
 在铵盐溶液中溶解度的因素。
在铵盐溶液中溶解度的因素。已知:①常温下,几种氢氧化物的溶度积:
| 物质 |  |  | 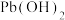 |  |
 |  | 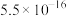 | 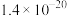 | 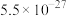 |
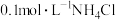 溶液、
溶液、 溶液,
溶液, 溶液和
溶液和 溶液。
溶液。③常温下,
 的电离常数
的电离常数 ,
, 的电离常数
的电离常数 。
。实验I.比较
 在不同浓度的
在不同浓度的 溶液中的溶解情况。
溶液中的溶解情况。| 操作 | 试剂X | 现象 |
 | i. 溶液 溶液 | 白色浊液逐渐变澄清 |
ii. 溶液 溶液 | 白色浊液变化不明显 |
(2)针对实验i,“白色浊液”变澄清的原因,提出如下假设:
假设①:
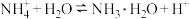 ,
,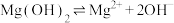 ,
, 。
。假设②:
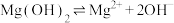 ,
,(3)为了验证(2)提出的假设,设计如下实验:
实验II.比较
 在不同浓度的
在不同浓度的 溶液中的溶解情况。
溶液中的溶解情况。| 操作 | 试剂X | 现象 |
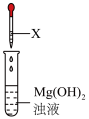 | iii.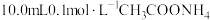 溶液 溶液 | 白色浊液逐渐变澄清 |
iv.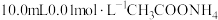 溶液 溶液 | 白色浊液变化不明显 |
(4)根据上述实验,有同学认为金属氢氧化物都能溶于
 溶液。为了验证他的观点,设计如下实验:
溶液。为了验证他的观点,设计如下实验:实验III.探究
 、
、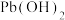 、
、 在
在 溶液中溶解情况。
溶液中溶解情况。| 操作 | 浊液Y | 现象 |
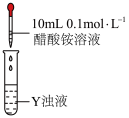 | v. | 没有明显现象 |
vi.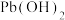 | 浊液变澄清溶液 | |
vii. | 没有明显现象 |
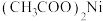 、
、 、
、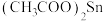 都易溶于水。
都易溶于水。预测:实验vi现象不同的可能原因是
(5)通过上述实验,影响氢氧化物的铵盐溶液中溶解度的因素主要有浓度、
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】为了研究非金属元素性质的变化规律,某同学设计如图实验装置。

(1)高锰酸钾在常温下与浓盐酸反应产生氯气,离子方程式为___________ 。
(2)如果A中盛放浓盐酸,B中盛放酸性高锰酸钾溶液,C中盛放饱和氢硫酸,反应开始后观察到C中产生淡黄色沉淀,证明氯的非金属性比硫的非金属性___________ (填“强”或“弱”或“无法判断”)。
(3)若用该装置证明Cl2氧化性强于I2的氧化性。则A中盛放浓盐酸,B中盛放高锰酸钾粉末,C中盛放淀粉KI溶液,则C中的现象为___________ 。
(4)现有浓硝酸、大理石、澄清石灰水、硅酸钠溶液,选择试剂用该装置证明:非金属性:N>C>Si。C中盛放试剂___________ ,实验现象为___________ ,该装置还存在不足之处,改进措施为___________ 。

(1)高锰酸钾在常温下与浓盐酸反应产生氯气,离子方程式为
(2)如果A中盛放浓盐酸,B中盛放酸性高锰酸钾溶液,C中盛放饱和氢硫酸,反应开始后观察到C中产生淡黄色沉淀,证明氯的非金属性比硫的非金属性
(3)若用该装置证明Cl2氧化性强于I2的氧化性。则A中盛放浓盐酸,B中盛放高锰酸钾粉末,C中盛放淀粉KI溶液,则C中的现象为
(4)现有浓硝酸、大理石、澄清石灰水、硅酸钠溶液,选择试剂用该装置证明:非金属性:N>C>Si。C中盛放试剂
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】高中常用“价类二维”思路研究物质的性质,如图是铁及其化合物的二维图的部分信息。

(1)X的化学式为______ 。图中物质只具有还原性的是______ 。(写化学式)
(2)将FeCl2溶液转化为FeCl3的试剂可选______ 。
a.稀硫酸 b.CuSO4溶液
c.酸性H2O2 d.溴水
(3)某中学实验小组设计如下实验探究亚铁盐的性质。
①实验I中由白色沉淀生成红褐色沉淀的化学方程式______ 。
②对实验II所得白色沉淀展开研究:
查阅资料:在溶液中不存在Fe(HCO3)2
i.取II中少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡;
ii.向i所得溶液中滴入KSCN试剂,溶液几乎不变红;
iii.向ii溶液中再滴入少量氯水,溶液立即变为红色。
根据以上现象,实验中生成的白色沉淀的化学式为______ 。
向ii溶液中再滴入少量氯水发生反应的离子方程式:_________ 。
(4) FeSO4可用作补铁剂,使用时医生建议与维生素C同服,同学甲猜测维生素C可将Fe3+转化为Fe2+以利于人体吸收。为了验证这一猜想,设计如下实验:
由上述实验能否得出维生素C可将Fe3+转化为Fe2+为的结论?______ (填“能”或“否”),请说明理由:___________ 。

(1)X的化学式为
(2)将FeCl2溶液转化为FeCl3的试剂可选
a.稀硫酸 b.CuSO4溶液
c.酸性H2O2 d.溴水
(3)某中学实验小组设计如下实验探究亚铁盐的性质。
实验方案 | 现象 | |
I | 1.0mL0.1mol/LFeSO4溶液中滴加1.0mL0.5mol/LNaOH溶液 | 生成白色沉淀,后沉淀基本变为红褐色 |
II | 1.0mL0.1mol/L FeSO4溶液中滴加1.0mL0.5mol/LNaHCO3溶液 | 生成白色沉淀,后沉淀颜色几乎不变 |
②对实验II所得白色沉淀展开研究:
查阅资料:在溶液中不存在Fe(HCO3)2
i.取II中少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡;
ii.向i所得溶液中滴入KSCN试剂,溶液几乎不变红;
iii.向ii溶液中再滴入少量氯水,溶液立即变为红色。
根据以上现象,实验中生成的白色沉淀的化学式为
向ii溶液中再滴入少量氯水发生反应的离子方程式:
(4) FeSO4可用作补铁剂,使用时医生建议与维生素C同服,同学甲猜测维生素C可将Fe3+转化为Fe2+以利于人体吸收。为了验证这一猜想,设计如下实验:
实验方案 | 实验现象 |
| 取适量Fe2(SO4)3溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液。 | 溶液紫红色褪去 |
您最近一年使用:0次



