重庆一中化学组李善梅老师,带着银制配饰用硫磺皂沐浴,发现配饰变黑了。于是在一个铝制容器中放入一定浓度的食盐溶液,再将变黑的银器浸入溶液中。放置一段时间后,黑色褪去,而银不会损失,已知此过程中能闻到淡淡的臭鸡蛋气味。下列关于以上现象说法错误的是( )
| A.银饰变黑属于化学腐蚀 |
| B.此硫磺皂为正品 |
| C.李老师的补救办法运用了原电池原理 |
| D.铝制容器可以用其它金属容器代替,只要能导电即可 |
更新时间:2020-10-21 12:10:49
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
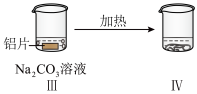
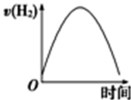
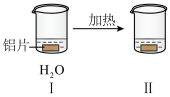
【推荐1】探究铝片与Na2CO3溶液的反应。
下列说法不正确 的是
 |
| |
| 无明显现象 | 铝片表面产生细小气泡 | 出现白色浑浊,产生大量气泡(经检验为H2和CO2) |
| A.对比Ⅰ、Ⅲ,说明Na2CO3溶液能破坏铝表面的保护膜 |
B.推测出现白色浑浊的原因:AlO + HCO + HCO + H2O = Al(OH)3↓+ CO + H2O = Al(OH)3↓+ CO |
C.加热和H2逸出对CO 水解平衡移动方向的影响是相反的 水解平衡移动方向的影响是相反的 |
D.Na2CO3溶液中存在水解平衡:CO + H2O ⇌ HCO + H2O ⇌ HCO + OH- + OH- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验操作不正确的是
| A.配制AlCl3溶液时,在溶液中滴加几滴稀盐酸 |
| B.探究温度对化学平衡移动的影响:将盛有NO2和N2O4混合气体的烧瓶,先后置于冷水和热水中,观察烧瓶中气体颜色的变化 |
| C.在pH试纸上分别滴加等浓度的CH3COONa、NaClO溶液,比较两者的水解程度的大小 |
| D.锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知常温下浓度为0.lmol/L的下列溶液的pH如下表,下列有关说法正确的是
| 溶质 | NaF | NaClO | Na2CO3 |
| pH | 7.5 | 9.7 | 11.6 |
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HClO< <HF <HF |
B.根据上表,水解方程式ClO-+H2O HClO+OH-的水解常数K=10-7.6 HClO+OH-的水解常数K=10-7.6 |
C.若将CO2通入0.lmol/LNa2CO3溶液中至溶液中性,则溶液中2c( )+c( )+c( )=0.1 mol/L )=0.1 mol/L |
| D.向上述NaClO溶液中通HF气体至恰好完全反应时:c(Na+)>c(F-)>(H+)>c(HClO)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作能达到实验目的的是
| A.用广泛pH试纸测得溶液的pH为2.3 |
| B.用滴加少量硫酸铜溶液的稀硫酸跟锌粒反应可以加快制取氢气的速率 |
| C.用酚酞溶液区分稀盐酸和食盐水 |
| D.将两根碳棒用导线相连接分别插入用盐桥相连的氯化铁溶液和氯化钾溶液中有电流产生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用足量铁片与稀硫酸反应制取氢气时,下列措施能使氢气生成速率加快且不影响氢气的量是
①加热
②将稀硫酸改为98%的浓硫酸
③加入少量KNO3固体
④铁粉替代铁片
⑤滴加几滴CuSO4溶液
⑥加入少量醋酸钠晶体(CH3COONa)
①加热
②将稀硫酸改为98%的浓硫酸
③加入少量KNO3固体
④铁粉替代铁片
⑤滴加几滴CuSO4溶液
⑥加入少量醋酸钠晶体(CH3COONa)
| A.①④⑤ | B.①③⑤ | C.②③⑥ | D.③④ |
您最近一年使用:0次