已知某工业废水中含有大量 CuSO4,少量的 Ag+、Hg2+以及部分污泥,通过下述过程可从该废水中回收硫酸铜晶体及其它物质.
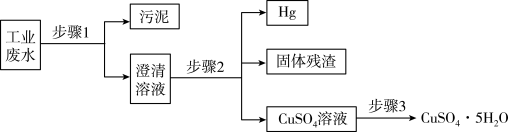
(1)步骤 1 的主要操作是_____ ,需用到的玻璃仪器除烧杯外有_____ 、_____ .
(2)步骤 2 中需加入某种试剂后再将混合物分离,该试剂是(填化学式)_____ ,固体残渣的成分是(填化学式)_____ .
(3)如何证明该步骤 2 后的溶液 Ag+已除尽_____ 。
(4)步骤 3 中涉及的操作是:蒸发浓缩、_____ 、过滤、烘干。
(5)写出在硫酸铜溶液中加入烧碱溶液发生反应的化学方程式___________ 。

(1)步骤 1 的主要操作是
(2)步骤 2 中需加入某种试剂后再将混合物分离,该试剂是(填化学式)
(3)如何证明该步骤 2 后的溶液 Ag+已除尽
(4)步骤 3 中涉及的操作是:蒸发浓缩、
(5)写出在硫酸铜溶液中加入烧碱溶液发生反应的化学方程式
更新时间:2020-10-19 16:39:34
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在,实验室里从海洋植物中提取碘的流程如下:
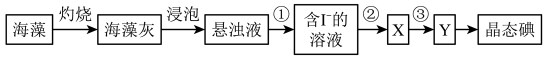
某化学兴趣小组将上述流程②③设计成如图所示实验。
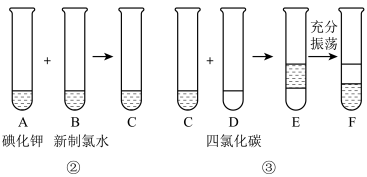
已知:②中发生反应的化学方程式为Cl2+2KI===2KCl+I2。
(1)写出提取流程中①③实验操作的名称:①__________ ,③________ 。
(2)四氯化碳是无色、密度比水大的液体。F中下层液体的颜色为________ 色,上层液体中溶质的主要成分为________ 。
(3)从F中得到碘单质还需进行的操作是________ 。

某化学兴趣小组将上述流程②③设计成如图所示实验。

已知:②中发生反应的化学方程式为Cl2+2KI===2KCl+I2。
(1)写出提取流程中①③实验操作的名称:①
(2)四氯化碳是无色、密度比水大的液体。F中下层液体的颜色为
(3)从F中得到碘单质还需进行的操作是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】某工厂酸性废液中含有Fe2+、Al3+、Fe3+、 ,以该废液为原料制备Fe2O3的工艺流程如下(部分操作和条件略去):
,以该废液为原料制备Fe2O3的工艺流程如下(部分操作和条件略去):
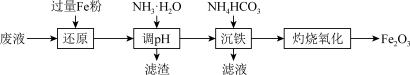
已知;NH4HCO3在热水中会分解。
(1)写出“还原”步骤中反应的离子方程式:___________ 。
(2)从流程中分析,“滤渣”的主要成分是___________ 。
(3)加入碳酸氢铵后过滤,发现滤液仍然浑浊,可能的原因是___________ ,用90℃热水洗涤FeCO3沉淀的目的是___________ 。
(4)若在实验室中灼烧FeCO3应在___________ (填仪器名称)中进行,“灼烧氧化”发生反应的化学方程式为___________ 。
 ,以该废液为原料制备Fe2O3的工艺流程如下(部分操作和条件略去):
,以该废液为原料制备Fe2O3的工艺流程如下(部分操作和条件略去):
已知;NH4HCO3在热水中会分解。
(1)写出“还原”步骤中反应的离子方程式:
(2)从流程中分析,“滤渣”的主要成分是
(3)加入碳酸氢铵后过滤,发现滤液仍然浑浊,可能的原因是
(4)若在实验室中灼烧FeCO3应在
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】一种由菱镁矿(主要成分MgCO3、还含少量FeCO3及SiO2)制备高纯氧化镁的工艺如下:
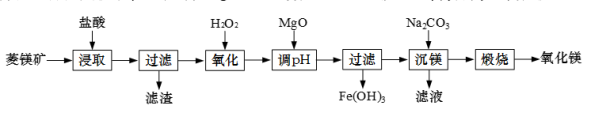
(1)“浸取”时加入盐酸需过量,原因是_______ 和_______ 。
(2) “调pH”时控制溶液的pH≈4.“调pH”时发生反应的离子方程式为_______ 。
(3)“沉镁”时,溶液中有Mg(OH)2和MgCO3析出。若此时溶液的pH=9,则“沉镁”所得溶液中c( )=
)=_______ mol·L-1。(已知Ksp[Mg(OH)2]=1.8×10-11,Ksp(MgCO3)=3.6×10-8)

(1)“浸取”时加入盐酸需过量,原因是
(2) “调pH”时控制溶液的pH≈4.“调pH”时发生反应的离子方程式为
(3)“沉镁”时,溶液中有Mg(OH)2和MgCO3析出。若此时溶液的pH=9,则“沉镁”所得溶液中c(
 )=
)=
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】碱式氯化铜是重要的无机杀菌剂,是一种绿色或墨绿色结晶性粉末,难溶于水,溶于稀酸和氨水,在空气中十分稳定。
Ⅰ.模拟制备碱式氯化铜。向CuCl2溶液中通入NH3和HCl,调节pH至5.0~5.5,控制反应温度于70~80℃,实验装置如图所示(部分夹持装置已省略)。
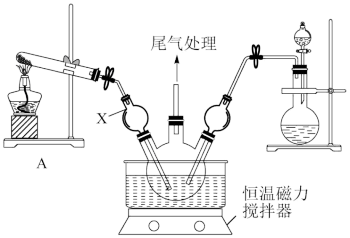
(1)仪器X的名称是___________ ,其主要作用有导气、___________ 。
(2)实验室利用装置A制NH3,发生反应的化学方程式为___________ 。
(3)反应过程中,在三颈烧瓶内除观察到溶液蓝绿色褪去,还可能观察到的现象有___________ 。
Ⅱ.无水碱式氯化铜组成的测定。称取产品4.29 g,加硝酸溶解,并加水定容至200 mL,得到待测液。
(4)铜的测定:取20.00 mL待测液,经测定Cu2+浓度为0.2 mol·L-1.则称取的样品中 n(Cu2+)=___________ mol。
(5)采用沉淀滴定法测定氯:用NH4SCN标准溶液滴定过量的AgNO3(已知:AgSCN是一种难溶于水的白色固体),实验如下图:

①滴定时,应选用下列哪种物质作为指示剂___________ (填标号)。
a.FeSO4 b.Fe(NO3)3 c.FeCl3
②重复实验操作三次,消耗NH4SCN溶液的体积平均为10.00 mL。则称取的样品中n(Cl-)=___________ mol。
(6)根据上述实验结果可推知无水碱式氯化铜的化学式为___________ 。
Ⅰ.模拟制备碱式氯化铜。向CuCl2溶液中通入NH3和HCl,调节pH至5.0~5.5,控制反应温度于70~80℃,实验装置如图所示(部分夹持装置已省略)。

(1)仪器X的名称是
(2)实验室利用装置A制NH3,发生反应的化学方程式为
(3)反应过程中,在三颈烧瓶内除观察到溶液蓝绿色褪去,还可能观察到的现象有
Ⅱ.无水碱式氯化铜组成的测定。称取产品4.29 g,加硝酸溶解,并加水定容至200 mL,得到待测液。
(4)铜的测定:取20.00 mL待测液,经测定Cu2+浓度为0.2 mol·L-1.则称取的样品中 n(Cu2+)=
(5)采用沉淀滴定法测定氯:用NH4SCN标准溶液滴定过量的AgNO3(已知:AgSCN是一种难溶于水的白色固体),实验如下图:

①滴定时,应选用下列哪种物质作为指示剂
a.FeSO4 b.Fe(NO3)3 c.FeCl3
②重复实验操作三次,消耗NH4SCN溶液的体积平均为10.00 mL。则称取的样品中n(Cl-)=
(6)根据上述实验结果可推知无水碱式氯化铜的化学式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】实验室制备氯气的方法是用软锰矿(主要成分为MnO2)与浓盐酸在加热条件下反应制得,也可以用高锰酸钾、氯酸钾或是重铬酸钾(K2Cr2O7)等与浓盐酸反应制得。
(1)实验室用软锰矿与浓盐酸加热制备氯气的反应的化学方程式为___________ ;若用足量浓盐酸与软锰矿共热制得3.36L氯气(已折算成标准状况),则在剩余溶液中加入足量AgNO3溶液得到的沉淀的质量___________ (填“大于”。“小于”或“等于”)43.05g,请说明理由:___________ 。
(2)如果用重铬酸钾(K2Cr2O7)代替软锰矿与浓盐酸反应制备氯气,其化学方程式为K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O。该反应的离子方程式为___________ ,反应中被还原的元素是___________ (填元素符号),氧化性:K2Cr2O7___________ (填“>”、“<”或“=”)Cl2;该反应中作还原剂的HCl与表现酸性的HCl的物质的量之比为___________ 。
(1)实验室用软锰矿与浓盐酸加热制备氯气的反应的化学方程式为
(2)如果用重铬酸钾(K2Cr2O7)代替软锰矿与浓盐酸反应制备氯气,其化学方程式为K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O。该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】纯碳酸钙广泛应用于精密电子陶瓷、医药等的生产,某兴趣小组按图所示实验步骤,模拟工业流程制备高纯碳酸钙,请回答下列问题。
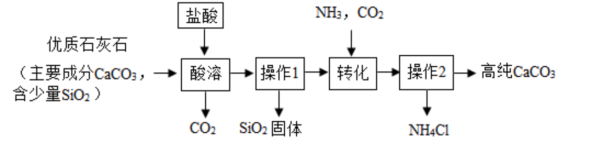
(1)“酸溶”过程中,提前将石灰石粉碎,并进行搅拌。目的是_______
(2)在“酸溶”过程中发生的化学反应方程式为_______
(3)“操作1”的名称_______
(4)实验室制取、收集干燥的NH3
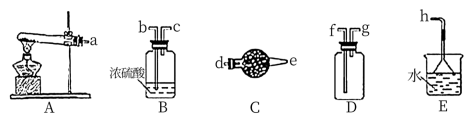
①需选用上述仪器装置的接口连接顺序是(填字母):a接_______ 、_______ 接_______ ,_______ 接h;实验室用A装置制取NH3的化学方程式为_______
②制备碳酸钙通入NH3和CO2气体时,应先通入的气体是_______ ,试写出制碳酸钙的化学方程式_______

(1)“酸溶”过程中,提前将石灰石粉碎,并进行搅拌。目的是
(2)在“酸溶”过程中发生的化学反应方程式为
(3)“操作1”的名称
(4)实验室制取、收集干燥的NH3

①需选用上述仪器装置的接口连接顺序是(填字母):a接
②制备碳酸钙通入NH3和CO2气体时,应先通入的气体是
您最近一年使用:0次



