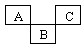
下表是元素周期表的一部分,回答下列有关问题(用化学符号回答):
(1)在①~⑩元素中,最活泼的金属元素是_____ ,最活泼的非金属元素是____ ,最不活泼的元素是_____ ,非金属气态氢化物最稳定的是______ ,原子半径最大的是______ ,可做半导体材料的是______ 。(填元素符号)
(2)在①~⑩元素中,⑧的氢化物是_____ ,最高价氧化物对应的水化物中碱性最强的是______ ,呈两性的是_____ 。写出在水溶液中三者之间相互反应的离子方程式:____ ,____ ,_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
4 | ⑩ |
(2)在①~⑩元素中,⑧的氢化物是
更新时间:2020-11-05 18:10:12
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】A、B、C、D、E都为短周期元素,A是相对原子质量最小的元素;B的+1价阳离子和C的﹣1价阴离子都与氖原子具有相同的电子层结构;D在C的下一周期,可与B形成BD型离子化合物;E和C为同一周期元素,其最高价氧化物对应的水化物为一种强酸。请根据以上信息回答下列问题:
(1)B元素在元素周期表中的位置是______________ ;
(2)画出C元素的原子结构示意图______ ;
(3)与E的氢化物分子所含电子总数相等的分子是______ (举一例,填化学式,);
(4)A与D形成的化合物中含有化学键的类型是_____ 。
(1)B元素在元素周期表中的位置是
(2)画出C元素的原子结构示意图
(3)与E的氢化物分子所含电子总数相等的分子是
(4)A与D形成的化合物中含有化学键的类型是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】有质子数均小于18的X、Y、Z三种元素, 离子的电子层结构与氖原子的相同,Y元素原子核内无中子,Z元素原子的最外层电子数是内层电子数的3倍。
离子的电子层结构与氖原子的相同,Y元素原子核内无中子,Z元素原子的最外层电子数是内层电子数的3倍。
(1)画出 离子的结构示意图
离子的结构示意图_______________________ ;
(2)写出Z元素的元素符号______________ ;
(3)写出X、Y、Z三种元素组成的化合物在水中的电离方程式_______________________ 。
 离子的电子层结构与氖原子的相同,Y元素原子核内无中子,Z元素原子的最外层电子数是内层电子数的3倍。
离子的电子层结构与氖原子的相同,Y元素原子核内无中子,Z元素原子的最外层电子数是内层电子数的3倍。(1)画出
 离子的结构示意图
离子的结构示意图(2)写出Z元素的元素符号
(3)写出X、Y、Z三种元素组成的化合物在水中的电离方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】如表列出了①~⑥六种元素在周期表中的位置:
请按要求回答下列问题:
(1)元素②、⑤形成的简单单核离子半径大小关系为____ (用元素符号表示)。
(2)表中所给元素非金属性最强的元素的气态氢化物的水溶液常用于刻蚀玻璃,请写出该反应的化学方程式___ 。
(3)上表中所涉及金属元素的最高价氧化物水化物的碱性大小关系___ (用化学式表示)。
(4)元素②、④形成原子个数比为1:1的化合物的电子式为____ 。
(5)①的简单氢化物可与⑥的单质作用产生白烟和一种单质,写出反应的方程式____ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ |
请按要求回答下列问题:
(1)元素②、⑤形成的简单单核离子半径大小关系为
(2)表中所给元素非金属性最强的元素的气态氢化物的水溶液常用于刻蚀玻璃,请写出该反应的化学方程式
(3)上表中所涉及金属元素的最高价氧化物水化物的碱性大小关系
(4)元素②、④形成原子个数比为1:1的化合物的电子式为
(5)①的简单氢化物可与⑥的单质作用产生白烟和一种单质,写出反应的方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】元素周期律和周期表是我们研究、预测物质性质的重要工具。下表是元素周期表中前四周期的5种元素的相关信息。
回答下列问题:
(1)D在元素周期表中的位置是___________ 。
(2)BH4的分子结构模型为___________ ,其气态氢化物的稳定性BH4___________ HD(填写“大于”“小于”或“等于”)。
(3)少量E的单质加入水中剧烈反应,反应的化学方程式是___________ ;将一块C单质加入上述形成的强碱溶液中反应的离子方程式是___________ ;元素A、E的最高价氧化物对应的水化物中,碱性更强的物质是___________ (填写化学式)。
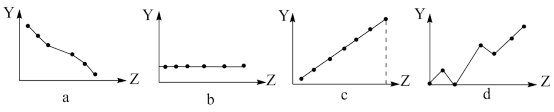
(4)下列曲线分别表示元素的某种性质(用Y表示)与核电荷数(用Z表示)的关系。请将正确曲线的图象标号填入相应的空格中:
第IIA族元素的最外层电子数____ ,第三周期主族元素的最高正化合价___ 。
| 元素 | 元素性质或原子结构 |
| A | 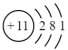 |
| B | B能形成多种单质,其中一种单质是硬度最大的物质 |
| C | 地壳中含量最高的金属元素,其合金可用于制造飞机外壳 |
| D | D的单质是一种黄绿色气体 |
| E | 用E的碳酸盐做焰色试验时火焰为紫色(透过蓝色钴玻璃片) |
(1)D在元素周期表中的位置是
(2)BH4的分子结构模型为
(3)少量E的单质加入水中剧烈反应,反应的化学方程式是
(4)下列曲线分别表示元素的某种性质(用Y表示)与核电荷数(用Z表示)的关系。请将正确曲线的图象标号填入相应的空格中:

第IIA族元素的最外层电子数
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。表中列出了a~g 7种元素在周期表中的位置。
(1)a的元素符号是_______ 。
(2)写出c单质与b的最高价氧化物水化物反应的离子方程式_______ 。
(3)d、e的最高价氧化物对应的水化物中,酸性较强的是_______ 。(填化学式)
(4)已知硒(Se)与d同主族,且位于d下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是_______ 。
① 其单质在常温下呈固态
② SeO2既有氧化性又有还原性
③ 最高价氧化物对应的水化物的化学式为H2SeO3
④ 非金属性比e元素的强
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | a | |||||||
| 3 | b | c | d | e |
(2)写出c单质与b的最高价氧化物水化物反应的离子方程式
(3)d、e的最高价氧化物对应的水化物中,酸性较强的是
(4)已知硒(Se)与d同主族,且位于d下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
① 其单质在常温下呈固态
② SeO2既有氧化性又有还原性
③ 最高价氧化物对应的水化物的化学式为H2SeO3
④ 非金属性比e元素的强
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】下表是元素周期表的一部分,用化学用语回答下列问题:
(1)画出元素⑨阴离子的结构示意图:______ ,⑧正下方的元素原子序数为____
(2)③⑤⑧的原子半径由小到大的顺序为________ (填元素符号)。
(3)⑤和⑦的最高价氧化物对应水化物的碱性强弱为___________ (填化学式)。
(4)③⑤两种元素的原子按1∶1组成的常见化合物的电子式为____________________ 。
(5)用电子式表示⑥和⑨形成的化合物的过程:____________________________________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
| 4 |
(1)画出元素⑨阴离子的结构示意图:
(2)③⑤⑧的原子半径由小到大的顺序为
(3)⑤和⑦的最高价氧化物对应水化物的碱性强弱为
(4)③⑤两种元素的原子按1∶1组成的常见化合物的电子式为
(5)用电子式表示⑥和⑨形成的化合物的过程:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
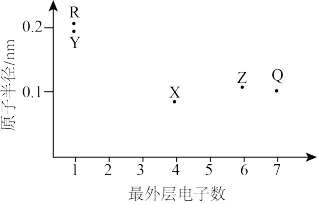
【推荐2】元素X、Y、Z、Q、R的原子序数依次增大且小于20,其原子半径和最外层电子数之间的关系如图所示。
(1)Z离子的结构示意图是____ 。
(2)Q元素在周期表中位于第____ 周期____ 族;关于Q所在主族的单质及化合物的叙述错误的是____ (填标号)。
A.从上到下,单质颜色越来越深,熔、沸点越来越高
B.单质均可与水发生反应生成两种酸
C.单质均具有强氧化性,能将Fe氧化至Fe3+
D.氢化物均易溶于水,且均为强酸
(3)X、Z、Q三种元素的最高价氧化物对应的水化物酸性由强到弱的顺序是____ (填化学式)。
(4)Y与Q可以形成_____ (填“共价”或“离子”)化合物,用电子式表示其形成过程为____ 。
(5)Y与R金属性较强的是____ (填元素符号),请从原子结构的角度解释原因____ 。

(1)Z离子的结构示意图是
(2)Q元素在周期表中位于第
A.从上到下,单质颜色越来越深,熔、沸点越来越高
B.单质均可与水发生反应生成两种酸
C.单质均具有强氧化性,能将Fe氧化至Fe3+
D.氢化物均易溶于水,且均为强酸
(3)X、Z、Q三种元素的最高价氧化物对应的水化物酸性由强到弱的顺序是
(4)Y与Q可以形成
(5)Y与R金属性较强的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】元素周期表、元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了a~g 7种元素在周期表中的位置。
(1)a的元素符号是_____ 。
(2)b、c的最高价氧化物对应的水化物(氢氧化物)中,碱性较弱的是_____ (填化学式)。
(3)非金属性e强于g,用原子结构解释原因_____________________________ ,得电子能力e大于g。
(4)下列对f及其化合物的推断中,正确的是_____ (填字母)。
A.f的最高化合价为+6价
B.f的氢化物的稳定性弱于d的氢化物的稳定性
C.f的最高价氧化物对应的水化物属于碱
(5)单质c与b的最高价氧化物的水化物反应的化学方程式为___________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | a | |||||||
3 | b | c | d | e | ||||
4 | f | g |
(2)b、c的最高价氧化物对应的水化物(氢氧化物)中,碱性较弱的是
(3)非金属性e强于g,用原子结构解释原因
(4)下列对f及其化合物的推断中,正确的是
A.f的最高化合价为+6价
B.f的氢化物的稳定性弱于d的氢化物的稳定性
C.f的最高价氧化物对应的水化物属于碱
(5)单质c与b的最高价氧化物的水化物反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是现行中学化学教科书中元素周期表的一部分,表中的每个编号表示一种元素,请根据要求回答问题。
(1)在这些元素中,最活泼的金属元素是_____ ,②表示的元素是_____ (填元素符号);
(2)①、⑤两种元素的原子半径大小为①_____ ⑤(填“< ”或“>”);
(3)③、④两种元素的金属性强弱顺序为:③_____ ④(填“< ”或“>”);
(4)写出⑥最高价氧化物的水化物的化学式_____ 。
(5)写出④单质与氢氧化钠溶液反应的化学方程式:_____ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||
(2)①、⑤两种元素的原子半径大小为①
(3)③、④两种元素的金属性强弱顺序为:③
(4)写出⑥最高价氧化物的水化物的化学式
(5)写出④单质与氢氧化钠溶液反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A~G是原子序数递增的短周期主族元素,最高正价或最低负价与原子序数的关系如图所示。
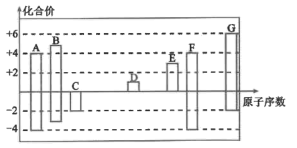
回答下列问题:
(1)G元素在周期表中的位置是_____ ,B元素常见单质的电子式是_____ 。
(2)下列叙述不正确的是______ (填字母)。
a.A元素的一种单质可用作电池的电极
b.B元素的一种氢化物可用作制冷剂
c.E元素的氢氧化物可用作消毒剂
(3)D2C2中所含的化学键类型有_______ ,D2C2与水反应的离子方程式_______ 。
(4)写出A的单质与B元素的最高价氧化物对应水化物的浓溶液反应的化学方程式_______ 。

回答下列问题:
(1)G元素在周期表中的位置是
(2)下列叙述不正确的是
a.A元素的一种单质可用作电池的电极
b.B元素的一种氢化物可用作制冷剂
c.E元素的氢氧化物可用作消毒剂
(3)D2C2中所含的化学键类型有
(4)写出A的单质与B元素的最高价氧化物对应水化物的浓溶液反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】元素周期表与元素周期律在化学学习研究中有很重要的作用。如表是元素周期表的一部分,回答下列问题(用相关化学用语回答)。
(1)③、⑥、⑨的简单离子半径由小到大的顺序___________ (用离子符号表示)。
(2)写出元素⑪的单质与水反应的化学方程式___________ 。
(3)元素③、④、⑩的简单气态氢化物的稳定性最强的是___________ (用化学式表示)。
(4)配制0.1mol/L500mL元素⑤的氢氧化物溶液,需用托盘天平称取该氢氧化物的质量是___________ g。
(5)⑤2⑨③3在加热条件下发生分解反应生成两种盐,其中氧化产物与还原产物的物质的量之比为3:1,该反应的化学方程式:___________ 。
(6)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是___________(填字母)。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
| 四 | ⑪ |
(2)写出元素⑪的单质与水反应的化学方程式
(3)元素③、④、⑩的简单气态氢化物的稳定性最强的是
(4)配制0.1mol/L500mL元素⑤的氢氧化物溶液,需用托盘天平称取该氢氧化物的质量是
(5)⑤2⑨③3在加热条件下发生分解反应生成两种盐,其中氧化产物与还原产物的物质的量之比为3:1,该反应的化学方程式:
(6)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是___________(填字母)。
| A.比较这两种元素单质的沸点 |
| B.比较这两种元素单质与氢气化合的难易 |
| C.比较这两种元素的最高价氧化物对应水化物的酸性强弱 |
| D.比较这两种元素的单质与酸或碱反应的难易程度 |
您最近一年使用:0次