铂(78Pt)被誉为“第一重要的高技术金属”,因独特的物理化学性质,被广泛应用于汽车、石油化工、电气电子等现代工业中。水合肼还原精炼法是铂精炼的方法之一,流程如下:

已知:①氯铂酸铵[(NH4)2PtCl6],黄色,难溶于水,易溶于盐酸并生成H2PtCl6;
②氯亚铂酸铵[(NH4)2PtCl4],红色,易溶于水。
回答下列问题:
(1)铂位于周期表中第______ 周期,试写出一种金属铂在中学化学中的应用____________
(2)工业原料粗氯铂酸铵中含有大量氯化铵等可溶性的盐,在实验室中预处理时,需将样品溶解过滤后洗涤,洗涤沉淀方法是____________
(3)在还原溶解中观察到的现象:__________
(4)氧化沉淀过程的反应方程式为:___________
(5)有研究表明,氯铂酸铵制取金属铂,除了煅烧外,也可将其溶解于盐酸中,加入Zn,得到产品,反应过程有Zn+2HCl = ZnCl2+H2↑;_________
(6)水合肼还原精炼法在溶解时的固液比、溶液的酸度(盐酸浓度)、反应时间等对于精炼铂的产率,均有较大的影响。在不同酸度下达到较高产率所需时间,以及不同固液比在最佳酸度下反应时间与产率关系如图所示,由此可得最佳的反应条件是_________


已知:①氯铂酸铵[(NH4)2PtCl6],黄色,难溶于水,易溶于盐酸并生成H2PtCl6;
②氯亚铂酸铵[(NH4)2PtCl4],红色,易溶于水。
回答下列问题:
(1)铂位于周期表中第
(2)工业原料粗氯铂酸铵中含有大量氯化铵等可溶性的盐,在实验室中预处理时,需将样品溶解过滤后洗涤,洗涤沉淀方法是
(3)在还原溶解中观察到的现象:
(4)氧化沉淀过程的反应方程式为:
(5)有研究表明,氯铂酸铵制取金属铂,除了煅烧外,也可将其溶解于盐酸中,加入Zn,得到产品,反应过程有Zn+2HCl = ZnCl2+H2↑;
(6)水合肼还原精炼法在溶解时的固液比、溶液的酸度(盐酸浓度)、反应时间等对于精炼铂的产率,均有较大的影响。在不同酸度下达到较高产率所需时间,以及不同固液比在最佳酸度下反应时间与产率关系如图所示,由此可得最佳的反应条件是

更新时间:2020-11-06 13:44:04
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】过氧化钙 是一种微溶于水的白色或淡黄色固体,在加热时可分解生成氧气,主要用作增氧剂、杀菌剂等。
是一种微溶于水的白色或淡黄色固体,在加热时可分解生成氧气,主要用作增氧剂、杀菌剂等。
(1)过氧化钙投入养鱼池,可持续供氧数十小时,该过程中发生反应的化学方程式为________ 。
(2)在碱性条件下制备 的装置如下图所示。
的装置如下图所示。

三颈瓶中发生的反应为: ,反应温度不能过高的原因有:温度过高,氨水易挥发、
,反应温度不能过高的原因有:温度过高,氨水易挥发、___________ 。
(3)实验小组测定渔农使用的过氧化钙增氧剂(杂质中不含钙元素)含量的方法如下:
方法1:

①滴加的 溶液须过量,目的是
溶液须过量,目的是___________ ;能表明 溶液已过量的实验操作和现象是
溶液已过量的实验操作和现象是___________ 。
方法2:准确称取 无水过氧化钙样品于锥形瓶中,加入
无水过氧化钙样品于锥形瓶中,加入 水和
水和 ,振荡使之溶解,立即用
,振荡使之溶解,立即用 的
的 溶液滴定至溶液呈微红色且半分钟内不褪色为止,重复实验3次,平均消耗
溶液滴定至溶液呈微红色且半分钟内不褪色为止,重复实验3次,平均消耗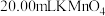 溶液。
溶液。
(已知: ,未配平)
,未配平)
②产品中 的质量分数为
的质量分数为___________ 。(请写出计算过程)
④为探索过氧化钙-亚铁组合工艺处理高藻水的效能,采用了不同浓度的过氧化钙和硫酸亚铁对高藻水进行处理,并测定藻细胞去除率,评估处理效果如图所示。则最佳过氧化钙-亚铁的组合为___________ (填序号)。

A. 和
和
B. 和
和
C. 和
和
D. 和
和
 是一种微溶于水的白色或淡黄色固体,在加热时可分解生成氧气,主要用作增氧剂、杀菌剂等。
是一种微溶于水的白色或淡黄色固体,在加热时可分解生成氧气,主要用作增氧剂、杀菌剂等。(1)过氧化钙投入养鱼池,可持续供氧数十小时,该过程中发生反应的化学方程式为
(2)在碱性条件下制备
 的装置如下图所示。
的装置如下图所示。
三颈瓶中发生的反应为:
 ,反应温度不能过高的原因有:温度过高,氨水易挥发、
,反应温度不能过高的原因有:温度过高,氨水易挥发、(3)实验小组测定渔农使用的过氧化钙增氧剂(杂质中不含钙元素)含量的方法如下:
方法1:

①滴加的
 溶液须过量,目的是
溶液须过量,目的是 溶液已过量的实验操作和现象是
溶液已过量的实验操作和现象是方法2:准确称取
 无水过氧化钙样品于锥形瓶中,加入
无水过氧化钙样品于锥形瓶中,加入 水和
水和 ,振荡使之溶解,立即用
,振荡使之溶解,立即用 的
的 溶液滴定至溶液呈微红色且半分钟内不褪色为止,重复实验3次,平均消耗
溶液滴定至溶液呈微红色且半分钟内不褪色为止,重复实验3次,平均消耗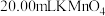 溶液。
溶液。(已知:
 ,未配平)
,未配平)②产品中
 的质量分数为
的质量分数为④为探索过氧化钙-亚铁组合工艺处理高藻水的效能,采用了不同浓度的过氧化钙和硫酸亚铁对高藻水进行处理,并测定藻细胞去除率,评估处理效果如图所示。则最佳过氧化钙-亚铁的组合为

A.
 和
和
B.
 和
和
C.
 和
和
D.
 和
和
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某次化学实验后,回收的废液中存在 。
。
(1)确定废液中存在 的方法为
的方法为______ 。
(2)现从废液中除去这些离子且回收铜、银两种金属。流程如图:

已知: 。
。
①试剂 是
是______ ,试剂是
______ 。
②滤液2中的金属阳离子有______ 。
③固体3中加入试剂 发生反应的离子方程式为
发生反应的离子方程式为______ 。
④流程中多次用到过滤,用到的仪器有铁架台、烧杯、还有______ 。
 。
。(1)确定废液中存在
 的方法为
的方法为(2)现从废液中除去这些离子且回收铜、银两种金属。流程如图:

已知:
 。
。①试剂
 是
是
②滤液2中的金属阳离子有
③固体3中加入试剂
 发生反应的离子方程式为
发生反应的离子方程式为④流程中多次用到过滤,用到的仪器有铁架台、烧杯、还有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】从工业废料中提取有用物质对资源的开发和利用有着十分重要的意义。现代工业开发了用“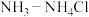 水溶液”浸出氧化锌烟灰(主要成分为
水溶液”浸出氧化锌烟灰(主要成分为 、
、 、
、 和
和 )制取高纯锌的工艺流程如下图所示:
)制取高纯锌的工艺流程如下图所示:

已知:①“溶浸”过程控制温度在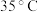 左右。
左右。
②浸出液中含 、
、 、
、 ,且存在
,且存在 (
( 为
为 或
或 )。
)。
(1) 在元素周期表中的位置是
在元素周期表中的位置是___________ 。
(2)“滤渣3”的主要成分为___________ 。
(3)为提高浸出速率,写出一种切合实际的措施___________ 。
(4)①“溶浸”过程需控制温度在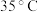 左右,原因是
左右,原因是___________ 。
②“溶浸”过程中,氧化铜发生反应的离子方程式为___________ 。
(5)“氧化除杂”的目的是将 转化为
转化为 胶体,再经吸附聚沉除去,溶液始终接近中性,该反应的离子方程式是
胶体,再经吸附聚沉除去,溶液始终接近中性,该反应的离子方程式是___________ 。
(6)“电解残留液”再生后重复利用,再生过程使用的 为
为___________ (填化学式)。
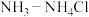 水溶液”浸出氧化锌烟灰(主要成分为
水溶液”浸出氧化锌烟灰(主要成分为 、
、 、
、 和
和 )制取高纯锌的工艺流程如下图所示:
)制取高纯锌的工艺流程如下图所示:
已知:①“溶浸”过程控制温度在
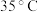 左右。
左右。②浸出液中含
 、
、 、
、 ,且存在
,且存在 (
( 为
为 或
或 )。
)。(1)
 在元素周期表中的位置是
在元素周期表中的位置是(2)“滤渣3”的主要成分为
(3)为提高浸出速率,写出一种切合实际的措施
(4)①“溶浸”过程需控制温度在
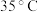 左右,原因是
左右,原因是②“溶浸”过程中,氧化铜发生反应的离子方程式为
(5)“氧化除杂”的目的是将
 转化为
转化为 胶体,再经吸附聚沉除去,溶液始终接近中性,该反应的离子方程式是
胶体,再经吸附聚沉除去,溶液始终接近中性,该反应的离子方程式是(6)“电解残留液”再生后重复利用,再生过程使用的
 为
为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】随着科技的进步,合理利用资源、保护环境成为当今社会关注的焦点。甲胺铅碘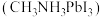 用作全固态钙钛矿敏化太阳能电池的敏化剂,可由
用作全固态钙钛矿敏化太阳能电池的敏化剂,可由 、
、 及HI为原料合成,回答下列问题:
及HI为原料合成,回答下列问题:
(1)制取甲胺的反应为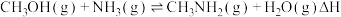 。已知该反应中相关化学键的键能数据如下:
。已知该反应中相关化学键的键能数据如下:
则该反应的
_______  。
。
(2)上述反应中所需的甲醇工业上利用水煤气合成,反应为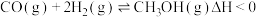 。在一定条件下,将
。在一定条件下,将 和
和 通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,
通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时, 的体积分数
的体积分数 变化趋势如图所示:
变化趋势如图所示:

①平衡时,M点 的体积分数为
的体积分数为 ,则CO的转化率为
,则CO的转化率为_______ 。
②X轴上a点的数值比b点_______ (填“大”或“小”)。某同学认为上图中Y轴表示温度,你认为他判断的理由是_______ 。
(3)工业上可采用 的方法来制取高纯度的CO和
的方法来制取高纯度的CO和 。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用
。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用 标注。甲醇
标注。甲醇 脱氢反应的第一步历程,有两种可能方式:
脱氢反应的第一步历程,有两种可能方式:
方式A: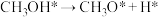
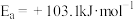
方式B: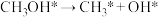
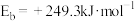
由活化能E值推测,甲醇裂解过程主要历经的方式应为_______ (填A、B)。如图为计算机模拟的各步反应的能量变化示意图:
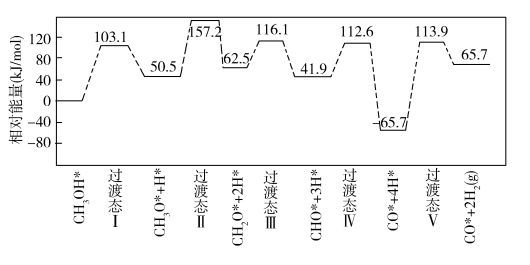
该历程中,放热最多的步骤的化学方程式为_______ 。
(4)用NaHS作污水处理的沉淀剂,可以处理工业废水中的 。已知:
。已知: 时,
时, 的电离平衡常数
的电离平衡常数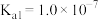 ,
,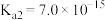 ,CuS的溶度积为
,CuS的溶度积为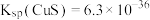 。反应
。反应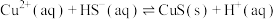 的平衡常数
的平衡常数
_______ (结果保留1位小数)。
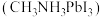 用作全固态钙钛矿敏化太阳能电池的敏化剂,可由
用作全固态钙钛矿敏化太阳能电池的敏化剂,可由 、
、 及HI为原料合成,回答下列问题:
及HI为原料合成,回答下列问题:(1)制取甲胺的反应为
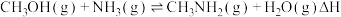 。已知该反应中相关化学键的键能数据如下:
。已知该反应中相关化学键的键能数据如下:| 共价键 | 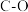 |  |  | 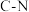 |  |
键能 | 351 | 463 | 393 | 293 | 414 |
则该反应的

 。
。(2)上述反应中所需的甲醇工业上利用水煤气合成,反应为
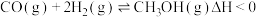 。在一定条件下,将
。在一定条件下,将 和
和 通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,
通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时, 的体积分数
的体积分数 变化趋势如图所示:
变化趋势如图所示:
①平衡时,M点
 的体积分数为
的体积分数为 ,则CO的转化率为
,则CO的转化率为②X轴上a点的数值比b点
(3)工业上可采用
 的方法来制取高纯度的CO和
的方法来制取高纯度的CO和 。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用
。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用 标注。甲醇
标注。甲醇 脱氢反应的第一步历程,有两种可能方式:
脱氢反应的第一步历程,有两种可能方式:方式A:
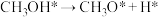
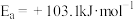
方式B:
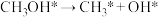
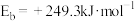
由活化能E值推测,甲醇裂解过程主要历经的方式应为

该历程中,放热最多的步骤的化学方程式为
(4)用NaHS作污水处理的沉淀剂,可以处理工业废水中的
 。已知:
。已知: 时,
时, 的电离平衡常数
的电离平衡常数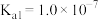 ,
,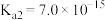 ,CuS的溶度积为
,CuS的溶度积为 。反应
。反应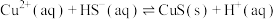 的平衡常数
的平衡常数
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。回答下列问题:
已知:2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
C(s)+O2(g)=CO2(g) ∆H=-393.5 kJ/mol
N2(g)+O2(g)=2NO(g) ΔH= +181 kJ/mol
(1)若某反应的平衡常数表达式为K=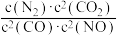 ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:_______ ;下列措施能够增大此反应中NO的转化率的是(填字母代号)_______ 。
a.增大容器压强 b.升高温度 c.使用优质催化剂 d.增大CO的浓度
(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,反应为C(s)+2NO(g) ⇌N2(g)+CO2(g),NO和N2的物质的量变化如表所示。
①0~5min内,以CO2表示的该反应速率v(CO2)=_______ ,该条件下的平衡常数K=_______ 。T1温度达平衡时NO的转化率α=_______ 。
②第15 min后,温度调整到T2,数据变化如上表所示,则T1_______ T2(填“>”“<”或“=”)。
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,则此时反应_______ 移动(填“正向”“逆向”或“不”);
已知:2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
C(s)+O2(g)=CO2(g) ∆H=-393.5 kJ/mol
N2(g)+O2(g)=2NO(g) ΔH= +181 kJ/mol
(1)若某反应的平衡常数表达式为K=
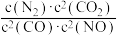 ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:a.增大容器压强 b.升高温度 c.使用优质催化剂 d.增大CO的浓度
(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,反应为C(s)+2NO(g) ⇌N2(g)+CO2(g),NO和N2的物质的量变化如表所示。
| 物质的量/mol | T1/℃ | T2/℃ | |||||
| 0 | 5 min | 10 min | 15 min | 20 min | 25 min | 30 min | |
| NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
| N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
①0~5min内,以CO2表示的该反应速率v(CO2)=
②第15 min后,温度调整到T2,数据变化如上表所示,则T1
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,则此时反应
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】随着全球气候问题的日益严重,人们需要更有力的政策来逐步淘汰化石燃料的使用。 的综合利用是解决温室问题的有效途径。
的综合利用是解决温室问题的有效途径。
(1)一种途径是用 转化为乙醇实现碳循环。如:
转化为乙醇实现碳循环。如:
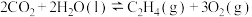

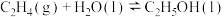

则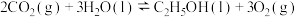

_______  。
。
(2)用 转化为甲醇和水蒸气也可实现碳循环:
转化为甲醇和水蒸气也可实现碳循环: ,一定条件下,往
,一定条件下,往 恒容密闭容器中充入
恒容密闭容器中充入 和
和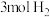 ,在不同催化剂作用下发生反应Ⅰ与反应Ⅱ,相同时间内
,在不同催化剂作用下发生反应Ⅰ与反应Ⅱ,相同时间内 的转化率随温度变化如图所示:
的转化率随温度变化如图所示:

①催化剂效果最佳的反应是_______ (填“反应Ⅰ”、“反应Ⅱ”)。
②a点的转化率比c点高的原因是_______ 。
③已知 温度下反应达到平衡时容器中的总压为
温度下反应达到平衡时容器中的总压为 ,若该反应的速率方程v正=kp(CO2)·p(H2O)-1,式中k为常数,p为气体分压,气体分压=气体总压×气体的物质的量分数。则c点时该反应的速率v=
,若该反应的速率方程v正=kp(CO2)·p(H2O)-1,式中k为常数,p为气体分压,气体分压=气体总压×气体的物质的量分数。则c点时该反应的速率v=_______ (用含k的式子表示),该反应的平衡常数
_______ (用平衡分压代替平衡浓度计算,列出计算式即可)。
(3)将 催化加氢制取乙烯是实现碳循环的另一种途径,研究表明催化加氢过程中往往伴随着副反应,生成
催化加氢制取乙烯是实现碳循环的另一种途径,研究表明催化加氢过程中往往伴随着副反应,生成 、
、 等低碳化合物,若
等低碳化合物,若 、
、 、
、 的物质的量之比为
的物质的量之比为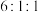 ,则
,则 催化加氢合成乙烯的选择性=
催化加氢合成乙烯的选择性=_______ (注: 的选择性=
的选择性= ×100%),在一定的温度和压强下,为了提高反应速率和乙烯的选择性,应当采取的措施为
×100%),在一定的温度和压强下,为了提高反应速率和乙烯的选择性,应当采取的措施为_______ 。
 的综合利用是解决温室问题的有效途径。
的综合利用是解决温室问题的有效途径。(1)一种途径是用
 转化为乙醇实现碳循环。如:
转化为乙醇实现碳循环。如: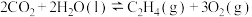

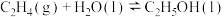

则
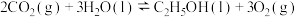

 。
。(2)用
 转化为甲醇和水蒸气也可实现碳循环:
转化为甲醇和水蒸气也可实现碳循环: ,一定条件下,往
,一定条件下,往 恒容密闭容器中充入
恒容密闭容器中充入 和
和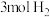 ,在不同催化剂作用下发生反应Ⅰ与反应Ⅱ,相同时间内
,在不同催化剂作用下发生反应Ⅰ与反应Ⅱ,相同时间内 的转化率随温度变化如图所示:
的转化率随温度变化如图所示:
①催化剂效果最佳的反应是
②a点的转化率比c点高的原因是

③已知
 温度下反应达到平衡时容器中的总压为
温度下反应达到平衡时容器中的总压为 ,若该反应的速率方程v正=kp(CO2)·p(H2O)-1,式中k为常数,p为气体分压,气体分压=气体总压×气体的物质的量分数。则c点时该反应的速率v=
,若该反应的速率方程v正=kp(CO2)·p(H2O)-1,式中k为常数,p为气体分压,气体分压=气体总压×气体的物质的量分数。则c点时该反应的速率v=
(3)将
 催化加氢制取乙烯是实现碳循环的另一种途径,研究表明催化加氢过程中往往伴随着副反应,生成
催化加氢制取乙烯是实现碳循环的另一种途径,研究表明催化加氢过程中往往伴随着副反应,生成 、
、 等低碳化合物,若
等低碳化合物,若 、
、 、
、 的物质的量之比为
的物质的量之比为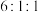 ,则
,则 催化加氢合成乙烯的选择性=
催化加氢合成乙烯的选择性= 的选择性=
的选择性= ×100%),在一定的温度和压强下,为了提高反应速率和乙烯的选择性,应当采取的措施为
×100%),在一定的温度和压强下,为了提高反应速率和乙烯的选择性,应当采取的措施为
您最近一年使用:0次



