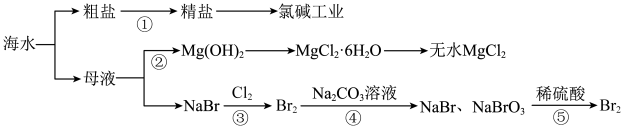
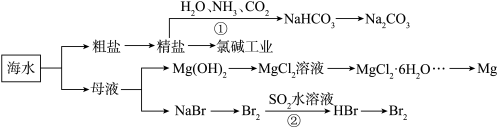
海洋中有丰富的资源,下图为海水利用的部分过程。下列有关说法不正确的是( )


| A.由反应①可知:相同温度下,NaHCO3的溶解度小于NaCl |
| B.工业上通过电解饱和MgCl2溶液制取金属镁 |
C.反应②的离子方程式为:Br2+SO2+2H2O=SO +2Br—+4H+ +2Br—+4H+ |
D.粗盐中含有的Mg2+、SO 等杂质离子,可通过依次加入BaCl2溶液、NaOH溶液、盐酸等 等杂质离子,可通过依次加入BaCl2溶液、NaOH溶液、盐酸等 |
20-21高三上·福建龙岩·期中 查看更多[2]
福建省龙岩市“长汀、连城、上杭、武平、永定、漳平”六县(市区)一中2021届高三上学期期中联考化学试题(已下线)专题14 海水资源的综合利用 环境保护与绿色化学 (限时精炼)-2022年高三毕业班化学常考点归纳与变式演练
更新时间:2020-11-11 19:49:32
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】一种绿色回收分银渣中的银的工艺流程如图:
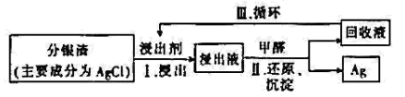
已知:浸出剂为 ,“浸出”时发生的主要反应为
,“浸出”时发生的主要反应为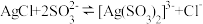 。
。
下列说法错误的是

已知:浸出剂为
 ,“浸出”时发生的主要反应为
,“浸出”时发生的主要反应为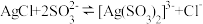 。
。下列说法错误的是
A.用 也能浸取分银渣中的Ag 也能浸取分银渣中的Ag |
| B.“浸出”过程中,浸取时间越长越好 |
| C.“还原”时,被还原的元素与被氧化的元素的物质的量之比为1∶1 |
| D.分离出Ag的操作中需要用到的硅酸盐材质的仪器有烧杯、玻璃棒、漏斗 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列除杂方案错误的是
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 |
| A | FeCl3(aq) | Al3+(aq) | NaOH溶液、盐酸 |
| B | AlCl3(aq) | Cu2+ | Al粉 |
| C | NH4Cl(aq) | Fe3+(aq) | NaOH溶液 |
| D | FeCl3(aq) | Cu2+ | Fe粉 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
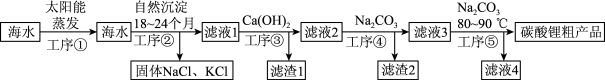
【推荐1】Li2CO3可用于制陶瓷、药物、催化剂等,微溶于水,在冷水中溶解度较热水中大,不溶于醇。利用海水资源(主要含Na+、Cl-,少量的Mg2+、K+、Li+、Ca2+、 )制备碳酸锂的一种工艺如图所示,下列说法错误的是
)制备碳酸锂的一种工艺如图所示,下列说法错误的是
 )制备碳酸锂的一种工艺如图所示,下列说法错误的是
)制备碳酸锂的一种工艺如图所示,下列说法错误的是
| A.工序③和工序④顺序可互换 |
| B.选择温度为80~90℃,可降低碳酸锂在水中的溶解度,提高产率 |
| C.用乙醇洗涤粗产品可起到快速干燥的效果 |
| D.利用过滤可分离NaCl和KCl |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】工业上用活性炭吸附海带提碘后废水中的I-制取I2,其流程如图:
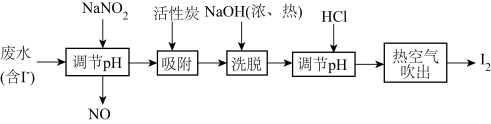
下列说法错误的是

下列说法错误的是
| A.NaNO2氧化I-时使溶液pH变小 |
| B.活性炭吸附是为了净化水溶液 |
| C.I2与NaOH(浓、热)反应的化学方程式:3I2+6NaOH(浓、热)=5NaI+NaIO3+3H2O |
| D.热空气能吹出I2,是因为I2在水中溶解度小、易升华 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】根据如图海水综合利用的工业流程图,判断下列说法正确的是
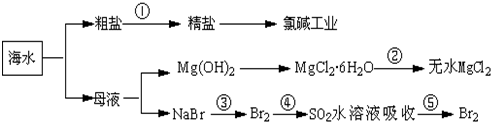

| A.除去粗盐中杂质Mg2+、SO42-、Ca2+,加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 |
| B.从能量转换角度看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程 |
| C.从第③步到第⑤步的目的是为了浓缩 |
| D.在过程④中SO2被氧化 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】海水晒盐可以得到粗盐,粗盐中含有泥沙等不溶性杂质。可能含MgCl2、CaCl2和Na2SO4等可溶性杂质,某同学设计如图实验方案提纯粗盐,同时验证可溶性杂质是否存在。对该过程的认识中,正确的是
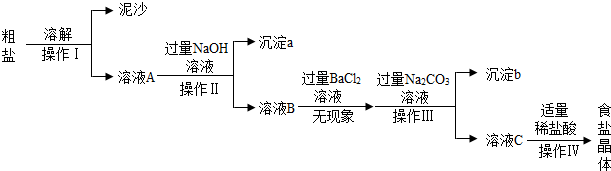

| A.操作I中需要进行搅拌,目的是提高氯化钠的溶解度 |
| B.NaOH溶液和Na2CO3溶液的顺序可以互换 |
| C.沉淀b中共有三种物质 |
| D.操作IV中加入盐酸至溶液呈中性或微酸性 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】海洋中部分化学资源的利用,如图所示,下列说法错误 的是
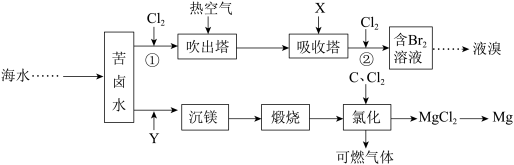

A.步骤①、②利用了 的氧化性,热空气吹出利用了溴的挥发性 的氧化性,热空气吹出利用了溴的挥发性 |
B.物质X常选用 ,Y常选用烧碱 ,Y常选用烧碱 |
| C.工业上常用热还原法冶炼金属镁 |
D.“氯化”过程中发生的反应为 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】溴乙烷是无色油状液体,是制造巴比妥的原料,工业上可用海水制备溴乙烷,部分工艺流程如图:
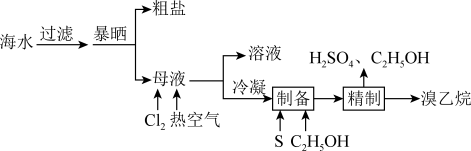
下列说法错误的是

下列说法错误的是
A.粗盐(含 、 、 、 、 杂质离子)提纯时,加入沉淀剂的顺序可以是 杂质离子)提纯时,加入沉淀剂的顺序可以是 、 、 和 和 |
| B.向“母液”中通入热空气,利用溴的易挥发性,将溴吹出 |
C.“制备”时氧化剂和还原剂的物质的量之比为 |
| D.“精制”时所用的玻璃仪器有分液漏斗、烧杯 |
您最近一年使用:0次

 、
、 、
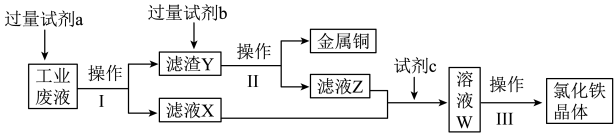
、 )中回收铜并制备氯化铁晶体,设计流程如图。下列说过法正确的是
)中回收铜并制备氯化铁晶体,设计流程如图。下列说过法正确的是