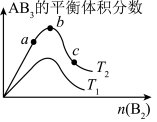
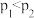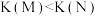某化学科研小组研究在其他条件不变时,改变某一条件对反应 的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据图像得出的结论正确的是()
的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据图像得出的结论正确的是()
①正反应一定是放热反应
②达到平衡时 的转化率大小为
的转化率大小为
③若 ,则正反应一定是吸热反应
,则正反应一定是吸热反应
④b点时,平衡体系中A、B原子数之比接近1:3
 的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据图像得出的结论正确的是()
的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据图像得出的结论正确的是()
①正反应一定是放热反应
②达到平衡时
 的转化率大小为
的转化率大小为
③若
 ,则正反应一定是吸热反应
,则正反应一定是吸热反应④b点时,平衡体系中A、B原子数之比接近1:3
| A.①② | B.①③ | C.②④ | D.③④ |
更新时间:2020/10/10 23:59:12
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学科研小组在其他条件不变时,改变某一条件对反应[可用aA(g)+bB(g) cC(g)表示]的化学平衡的影响,得到如图图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。根据图像,下列判断正确的是()
cC(g)表示]的化学平衡的影响,得到如图图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。根据图像,下列判断正确的是()
 cC(g)表示]的化学平衡的影响,得到如图图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。根据图像,下列判断正确的是()
cC(g)表示]的化学平衡的影响,得到如图图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。根据图像,下列判断正确的是()A.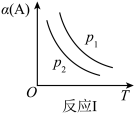 如图反应:若p1>p2,则此反应只能在高温下自发进行 如图反应:若p1>p2,则此反应只能在高温下自发进行 |
B.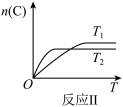 如图反应:此反应的△H<0,且T1<T2 如图反应:此反应的△H<0,且T1<T2 |
C.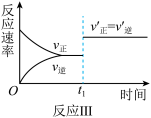 如图反应:表示t1时刻一定是使用催化剂对反应速率的影响 如图反应:表示t1时刻一定是使用催化剂对反应速率的影响 |
D. 如图反应:表示t1时刻增大B的浓度对反应速率的影响 如图反应:表示t1时刻增大B的浓度对反应速率的影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在一定条件下,利用CO2合成CH3OH的反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1.研究发现,反应过程中会发生产副反应:CO2(g)+H2(g)
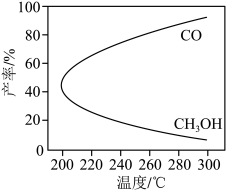
CH3OH(g)+H2O(g) △H1.研究发现,反应过程中会发生产副反应:CO2(g)+H2(g) CO(g)+H2O(g) △H2,温度对CH3OH、CO产率的影响如图所示。下列说法中不正确的是
CO(g)+H2O(g) △H2,温度对CH3OH、CO产率的影响如图所示。下列说法中不正确的是
 CH3OH(g)+H2O(g) △H1.研究发现,反应过程中会发生产副反应:CO2(g)+H2(g)
CH3OH(g)+H2O(g) △H1.研究发现,反应过程中会发生产副反应:CO2(g)+H2(g) CO(g)+H2O(g) △H2,温度对CH3OH、CO产率的影响如图所示。下列说法中不正确的是
CO(g)+H2O(g) △H2,温度对CH3OH、CO产率的影响如图所示。下列说法中不正确的是
| A.△H1<0,△H2>0 |
| B.增大压强有利于加快合成反应的速率 |
| C.生产过程中,温度越高越有利于提高CH3OH的产率 |
D.合成CH3OH反应的平衡常数表达式是K=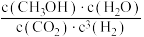 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】密闭容器中,由H2和CO直接制备二甲醚(CH3OCH3),其过程包含以下反应:
i. CO(g)+2H2(g) CH3OH(g)
CH3OH(g)  H1=-90.1 kJ·mol-1
H1=-90.1 kJ·mol-1
ii. 2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)  H2=-24.5 kJ·mol-1
H2=-24.5 kJ·mol-1
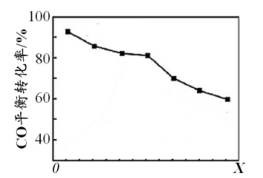
当其他条件相同时,由H2和CO直接制备二甲醚的反应中,CO平衡转化率随条件X的变化曲线如下图所示。下列说法正确的是
i. CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)  H1=-90.1 kJ·mol-1
H1=-90.1 kJ·mol-1ii. 2CH3OH(g)
 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)  H2=-24.5 kJ·mol-1
H2=-24.5 kJ·mol-1当其他条件相同时,由H2和CO直接制备二甲醚的反应中,CO平衡转化率随条件X的变化曲线如下图所示。下列说法正确的是

| A.由H2和CO直接制备二甲醚的反应为放热反应 |
| B.条件X为压强 |
| C.X增大,二甲醚的产率一定增大 |
| D.X增大,该反应的平衡常数一定减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】mA(g)+nB(g)  pC(g)(正反应为放热反应)的可逆反应,在恒温条件下,平衡时B在混合物中的含量(B%)与压强的关系如图所示,有关叙述正确的是
pC(g)(正反应为放热反应)的可逆反应,在恒温条件下,平衡时B在混合物中的含量(B%)与压强的关系如图所示,有关叙述正确的是

 pC(g)(正反应为放热反应)的可逆反应,在恒温条件下,平衡时B在混合物中的含量(B%)与压强的关系如图所示,有关叙述正确的是
pC(g)(正反应为放热反应)的可逆反应,在恒温条件下,平衡时B在混合物中的含量(B%)与压强的关系如图所示,有关叙述正确的是 
| A.m+n> p |
| B.x点的速率关系为v正>v逆 |
| C.n>p |
| D.x点比y点混合物反应速率快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸盐在水溶液中有四种含铁型体,25℃时,它们的物质的量分数随pH的变化如图所示。下列叙述错误的是
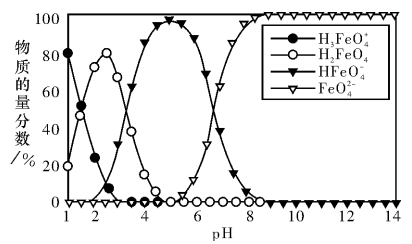

A.已知H3FeO4+的电离平衡常数分别为:K1=2.5×10-2,K2=4.8×10-4,K3=5.0×10-8,当pII=4时,溶液中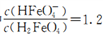 |
| B.为获得尽可能纯净的高铁酸盐,应控制pH≥9 |
| C.向pH=5的高铁酸盐溶液中加入KOH溶液,发生反应的离子方程式为HFeO4ˉ+OHˉ=FeO42-+H2O |
| D.pH=2时,溶液中主要含铁型体浓度的大小关系为c(H2FeO4)>c(H3FeO4+)> c (HFeO4ˉ) |
您最近一年使用:0次

 :
:
 ,在密闭容器中通入一定量的
,在密闭容器中通入一定量的 和
和 ,测得平衡时
,测得平衡时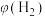 与温度及压强的关系如图所示。下列说法正确的是
与温度及压强的关系如图所示。下列说法正确的是