铁是人体内一种微量元素,以Fe2+的形式存在。回答下列问题:
(1)下列微粒中,既有氧化性也有还原性的是_______________ 填字母)。
A.Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中Fe3+是___________ (填“氧化剂”或“还原剂”)。
(3)某种麦片中含有微量的细小铁粉,食用该麦片后,铁粉与胃酸(HCl)反应的离子方程式_____________
(1)下列微粒中,既有氧化性也有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中Fe3+是
(3)某种麦片中含有微量的细小铁粉,食用该麦片后,铁粉与胃酸(HCl)反应的离子方程式
更新时间:2020-11-12 09:37:58
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】实验室可用KMnO4和浓盐酸反应制取氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
(1)该反应氧化剂是(填化学式,下同)___ ,还原剂是___ ,氧化产物是___ ,还原产物是___ 。被氧化的元素是___ ,参加还原反应的元素是___ 。
(2)浓盐酸在反应中显示出来的性质是___ 。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)若产生10个Cl2,则被氧化的HCl为___ 个,转移电子的数目为___ 个。
(4)生成的氯气除用向上排空气法收集还可以用___ 。
(1)该反应氧化剂是(填化学式,下同)
(2)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)若产生10个Cl2,则被氧化的HCl为
(4)生成的氯气除用向上排空气法收集还可以用
您最近半年使用:0次
【推荐2】研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)火药是中国的四大发明之一,黑火药在发生爆炸时,主要发生如下反应为: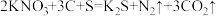 。每生成1个
。每生成1个 ,该反应转移电子
,该反应转移电子_______ 个。
(2)中国古代著作中有“银针验毒”的记录,其原理为: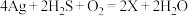 ,则X的化学式是
,则X的化学式是_______ ,其中 在该反应中
在该反应中_______ (填标号)。
A.作氧化剂 B.作还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)按如图所示操作,充分反应后:
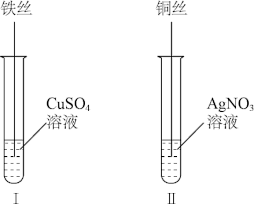
①II中铜丝上观察到的现象是_______ 。
②结合I、II实验现象可知 、
、 、
、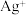 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______ 。
(4)已知Cl2可发生反应:2KBrO3 +Cl2=Br2 + 2KClO3。
①该反应中氧化剂是_______ (填化学式,下同),还原剂是_______ 。
②用双线桥法标出电子转移的数目和方向:_______ 。
(1)火药是中国的四大发明之一,黑火药在发生爆炸时,主要发生如下反应为:
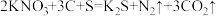 。每生成1个
。每生成1个 ,该反应转移电子
,该反应转移电子(2)中国古代著作中有“银针验毒”的记录,其原理为:
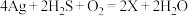 ,则X的化学式是
,则X的化学式是 在该反应中
在该反应中A.作氧化剂 B.作还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)按如图所示操作,充分反应后:

①II中铜丝上观察到的现象是
②结合I、II实验现象可知
 、
、 、
、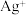 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(4)已知Cl2可发生反应:2KBrO3 +Cl2=Br2 + 2KClO3。
①该反应中氧化剂是
②用双线桥法标出电子转移的数目和方向:
您最近半年使用:0次
【推荐3】回答下列问题:
(1)写出下列物质在水溶液中的电离方程式。
①(NH4)2CO3:___ 。
②H2SO3:___ 。
(2)含0.6molAl3+的Al2(SO4)3中所含有的SO 的物质的量是
的物质的量是___ mol。
(3)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则R的摩尔质量为___ 。
(4)已知:4HCl+5NaClO2=5NaCl+4ClO2↑+2H2O。反应中氧化产物是___ ,还原剂与氧化剂的物质的量之比为___ 。
(1)写出下列物质在水溶液中的电离方程式。
①(NH4)2CO3:
②H2SO3:
(2)含0.6molAl3+的Al2(SO4)3中所含有的SO
 的物质的量是
的物质的量是(3)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则R的摩尔质量为
(4)已知:4HCl+5NaClO2=5NaCl+4ClO2↑+2H2O。反应中氧化产物是
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)写出下列俗名的化学式:铁红__ ,小苏打___ 。
(2)写出工业制取漂白粉的化学方程式___ 。
(3)最近报纸上报导了有人混用洗涤剂发生了中毒事件,当事人先用洁厕灵(强酸性,含盐酸)洗卫生间,再用84消毒液(含NaClO)进行杀菌。请写出涉及反应的离子方程式___ 。
(4)碱金属能形成离子型氢化物,如氢化钠的化学式为NaH,其中H-具有较强的还原性。常用NaH在高温下将TiCl4还原成Ti,反应的化学方程式为___ 。
(2)写出工业制取漂白粉的化学方程式
(3)最近报纸上报导了有人混用洗涤剂发生了中毒事件,当事人先用洁厕灵(强酸性,含盐酸)洗卫生间,再用84消毒液(含NaClO)进行杀菌。请写出涉及反应的离子方程式
(4)碱金属能形成离子型氢化物,如氢化钠的化学式为NaH,其中H-具有较强的还原性。常用NaH在高温下将TiCl4还原成Ti,反应的化学方程式为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】 在氧化还原反应中,氧化剂______ 电子,发生的反应是______ 反应;还原剂______ 电子,发生的反应是______ 反应。铁与氯气反应的方程式为,2Fe+3Cl2=2FeCl3生成物中铁是______ 价,铁与盐酸的反应式为______ ,生成物中铁是______ 价,事实证明,氯气的氧化性比盐酸的氧化性(填“强”“弱”)______ 。
您最近半年使用:0次

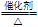 4NO+6H2O。
4NO+6H2O。

