某温度下,在2L容器中有3种气体物质进行反应,X、Y、Z三种物质的量随时间的变化曲线如图所示。
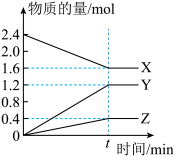
(1)该反应的化学方程式是___________________ 。
(2)若t=10 min,则Y的平均反应速率是__________ ,想要提高反应速率,可适当采取的措施是________ ,________ ,_______ 。(填三个)

(1)该反应的化学方程式是
(2)若t=10 min,则Y的平均反应速率是
更新时间:2020-11-21 20:59:55
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】I.用一定质量的Zn跟足量的稀硫酸反应制氢气,请回答:
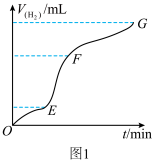
(1)实验过程如图1所示,EF段化学反应速率加快与该反应是___________ (填“放热”或“吸热”)反应有关。
Ⅱ.某温度时,气体A、B在5 L密闭容器中反应的物质的量随时间变化的曲线如图2所示。由图中数据分析求:___________ 。
(4)反应开始至4 min时,A的平均反应速率为___________ 。
(5)4min时,正、逆反应速率的大小关系为:v(正)___________ v(逆) (填“>”、“<”或“=”)。
(6)平衡时气体A的体积分数为___________ 。
(1)实验过程如图1所示,EF段化学反应速率加快与该反应是
| A.蒸馏水 | B.NaCl溶液 | C.NaNO3固体 | D.CuSO4固体 |
Ⅱ.某温度时,气体A、B在5 L密闭容器中反应的物质的量随时间变化的曲线如图2所示。由图中数据分析求:
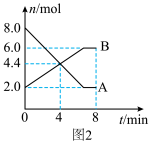
(4)反应开始至4 min时,A的平均反应速率为
(5)4min时,正、逆反应速率的大小关系为:v(正)
(6)平衡时气体A的体积分数为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】Ⅰ.一定温度下,在容积为2L的密闭容器中进行反应:aN(g)⇌bM(g),M、N的物质的量随时间的变化曲线如图所示:

(1)此反应的化学方程式中,已知计量系数比为最简整数比,则b=_______ 。
(2)若t2-t1=10 min,则从t1到t2时刻,以M的浓度变化表示该反应的平均反应速率,计算出来的结果为_______ mol/(L·min)。
Ⅱ.一定条件下,向2L恒容密闭容器中充入1mol PCl5,发生反应:PCl5(g)⇌PCl3(g)+Cl2(g)反应过程中测定的部分数据见表(反应过程中条件不变);
请回答下列问题:
(3)x的值是_______ 。
(4)60s时,PCl5的转化率是_______ 。
(5)达平衡时,容器中Cl2的体积分数是_______ (结果保留一位小数)

(1)此反应的化学方程式中,已知计量系数比为最简整数比,则b=
(2)若t2-t1=10 min,则从t1到t2时刻,以M的浓度变化表示该反应的平均反应速率,计算出来的结果为
Ⅱ.一定条件下,向2L恒容密闭容器中充入1mol PCl5,发生反应:PCl5(g)⇌PCl3(g)+Cl2(g)反应过程中测定的部分数据见表(反应过程中条件不变);
| t/s | 0 | 60 | 150 | 250 | 350 | 450 |
| n(PCl3)/mol | 0 | 0.12 | 0.19 | 0.2 | 0.2 | x |
请回答下列问题:
(3)x的值是
(4)60s时,PCl5的转化率是
(5)达平衡时,容器中Cl2的体积分数是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】80℃时,将0.40mol的N2O4气体充入2L的固定容积的密闭容器中,发生如下反应:N2O4 2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
(1)计算20s~40s内用N2O4表示的平均反应速率为_______
(2)计算在80℃时该反应的平衡常数K=_______
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色_______ (填“变浅”、“变深”或“不变”)
(4)要增大该反应的K值,可采取的措施有(填序号)_______
 2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:| 时间(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(2)计算在80℃时该反应的平衡常数K=
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色
(4)要增大该反应的K值,可采取的措施有(填序号)_______
| A.增大N2O4的起始浓度 | B.向混合气体中通入NO2 |
| C.使用高效催化剂 | D.升高温度 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)某温度时,在2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式_______ 和反应开始至2 min末Z的平均反应速率分别为_______

(2)在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:3A(g)+B(g) xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则
①x的值为___________ ;
②B的平衡浓度为___________ ;
③A的转化率为___________ ;
④D的体积分数为___________ ;

(2)在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:3A(g)+B(g)
 xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则 ①x的值为
②B的平衡浓度为
③A的转化率为
④D的体积分数为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】在某一容积为2L的恒容密闭容器中,A、B、C、D四种气体物质发生可逆反应,其物质的量n(mol)随时间t(min)的变化曲线如图所示。回答下列问题:

(1)该反应的化学方程式为____ 。
(2)前2min内用A的浓度变化表示的化学反应速率为____ ;
(3)在2min时,图象发生改变的原因可能是_____ (填字母)
A.增大B的物质的量B.降低温度C.加入催化剂D.减小A的物质的量
(4)不同条件下的该反应的速率:①v(A)=1.0mol·L-1·s-1,②v(B)=1.0 m ol·L-1·s-1,③v(C)=1.2 mol·L-1·s-1,④v(D)=1.2mol·L-1·s-1。其中反应速率最快的是___ (填序号)。

(1)该反应的化学方程式为
(2)前2min内用A的浓度变化表示的化学反应速率为
(3)在2min时,图象发生改变的原因可能是
A.增大B的物质的量B.降低温度C.加入催化剂D.减小A的物质的量
(4)不同条件下的该反应的速率:①v(A)=1.0mol·L-1·s-1,②v(B)=1.0 m ol·L-1·s-1,③v(C)=1.2 mol·L-1·s-1,④v(D)=1.2mol·L-1·s-1。其中反应速率最快的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】一定温度下,在2L的密闭容器中,M、N两种气体的物质的量随时间变化的曲线如图所示:

(1)反应的化学方程式为___________ 。
(2)反应达到最大限度的时间是___________ min,该时间内的平均反应速率v(N)=___________ 。
(3)判断该反应达到平衡状态的依据是___________ (填序号)
①该条件下,正、逆反应速率都为零
②2V正(N)=V逆(M)
③该条件下,N的物质的量保持不变
(4)能加快反应速率的措施任写两条___________

(1)反应的化学方程式为
(2)反应达到最大限度的时间是
(3)判断该反应达到平衡状态的依据是
①该条件下,正、逆反应速率都为零
②2V正(N)=V逆(M)
③该条件下,N的物质的量保持不变
(4)能加快反应速率的措施任写两条
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】简要回答下列问题。
(1)NO暴露在空气中,出现红棕色的原因是________ 。
(2)将食品置于低温条件下,常常可以保存更长时间的原因是________ 。
(3)盛有浓硫酸的容器敞口放置一段时间后,硫酸浓度变小的原因是________ 。
(4)推广使用新能源汽车的目的是________ 。
(1)NO暴露在空气中,出现红棕色的原因是
(2)将食品置于低温条件下,常常可以保存更长时间的原因是
(3)盛有浓硫酸的容器敞口放置一段时间后,硫酸浓度变小的原因是
(4)推广使用新能源汽车的目的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
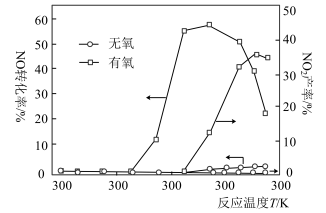
【推荐2】6NO(g)+4NH3(g)⇌5N2(g)+6H2O(g) ΔH=-1807.0kJ·mol-1;NO和NH3在Ag2O催化剂表面的反应活性随温度的变化曲线见下图。随着反应温度的进一步升高,在有氧的条件下NO的转化率明显下降的可能原因是___________ 。

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L﹣1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:
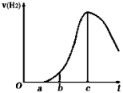
(1)曲线由O→a段不产生氢气的原因是_____________________ ;有关反应的离子方程式为________________________ ;
(2)曲线a→c段,产生氢气的速率增加较快的主要原因________________________________________ ;

(1)曲线由O→a段不产生氢气的原因是
(2)曲线a→c段,产生氢气的速率增加较快的主要原因
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】催化剂是能改变____ 而在反应前后____ 和____ 不变的物质。反应过程中即包括催化剂____ 反应又包括催化剂____ 的反应。催化剂通过参与反应改变____ 、改变____ 来改变化学反应速率。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】CO2/HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。HCOOH催化释氢。在催化剂作用下,HCOOH分解生成CO2和H2可能的反应机理如图所示。

(1)HCOOD催化释氢反应除生成CO2外,还生成__ (填化学式)。
(2)研究发现:其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳,其具体优点是__ 。

(1)HCOOD催化释氢反应除生成CO2外,还生成
(2)研究发现:其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳,其具体优点是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】某化学反应2A B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol•L-1)随反应时间(min)的变化情况见表,表中温度的单位为摄氏度(℃)。
B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol•L-1)随反应时间(min)的变化情况见表,表中温度的单位为摄氏度(℃)。
根据上述数据,回答下列问题。
(1)在实验1、2中,有一个实验使用了催化剂。请利用表中数据判断哪个实验使用了催化剂,并说明理由____ 。
(2)根据表中数据可知,实验3一定达到化学平衡状态的时间是____ 。
A.10min后 B.20min后 C.30min后
 B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol•L-1)随反应时间(min)的变化情况见表,表中温度的单位为摄氏度(℃)。
B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol•L-1)随反应时间(min)的变化情况见表,表中温度的单位为摄氏度(℃)。| 实验序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 |
| 2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 |
(1)在实验1、2中,有一个实验使用了催化剂。请利用表中数据判断哪个实验使用了催化剂,并说明理由
(2)根据表中数据可知,实验3一定达到化学平衡状态的时间是
A.10min后 B.20min后 C.30min后
您最近一年使用:0次



