(1)1mol 乙烷在氧气中完全燃烧生成二氧化碳和液态水,放出热量 1558.3kJ。写出 乙烷燃烧的热化学方程式:__________________ 。
(2)已知:2SO2(g)+O2(g)=2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)=2NO2(g) ΔH=-113.0 kJ·mol-1
则反应 NO2(g)+SO2(g)=SO3(g)+NO(g)的 ΔH=_______________ kJ·mol-1。
(3)向盛有10mL0.01 mol/L 的硫氰化钾溶液的小烧杯中,加入10mol0.01mol/L的FeCl3溶液,混合液立即___ 。写出上述反应的离子方程式____________________ 。
(2)已知:2SO2(g)+O2(g)=2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)=2NO2(g) ΔH=-113.0 kJ·mol-1
则反应 NO2(g)+SO2(g)=SO3(g)+NO(g)的 ΔH=
(3)向盛有10mL0.01 mol/L 的硫氰化钾溶液的小烧杯中,加入10mol0.01mol/L的FeCl3溶液,混合液立即
更新时间:2020-11-25 07:40:46
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】有四种常见药物①维生素C;②青霉素;③胃舒平;④麻黄碱。回答下列问题:
(1)某同学胃酸过多,应选用的药物是_______ (填序号)。抗酸药是治疗胃酸过多的一类药物,写出一种抗酸药与胃酸反应的化学方程式_______ 。
(2)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是_______ (填序号)。
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是_______ (填序号)。
(4)_______ (填序号)又称为抗坏血酸,它的分子式为_______ 。
(5)为预防缺铁性贫血,一些食品中加入了铁元素(含Fe2+物质)。若向铁强化牛奶中滴加KSCN溶液,发现牛奶变为红色,说明_______ ,此时若向其中加入一片维生素C,则发现红色消失,该实验说明维生素C具有_______ 性。
(1)某同学胃酸过多,应选用的药物是
(2)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是
(4)
(5)为预防缺铁性贫血,一些食品中加入了铁元素(含Fe2+物质)。若向铁强化牛奶中滴加KSCN溶液,发现牛奶变为红色,说明
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】钠、铝、铁是三种重要的金属。请回答:
(1)将一小块金属钠投入水中,发生反应的离子方程式为_______ ;可观察到的实验现象是_______ (填编号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(2)Fe跟 在一定条件下反应,所得产物的化学式是
在一定条件下反应,所得产物的化学式是_______ 。将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成_______ 色。
b.向另一支试管中滴加NaOH溶液,现象为_______ ,反应的离子方程式是_______ 。
(1)将一小块金属钠投入水中,发生反应的离子方程式为
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(2)Fe跟
 在一定条件下反应,所得产物的化学式是
在一定条件下反应,所得产物的化学式是a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,现象为
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】按要求写热化学方程式:
(1)25℃、101kPa条件下充分燃烧一定量的C2H2气体放出热量为1300kJ,经测定,将生成的CO2通入足量澄清石灰水中产生100g白色沉淀,写出表示C2H2气体充分燃烧的热化学方程式:___ ;
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式:___ 。
(1)25℃、101kPa条件下充分燃烧一定量的C2H2气体放出热量为1300kJ,经测定,将生成的CO2通入足量澄清石灰水中产生100g白色沉淀,写出表示C2H2气体充分燃烧的热化学方程式:
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式:
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和水,常温下1g甲硅烷自燃放出的热量为44.6KJ,其热化学方程式为__________________________ 。
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】已知下列热化学方程式:
①H2(g) + O2(g) = H2O(l)△H = -285.8 kJ / mol
O2(g) = H2O(l)△H = -285.8 kJ / mol
②C(s) + O2(g) = CO2(g)△H = -393.5 kJ / mol
③C(s) + H2O(g) = CO(g) + H2(g)△H = +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是______ (填序号,下同),属于吸热反应的是____ 。
(2)1 mol H2完全燃烧生成液态水,放出的热量为____ kJ。
(3)写出下列反应的热化学方程式
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68 kJ的热量;
_______________________________________________
②2 molCu(s) 与适量O2(g)反应生成CuO(s),放出314 kJ热量;
_______________________________________________
①H2(g) +
 O2(g) = H2O(l)△H = -285.8 kJ / mol
O2(g) = H2O(l)△H = -285.8 kJ / mol②C(s) + O2(g) = CO2(g)△H = -393.5 kJ / mol
③C(s) + H2O(g) = CO(g) + H2(g)△H = +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是
(2)1 mol H2完全燃烧生成液态水,放出的热量为
(3)写出下列反应的热化学方程式
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68 kJ的热量;
②2 molCu(s) 与适量O2(g)反应生成CuO(s),放出314 kJ热量;
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】煤燃烧后的主要产物是CO、CO2。
(1)以CO2为原料可制备甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,向1L的恒容密闭容器中充入1mol CO2(g)和3mol H2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,向1L的恒容密闭容器中充入1mol CO2(g)和3mol H2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图所示。
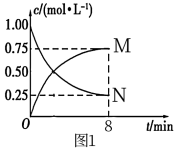

①图1中N表示的是______ (填化学式);0~8min内,以氢气表示的平均反应速率v(H2)=_______ mol • L-1 • min-1。
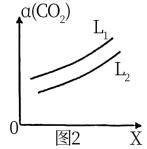
②在一定条件下,体系中CO2的平衡转化率(ɑ)与L和X的关系如图2所示,L和X分别表示温度和压强。X表示的物理量是____________ (填“温度”或“压强”),L1________ (填“>”或“<”)L2。
(2)向一体积为20L的恒容密闭容器中通入1molCO2发生反应:2CO2(g) 2CO(g)+O2(g),在不同温度下各物质的体积分数变化如图3所示。1600℃时反应达到平衡,则此时反应的平衡常数K
2CO(g)+O2(g),在不同温度下各物质的体积分数变化如图3所示。1600℃时反应达到平衡,则此时反应的平衡常数K_____________ 。
(1)以CO2为原料可制备甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,向1L的恒容密闭容器中充入1mol CO2(g)和3mol H2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,向1L的恒容密闭容器中充入1mol CO2(g)和3mol H2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图所示。


①图1中N表示的是
②在一定条件下,体系中CO2的平衡转化率(ɑ)与L和X的关系如图2所示,L和X分别表示温度和压强。X表示的物理量是
(2)向一体积为20L的恒容密闭容器中通入1molCO2发生反应:2CO2(g)
 2CO(g)+O2(g),在不同温度下各物质的体积分数变化如图3所示。1600℃时反应达到平衡,则此时反应的平衡常数K
2CO(g)+O2(g),在不同温度下各物质的体积分数变化如图3所示。1600℃时反应达到平衡,则此时反应的平衡常数K
您最近半年使用:0次
【推荐2】甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整。向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
(1)反应CO(g)+H2O(g)=CO2(g)+H2(g)的ΔH=________ kJ·mol-1。
(2)甲烷的燃烧热为ΔH2,则ΔH2________ ΔH1(填“>”、“=”或“<”)。
| 化学方程式 | 焓变ΔH(kJ·mol-1) | |
| 甲烷氧化 | CH4(g)+2O2(g)=CO2(g)+2H2O(g) | ΔH1 |
| CH4(g)+O2(g)=CO2(g)+2H2(g) | -322.0 | |
| 蒸汽重整 | CH4(g)+H2O(g)=CO(g)+3H2(g) | 206.2 |
| CH4(g)+2H2O(g)=CO2(g)+4H2(g) | 165.0 |
(1)反应CO(g)+H2O(g)=CO2(g)+H2(g)的ΔH=
(2)甲烷的燃烧热为ΔH2,则ΔH2
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】氨基甲酸铵(H2NCOONH4)为尿素生产过程的中间产物,易分解。某小组对氨基甲酸铵的分解实验进行探究
已知:Ⅰ.N2(g)+3H2(g) ⇌2NH3(g) ΔH1=-92.4 kJ·mol-1
Ⅱ.C(s)+O2(g) ⇌CO2(g) ΔH2=-393.8 kJ·mol-1
Ⅲ.N2(g)+3H2(g)+C(s)+O2(g) ⇌H2NCOONH4(s) ΔH3=-645.7 kJ·mol-1
(1)写出H2NCOONH4分解生成NH3与CO2气体的热化学方程式:_______
(2)已知:R ln Kp=- +C(C为常数)。根据表中实验数据得到图像(如图所示),则该反应的反应热ΔH=
+C(C为常数)。根据表中实验数据得到图像(如图所示),则该反应的反应热ΔH=_______ kJ·mol-1

已知:Ⅰ.N2(g)+3H2(g) ⇌2NH3(g) ΔH1=-92.4 kJ·mol-1
Ⅱ.C(s)+O2(g) ⇌CO2(g) ΔH2=-393.8 kJ·mol-1
Ⅲ.N2(g)+3H2(g)+C(s)+O2(g) ⇌H2NCOONH4(s) ΔH3=-645.7 kJ·mol-1
(1)写出H2NCOONH4分解生成NH3与CO2气体的热化学方程式:
(2)已知:R ln Kp=-
 +C(C为常数)。根据表中实验数据得到图像(如图所示),则该反应的反应热ΔH=
+C(C为常数)。根据表中实验数据得到图像(如图所示),则该反应的反应热ΔH=
您最近半年使用:0次



