据2020年9月15日新闻联播报道,欧洲南方天文台的天文专家团队在金星大气层中探测到磷化氢(PH3)气体。磷化氢是一种无色气体,极毒、有鱼腥臭气味。磷化氢的化学性质活泼,极易与氧气、氯气等发生剧烈反应,在温度高于500℃时分解为两种单质。
(1)从“磷化氢的化学性质活泼,极易与氧气、氯气等发生剧烈反应”的描述中可知,磷化氢具有_____ (“氧化性”“还原性”或“氧化性和还原性”)。
(2)实验室中可以用白磷与浓氢氧化钾共热制取磷化氢,反应的化学方程式如下:P4+3KOH(浓)+3H2O PH3↑+3KH2PO2
PH3↑+3KH2PO2
①KH2PO2中P元素的化合价是______ 。
②上述反应中,氧化剂与还原剂的质量比为______ ;氧化产物与还原产物的物质的量之比为______ 。用双线桥表示该反应电子转移的方向和数目_________ ;P4+3KOH(浓)+3H2O=PH3↑+3KH2PO2;若有124g白磷参与反应,则转移电子的数目为______ (NA表示阿伏加德罗常数的值);
③H3PO2与过量的KOH溶液反应生成KH2PO2,则H3PO2为______ 元酸。H3PO2是一种弱酸,写出H3PO2与过量的KOH溶液反应的离子方程式________ 。
(1)从“磷化氢的化学性质活泼,极易与氧气、氯气等发生剧烈反应”的描述中可知,磷化氢具有
(2)实验室中可以用白磷与浓氢氧化钾共热制取磷化氢,反应的化学方程式如下:P4+3KOH(浓)+3H2O
 PH3↑+3KH2PO2
PH3↑+3KH2PO2①KH2PO2中P元素的化合价是
②上述反应中,氧化剂与还原剂的质量比为
③H3PO2与过量的KOH溶液反应生成KH2PO2,则H3PO2为
更新时间:2020-11-28 21:47:43
|
相似题推荐
【推荐1】二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒(Se)可能成为环境污染物,可通过与浓HNO3或浓H2SO4反应后,经SO2还原来回收Se。
(1)Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1∶1,写出化学方程式:__ 。
(2)已知:Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O(Ⅰ)
2SO2+SeO2+2H2O=Se+2SO +4H+(Ⅱ)
+4H+(Ⅱ)
SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是__ 。
(3)可以通过下面的方法测定回收得到的SeO2样品中SeO2的含量:
①SeO2+KI+HNO3=Se+I2+KNO3+H2O
②I2+2Na2S2O3=Na2S4O6+2NaI
配平方程式①,用双线桥标出电子转移的方向和数目___ 。
(4)按(3)中的方法测定SeO2的含量。实验中,准确称量SeO2样品0.1500g,消耗0.2000mol•L-1的Na2S2O3溶液25.00mL,所测样品中SeO2的质量分数为___ 。
(1)Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1∶1,写出化学方程式:
(2)已知:Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O(Ⅰ)
2SO2+SeO2+2H2O=Se+2SO
 +4H+(Ⅱ)
+4H+(Ⅱ)SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是
(3)可以通过下面的方法测定回收得到的SeO2样品中SeO2的含量:
①SeO2+KI+HNO3=Se+I2+KNO3+H2O
②I2+2Na2S2O3=Na2S4O6+2NaI
配平方程式①,用双线桥标出电子转移的方向和数目
(4)按(3)中的方法测定SeO2的含量。实验中,准确称量SeO2样品0.1500g,消耗0.2000mol•L-1的Na2S2O3溶液25.00mL,所测样品中SeO2的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】NaClO广泛用作水处理剂及漂白剂。
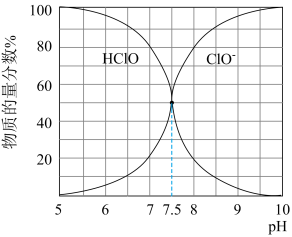
已知:25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH的分布如下图所示。
(1)工业上将Cl2通入 的NaOH溶液中制备NaClO。
的NaOH溶液中制备NaClO。
①NaClO属于______ (填“酸”、“盐”、“氧化物”),制备NaClO的离子方程式为_______ 。
②取少量pH=9时的溶液加入稀硫酸,发生离子方程式除了 外,还有
外,还有______ 。
③若反应温度过高会生成副产物NaClO3,写出该反应的离子方程式并用双线桥标明电子转移的方向和数目_______ ,该反应中氧化剂与还原剂的物质的量之比是_____ 。
(2)含NaClO消毒液与洁厕剂(含有盐酸)会产生有毒气体,写出该反应的离子方程式______ 。
已知:25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH的分布如下图所示。

(1)工业上将Cl2通入
 的NaOH溶液中制备NaClO。
的NaOH溶液中制备NaClO。①NaClO属于
②取少量pH=9时的溶液加入稀硫酸,发生离子方程式除了
 外,还有
外,还有③若反应温度过高会生成副产物NaClO3,写出该反应的离子方程式并用双线桥标明电子转移的方向和数目
(2)含NaClO消毒液与洁厕剂(含有盐酸)会产生有毒气体,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】商代炼铜时,所用的矿物原料主要是孔雀石,主要燃料是木炭,在温度1 000 ℃左右冶炼,可能涉及的反应有:①Cu2(OH)2CO3 2CuO+CO2↑+H2O;②2CuO+C
2CuO+CO2↑+H2O;②2CuO+C 2Cu+CO2↑;③CuO+CO
2Cu+CO2↑;③CuO+CO Cu+CO2;④CO2+C
Cu+CO2;④CO2+C 2CO。
2CO。
(1)从四种基本反应类型来看,①②④的反应类型分别为①____________ ,②____________ ,④____________ 。
(2)反应③中,________ 发生氧化反应,________ 发生还原反应。
(3)用双线桥法表示反应②的电子转移方向与数目________ 。
 2CuO+CO2↑+H2O;②2CuO+C
2CuO+CO2↑+H2O;②2CuO+C 2Cu+CO2↑;③CuO+CO
2Cu+CO2↑;③CuO+CO Cu+CO2;④CO2+C
Cu+CO2;④CO2+C 2CO。
2CO。(1)从四种基本反应类型来看,①②④的反应类型分别为①
(2)反应③中,
(3)用双线桥法表示反应②的电子转移方向与数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)平常我们食用的水果中含有丰富的维生素C,维生素C又被称为“抗坏血酸”,在人体内有重要的功能,例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有___________ (填“氧化性”或“还原性”)。
(2)工业废水中含有的重铬酸根离子(Cr2O )有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O
)有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O + 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是
+ 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是___________ (填离子符号,下同),氧化剂是___________ 。
(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S + 2KNO3 + 3C = K2S + N2↑+ 3CO2↑,在该反应中,还原剂是___________ (填化学式,下同),氧化剂是___________ 。
(4)在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石烙化成团。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)
①请完成上述火法炼锌反应的化学方程式:________
ZnCO3 +___________ = ___________ +___________ CO↑。
②在该反应中,还原剂是___________ (填化学式,下同),被还原的是___________ 。
(1)平常我们食用的水果中含有丰富的维生素C,维生素C又被称为“抗坏血酸”,在人体内有重要的功能,例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(2)工业废水中含有的重铬酸根离子(Cr2O
 )有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O
)有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O + 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是
+ 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S + 2KNO3 + 3C = K2S + N2↑+ 3CO2↑,在该反应中,还原剂是
(4)在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石烙化成团。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)
①请完成上述火法炼锌反应的化学方程式:
ZnCO3 +___________ = ___________ +___________ CO↑。
②在该反应中,还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列填空:
I.(1)呼吸面具中,Na2O2起反应的化学方程式为_____________ 。
(2)印刷电路板由高分子材料和铜箔复合而成,用FeCl3溶液刻制印刷电路时,发生的反应离子方程式为__________________ 。
(3)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的物质的量浓度之比为3:2,则已反应的Fe3+和未反应的Fe3+的物质的量之比为_____________ 。
II.某一反应体系中有反应物和生成物共6种: HCl、H2SO4、SnCl2、SnCl4、FeSO4、Fe(SO4)3,反应前在溶液中滴加KSCN 溶液显红色,反应后红色消失。
(1)该反应中的还原剂是_____________ 。
(2)写出该反应的化学方程式_____________ 。
I.(1)呼吸面具中,Na2O2起反应的化学方程式为
(2)印刷电路板由高分子材料和铜箔复合而成,用FeCl3溶液刻制印刷电路时,发生的反应离子方程式为
(3)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的物质的量浓度之比为3:2,则已反应的Fe3+和未反应的Fe3+的物质的量之比为
II.某一反应体系中有反应物和生成物共6种: HCl、H2SO4、SnCl2、SnCl4、FeSO4、Fe(SO4)3,反应前在溶液中滴加KSCN 溶液显红色,反应后红色消失。
(1)该反应中的还原剂是
(2)写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。根据所学知识回答下列问题:
(1) 是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验
是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验 是否泄漏,有关反应的化学方程式为
是否泄漏,有关反应的化学方程式为 ,该反应中氧化剂为
,该反应中氧化剂为___________ (填化学式),标准状况下,每生成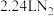 ,反应中转移的电子的物质的量为
,反应中转移的电子的物质的量为___________  。
。
(2)在一定条件下, 可与
可与 发生反应:
发生反应: ,在此过程中
,在此过程中 被
被___________ (填“氧化”或“还原”), 中
中 的化合价是
的化合价是___________ 价。
(3)某一反应体系有反应物和生成物共七种物质: 、
、 、
、 、
、 、
、 、
、 、
、 ,已知该反应中有气体生成。
,已知该反应中有气体生成。
①该反应中的还原剂是___________ (填化学式,下同),被还原的物质为___________ 。
②写出该反应的化学方程式:___________ 。
(1)
 是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验
是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验 是否泄漏,有关反应的化学方程式为
是否泄漏,有关反应的化学方程式为 ,该反应中氧化剂为
,该反应中氧化剂为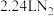 ,反应中转移的电子的物质的量为
,反应中转移的电子的物质的量为 。
。(2)在一定条件下,
 可与
可与 发生反应:
发生反应: ,在此过程中
,在此过程中 被
被 中
中 的化合价是
的化合价是(3)某一反应体系有反应物和生成物共七种物质:
 、
、 、
、 、
、 、
、 、
、 、
、 ,已知该反应中有气体生成。
,已知该反应中有气体生成。①该反应中的还原剂是
②写出该反应的化学方程式:
您最近一年使用:0次
【推荐2】Ⅰ.NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生反应:2NaNO2+4HI===2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是________ 。
(2)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有①水、②碘化钾淀粉试纸、③淀粉、④白酒、
⑤食醋,你认为必须选用的物质有________ (填序号)。
(3)请配平以下化学方程式:
______________________________
若反应过程中转移5 mol电子,则生成标准状况下N2的体积为________ L。
Ⅱ.“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业的味精”。钒对稀酸是稳定的,但室温下能溶解于浓硝酸中生成VO2+。
(4)请写出金属钒与浓硝酸反应的离子方程式:_______________________________ 。
(5)V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO43-),溶于强酸生成含钒氧离子(VO2+)的盐。请写出V2O5分别与烧碱溶液和稀硫酸反应生成的盐的化学式:________ 、________ 。
(1)上述反应中氧化剂是
(2)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有①水、②碘化钾淀粉试纸、③淀粉、④白酒、

⑤食醋,你认为必须选用的物质有
(3)请配平以下化学方程式:
若反应过程中转移5 mol电子,则生成标准状况下N2的体积为
Ⅱ.“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业的味精”。钒对稀酸是稳定的,但室温下能溶解于浓硝酸中生成VO2+。
(4)请写出金属钒与浓硝酸反应的离子方程式:
(5)V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO43-),溶于强酸生成含钒氧离子(VO2+)的盐。请写出V2O5分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
您最近一年使用:0次

 4Fe+3CO2↑
4Fe+3CO2↑ 2H2+CO2
2H2+CO2 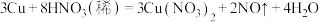
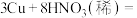
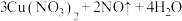
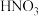 在反应中体现的性质有
在反应中体现的性质有

