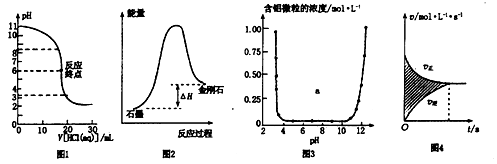
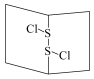
分析下表中数据,判断下列有关说法,其中正确的是
化学键 | H—H | Cl—Cl | H—Cl |
| 键能/(kJ·mol-1) | 436 | 243 | 431 |
| A.H—Cl键断裂需要吸收的热量为431 kJ |
| B.氢气和氯气反应生成2 mol氯化氢气体,反应的ΔH=-183 kJ·mol-1 |
| C.氢气和氯气反应生成1 mol氯化氢气体,反应的ΔH=-183 kJ·mol-1 |
| D.H2、Cl2、HCl三种分子的稳定性最强的是Cl2 |
18-19高二上·福建莆田·期中 查看更多[4]
河北省唐山市迁西县职业技术教育中心2021-2022学年高二(普职融通部)上学期9月月考化学试题浙江省舟山市舟山中学2021-2022学年高一下学期阶段性检测化学试题(已下线)练习19 共价键-2020-2021学年【补习教材·寒假作业】高二化学(人教版)福建省莆田第十五中学2018-2019学年高二上学期期中考试化学试题
更新时间:2020-12-04 19:54:41
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列图像均表示化学反应中的能量变化,其中描述正确的是
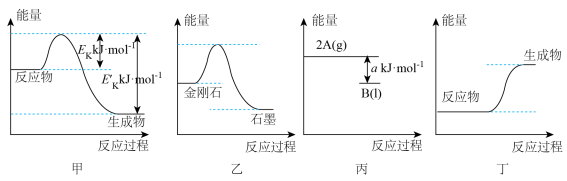
A.图甲可以表示反应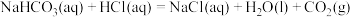 的能量变化 的能量变化 |
| B.图乙说明金刚石比石墨稳定 |
C.根据图丙可以判断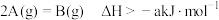 . . |
| D.图丁中断裂反应物中化学键所需的总能量低于形成生成物中化学键所释放的总能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】 和
和 在一定条件下能发生反应:
在一定条件下能发生反应: ,生成2molHI(g)反应放出热量akJ,已知a、b、c均大于零,下列说法错误的是
,生成2molHI(g)反应放出热量akJ,已知a、b、c均大于零,下列说法错误的是

 和
和 在一定条件下能发生反应:
在一定条件下能发生反应: ,生成2molHI(g)反应放出热量akJ,已知a、b、c均大于零,下列说法错误的是
,生成2molHI(g)反应放出热量akJ,已知a、b、c均大于零,下列说法错误的是
| A.断开1molH—H键和1molI—I键所需能量小于断开2molH—I键所需能量 |
| B.反应物的总能量高于生成物的总能量 |
| C.断开1molH—I键所需能量为(c+b+a)kJ |
D.向密闭容器中加入2mol 和2mol 和2mol ,充分反应后放出的热量小于2akJ ,充分反应后放出的热量小于2akJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】科学家实现了聚乙烯塑料转化成高附加值的产品,流程如图所示。下列叙述正确的是
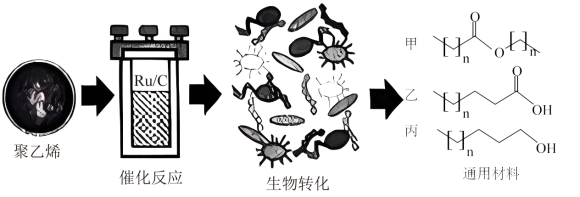

| A.聚乙烯不可用作食品外包装材料 |
| B.高温下生物转化比低温下快 |
| C.丙比乙多一个-CH2- |
| D.甲在碱性介质中能发生水解 |
您最近一年使用:0次
【推荐2】已知丙烷与Br2发生一元取代反应的机理如下(R·、X·表示自由基):
(1)Br2(g)→2Br·(g)ΔH1
(2)CH3CH2CH3(g)+Br·(g)→CH3CH2C H2(g)+HBr(g)ΔH2
CH3CH2CH3(g)+Br·(g)→CH3C HCH3(g)+HBr(g)ΔH2'
(3)CH3CH2C H2(g)+Br·(g)→CH3CH2CH2Br(g)ΔH3
CH3C HCH3(g)+Br·(g)→CH3CHBrCH3(g)ΔH3'
其中,(2)是决定反应速率的关键步骤,其“能量-反应进程”如图所示。
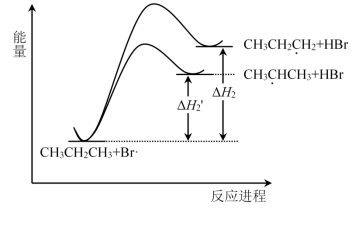
下列说法不正确 的是
(1)Br2(g)→2Br·(g)ΔH1
(2)CH3CH2CH3(g)+Br·(g)→CH3CH2
CH3CH2CH3(g)+Br·(g)→CH3
(3)CH3CH2
CH3
其中,(2)是决定反应速率的关键步骤,其“能量-反应进程”如图所示。

下列说法
| A.稳定性:CH3 |
| B.△H1>0 |
| C.丙烷与Br2发生一元取代反应的产物以CH3CHBrCH3为主 |
| D.适当升高温度,可以提高产物中CH3CH2CH2Br的比例 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知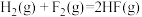 的能量变化如图所示,根据图示数据推知,
的能量变化如图所示,根据图示数据推知, 键的键能为( )
键的键能为( )
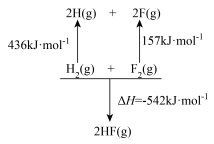
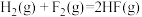 的能量变化如图所示,根据图示数据推知,
的能量变化如图所示,根据图示数据推知, 键的键能为( )
键的键能为( )
A.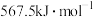 | B. | C. | D.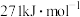 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知:N2(g)+3H2(g) 2NH3(l)△H=﹣132kJ/mol,蒸发1mol NH3(l)需要吸收的能量为20kJ,相关数据如下
2NH3(l)△H=﹣132kJ/mol,蒸发1mol NH3(l)需要吸收的能量为20kJ,相关数据如下
一定条件下,在体积1L的密闭容器中加入1molN2(g)和3molH2(g)充分反应,生成NH3(g)放出热量QkJ,下列说法正确的是
 2NH3(l)△H=﹣132kJ/mol,蒸发1mol NH3(l)需要吸收的能量为20kJ,相关数据如下
2NH3(l)△H=﹣132kJ/mol,蒸发1mol NH3(l)需要吸收的能量为20kJ,相关数据如下| H2(g) | N2(g) | NH3(g) | |
| 1mol分子中的化学键形成时要释放出的能量/kJ | 436 | 946 | a |
一定条件下,在体积1L的密闭容器中加入1molN2(g)和3molH2(g)充分反应,生成NH3(g)放出热量QkJ,下列说法正确的是

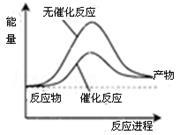
| A.上图可表示合成氨过程中的能量变化 |
| B.a的数值为1173 |
| C.Q的数值为92 |
| D.其它条件相同,反应使用催化剂时释放出的能量大于无催化剂时释放出的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
A.邻羟基苯甲醛(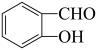 )的熔、沸点比对羟基苯甲醛( )的熔、沸点比对羟基苯甲醛(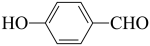 )的熔、沸点低 )的熔、沸点低 |
| B.HF比HCl稳定可用范德华力强弱解释 |
C.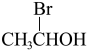 中不含手性碳原子 中不含手性碳原子 |
| D.形成氢键A—H…B—的三个原子总在一条直线上 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】根据价层电子对互斥理论的分析,影响键角大小的因素主要有三:一是中心原子的杂化类型;二是中心原子的孤电子对数;三是中心原子的电负性大小等。下列关于键角的比较不正确 的是
A.甲醛(HCHO)和光气(COCl2)分子中:键角 |
B.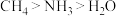 |
C.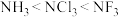 |
D. |
您最近一年使用:0次

 2SO3(g)△H=一98.3kJ/mol。将lmolSO2和0.5molO2充入 一密闭容器中充分反应,放出49.15kJ的热量
2SO3(g)△H=一98.3kJ/mol。将lmolSO2和0.5molO2充入 一密闭容器中充分反应,放出49.15kJ的热量