短周期元素A、B、C、D、E的原子序数依次增大,其中只有A与C、B与D同主族,C的离子和B的离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物溶于水形成的溶液呈碱性,E的单质为黄绿色气体可用于漂白和消毒,用化学用语 回答下列问题:
(1)写出元素E的简单离子结构示意图:________________________ ;
(2)由A分别与B、D、E所形成的共价化合物,热稳定性最差的是___________ (填化学式);
(3)由A和E形成的化合物与A和B形成的化合物反应所得产物的化学式为___________ ;由A和C形成的化合物的电子式为______________ ;
(4)元素A和氧元素以原子个数比1∶1化合形成化合物Q,元素B与氢元素以原子个数比1∶2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成B单质和A的另一种氧化物,写出该反应的化学方程式:______________________ 。
(1)写出元素E的简单离子结构示意图:
(2)由A分别与B、D、E所形成的共价化合物,热稳定性最差的是
(3)由A和E形成的化合物与A和B形成的化合物反应所得产物的化学式为
(4)元素A和氧元素以原子个数比1∶1化合形成化合物Q,元素B与氢元素以原子个数比1∶2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成B单质和A的另一种氧化物,写出该反应的化学方程式:
更新时间:2020-04-17 14:04:46
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D是四种短周期元素, E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为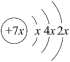 ,B是同周期第一电离能最小的元素,C原子的最外层有三个未成对电子,E的价层电子排布式为3d54s1,回答下列问题:
,B是同周期第一电离能最小的元素,C原子的最外层有三个未成对电子,E的价层电子排布式为3d54s1,回答下列问题:
(1)上述五种元素的最高价氧化物对应水化物酸性最强的是_______ (用化学式表示,下同),碱性最强的是_______ 。
(2)D所在周期(除稀有气体元素外)中第一电离能最大的元素是_______ (用元素符号表示,下同),电负性最大的元是_______ 。
(3)D的简单氢化物比C的简单氢化物的沸点_______ (填“高”或“低”),原因是_______ 。
(4)元素周期表可按电子排布分为s区、p区等,则E元素在_______ 区。
(5)B、C最高价氧化物的晶体类型分别是_______ 晶体、_______ 晶体。
(6)画出D的核外电子排布图_______ 。
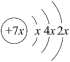 ,B是同周期第一电离能最小的元素,C原子的最外层有三个未成对电子,E的价层电子排布式为3d54s1,回答下列问题:
,B是同周期第一电离能最小的元素,C原子的最外层有三个未成对电子,E的价层电子排布式为3d54s1,回答下列问题:(1)上述五种元素的最高价氧化物对应水化物酸性最强的是
(2)D所在周期(除稀有气体元素外)中第一电离能最大的元素是
(3)D的简单氢化物比C的简单氢化物的沸点
(4)元素周期表可按电子排布分为s区、p区等,则E元素在
(5)B、C最高价氧化物的晶体类型分别是
(6)画出D的核外电子排布图
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D为原子序数依次增大的四种短周期元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C的最高正价为+5价,核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是___________ (填元素符号),C原子价电子运动状态有___________ 种。
(2)单质A有两种同素异形体,其中沸点高的是_____ (填分子式);B的氢化物所属的晶体类型为______ 。
(3)C和D反应可生成组成比为1︰3的化合物E,E的立体构型为_____ ,中心原子的杂化轨道类型为_____ 。
(4)A和B能够形成化合物F,其晶胞结构如图所示,F的化学式为______ ,晶胞中A的配位数为______ ,A原子和B原子的最近距离为______ pm,晶胞参数a=apm,阿伏加德罗常数的值为NA,晶体F的密度为____ g·cm-3(列出计算式)。

(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1︰3的化合物E,E的立体构型为
(4)A和B能够形成化合物F,其晶胞结构如图所示,F的化学式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表标出的是元素周期表中的一部分元素,回答下列问题:
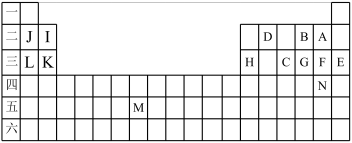
(1)表中用字母标出的14种元素中,化学性质最不活泼的是__________ (用元素符号表示,下同)金属性最强的是__________ ,非金属性最强的是__________ ,D元素在周期表中的位置是________ ,属于过渡元素的是____________ (该空用字母表示)。
(2)B、C、G最简单氢化物中稳定顺序_____ >______ >______ (填化学式)。
(3)H分别与第三周期中原子半径最大、最小的最高价氧化物的水化物之间的离子反应方程式是_________________________________ ;______________________ 。

(1)表中用字母标出的14种元素中,化学性质最不活泼的是
(2)B、C、G最简单氢化物中稳定顺序
(3)H分别与第三周期中原子半径最大、最小的最高价氧化物的水化物之间的离子反应方程式是
您最近一年使用:0次
【推荐1】X是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y基态原子的3p轨道上有2个未成对电子。元素Z 的原子最外层电子数是其内层的3倍。回答下列问题:
(1)元素X在元素周期表中位于_______ 区,单质X的晶体类型为____________ ,其中X原子的配位数为______________ 。
(2)已知元素Y可与元素Z的相对原子质量之差为16,则元素Y基态原子的外围电子排布图为______________________ ,其同周期元素中,第一电离能最大的是______ (写元素符号)。元素Y的含氧酸中,酸性最强的是________ (写化学式),该酸根离子的立体构型为________ 。
(3)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为______________________ 。
(4)X与Y形成的一种化合物的立方晶胞如图所示。

该化合物的化学式为_______ ,已知此晶体的密度为ρg·cm–3,阿伏伽德罗常数为NA,则此晶胞中X与Y的最近距离是______ cm。(写出计算式,不要求计算结果。)
(1)元素X在元素周期表中位于
(2)已知元素Y可与元素Z的相对原子质量之差为16,则元素Y基态原子的外围电子排布图为
(3)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为
(4)X与Y形成的一种化合物的立方晶胞如图所示。

该化合物的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】已知元素X、Y、Z、M、R均属前四周期且原子序数依次增大。X的核外电子总数与其周期数相同;Y的基态原子的核外电子占据3个能级,且最高能级轨道为半充满状态;Z的原子最外层电子数是其内层电子数的3倍;M的原子序数是Z的两倍;R的内部各能层均排满,且最外层电子数为1。
(1)在第2周期中,第一电离能大于Z的元素有_______ 种。
(2)基态M原子的价电子中,两种自旋状态的电子数之比为_______ 。
(3) 的键角
的键角_______ (填“大于”或“小于”)X2Z的键角,原因是_______ 。
(4)这些元素形成的含氧酸中,分子内中心原子的价层电子对数为4的所有酸是_______ (填化学式,下同);酸根呈平面正三角形结构的酸是_______ 。
(5) 难溶于水,易溶于氨水,写出其溶于氨水的离子方程式
难溶于水,易溶于氨水,写出其溶于氨水的离子方程式_______ ;NF3不易与 形成配离子,其原因是
形成配离子,其原因是_______ 。
(1)在第2周期中,第一电离能大于Z的元素有
(2)基态M原子的价电子中,两种自旋状态的电子数之比为
(3)
 的键角
的键角(4)这些元素形成的含氧酸中,分子内中心原子的价层电子对数为4的所有酸是
(5)
 难溶于水,易溶于氨水,写出其溶于氨水的离子方程式
难溶于水,易溶于氨水,写出其溶于氨水的离子方程式 形成配离子,其原因是
形成配离子,其原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、Q、E五种元素中,X原子核外M层中只有两对成对电子,Y原子核外L层电子数是K层两倍,Z是地壳内含量(质量分数)最高元素,Q核电荷数是X与Z核电荷数之和,E电负性最大。
(1)相同条件下XZ2与YZ2分子在水中溶解度较大是 ,理由是
;
(2)Q的外围电子排布为 ,在形成化合物时它的最高化合价为 ;
(3)在测定E的气态氢化物的相对分子质量时,实验测得的值一般高于理论值的主要原因是: 。
(1)相同条件下XZ2与YZ2分子在水中溶解度较大是 ,理由是
;
(2)Q的外围电子排布为 ,在形成化合物时它的最高化合价为 ;
(3)在测定E的气态氢化物的相对分子质量时,实验测得的值一般高于理论值的主要原因是: 。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子最外层电子数的3倍。回答以下问题:
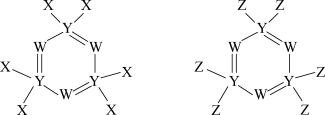
(1)W、X、Y、Z四种元素依次为___________ 、___________ 、___________ 、___________ ,其中___________ 元素原子半径最大,___________ 元素的氢化物最稳定(用元素符号表示)。
(2)X的氢化物在水中是一种弱酸,但却可以刻蚀玻璃,其中发生主要反应的化学方程式为___________
(3)由Z、W和氢三种元素形成的离子化合物的电子式为___________ ,实验室常以它为原料制取W的最简单氢化物,请写出该反应的化学方程式___________ 。

(1)W、X、Y、Z四种元素依次为
(2)X的氢化物在水中是一种弱酸,但却可以刻蚀玻璃,其中发生主要反应的化学方程式为
(3)由Z、W和氢三种元素形成的离子化合物的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E 是核电荷数依次增大的五种短周期主族元素,A 元素的原子核内只有 1 个质子;B 元素的原子半径是其所在主族中最小的,B 的最高价氧化物对应水化物的化学式为HBO3; C 元素原子的最外层电子数比次外层多 4;C 的阴离子与 D 的阳离子具有相同的电子排布,两元素可形成化合物 D2C;C、E 同主族。
(1)E 元素形成的最高价氧化物对应的水化物的化学式为___________ 。
(2)元素 C、D、E 形成的简单离子半径大小关系是___________ (用离子符号表示)。
(3)用电子式表示化合物A2C的形成过程:___________ 。C、D 还可形成化合物 D2C2, D2C2中含有的化学键类型是___________ 。
(4)由 A、B、C 三种元素形成的离子化合物的化学式为___________ ,它与强碱溶液共热,发生反应的离子方程式是___________ 。
(1)E 元素形成的最高价氧化物对应的水化物的化学式为
(2)元素 C、D、E 形成的简单离子半径大小关系是
(3)用电子式表示化合物A2C的形成过程:
(4)由 A、B、C 三种元素形成的离子化合物的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】元素的电负性用来描述不同元素的原子对键合电子吸引力的大小。电负性应用:
判断元素的金属性和非金属性的强弱。下表列出了同周期的几种短周期元素的部分性质
请回答下列问题:
(l)写出D元素的离子结构示意图_______________ 。
(2)X的值应为____ (填字母)。
A.3.6 B.3.1 C.1.4 D.2.1
(3)分析表中数据,简述同周期元素(除惰性气体)电负性大小与原子半径的关系:________________________________ 。
(4)A、B、C三种元素形成的氢化物中,其稳定性由强到弱的顺序是:__________________ (用化学式表示)。
(5)A、D最高价氧化物对应水化物相互反应的化学方程式:____ 。
判断元素的金属性和非金属性的强弱。下表列出了同周期的几种短周期元素的部分性质
请回答下列问题:
| 元素符号 | A | B | C | D | E |
| 电负性 | 3.0 | 2.5 | X | 1.5 | 0.9 |
| 原子半径(单位nm) | 0.099 | 0.102 | 0.110 | 0.143 | 0.186 |
| 主要化合价 | -1,+7 | -2,+6 | -3,+5 | +3 | +1 |
(2)X的值应为
A.3.6 B.3.1 C.1.4 D.2.1
(3)分析表中数据,简述同周期元素(除惰性气体)电负性大小与原子半径的关系:
(4)A、B、C三种元素形成的氢化物中,其稳定性由强到弱的顺序是:
(5)A、D最高价氧化物对应水化物相互反应的化学方程式:
您最近一年使用:0次



