某科研团队研制出的“ ”(
”( 表示过渡金属)体系,在温和条件下显著提高了氮气和氢气合成
表示过渡金属)体系,在温和条件下显著提高了氮气和氢气合成 的效率,其原理示意图如图:
的效率,其原理示意图如图:
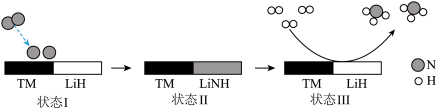
下列分析不合理的是
 ”(
”( 表示过渡金属)体系,在温和条件下显著提高了氮气和氢气合成
表示过渡金属)体系,在温和条件下显著提高了氮气和氢气合成 的效率,其原理示意图如图:
的效率,其原理示意图如图:
下列分析不合理的是
A.状态Ⅰ为 键断裂,是放热过程 键断裂,是放热过程 |
| B.该体系不能用于水的分解 |
C.在该体系中“ ”是催化剂 ”是催化剂 |
D.生成 的过程存在反应: 的过程存在反应: |
更新时间:2020-12-18 23:35:52
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知:H-H、N-H、N≡N的键能分别为436kJ/mol,391kJ/mol,946kJ/mol,则:1molH2(g)与足量氮气完全反应生成NH3(g)的反应热△H(kJ/mol)为( )
| A.+30.67 | B.-345.3 | C.-30.67 | D.+345.3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知 2O(g)=O2(g) ∆H = - 496 kJ ∙mol -1,结合能量变化示意图。下列说法正确的是
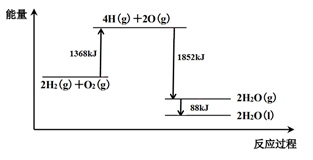

| A.拆开 1 mol H2(g) 中的化学键需要吸收 932 kJ能量 |
| B.拆开 1 mol H2O(g) 中所有化学键需要吸收 926 kJ能量 |
| C.1 mol H2O(l) 转变为 1mol H2O(g)需要吸收 88 kJ能量 |
| D.2 mol H2(g) 和 1mol O2(g) 反应生成 2 mol H2O(l),共放热 1940 kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】中国科学院天津工业生物技术研究所一支科研团队在实验室里首次实现了二氧化碳到淀粉的全合成,相关成果北京时间9月24日由国际知名学术期刊《科学》在线发表。下列说法中正确的是
| A.该合成过程是一个放热过程 |
B.该过程中只有 这一种反应物 这一种反应物 |
| C.该过程不需要任何的催化剂 |
| D.该成果如果实现量产,则在未来能够解决人类的粮食问题,是一个伟大的发现 |
您最近一年使用:0次
【推荐2】在其他条件具备时,若一反应较难进行,则其主要原因可能是
①参加反应的分子的能量普遍较低 ②参加反应的分子的能量普遍较高
③单位时间内反应物活化分子有效碰撞次数较少 ④化学反应的活化能较低
⑤反应物分子中活化分子百分数较小 ⑥反应物分子中活化分子百分数较大.
①参加反应的分子的能量普遍较低 ②参加反应的分子的能量普遍较高
③单位时间内反应物活化分子有效碰撞次数较少 ④化学反应的活化能较低
⑤反应物分子中活化分子百分数较小 ⑥反应物分子中活化分子百分数较大.
| A.①③⑤ | B.②④⑥ | C.①④⑥ | D.②③⑤ |
您最近一年使用:0次




