二硫化硒(SeS2)具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。
(1)二硫化硒(SeS2)具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。硒与硫在元素周期表中的相对位置如图所示。

硒在元素周期表中的位置是___________ ;硒原子核外有___________ 个未成对电子;硒化氢的电子式为___________ 。
(2)已知SeS2分子比例模型如所示,推测SeS2为___________ 分子(填“极性”或“非极性”)。
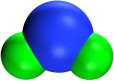
(3)SeS2中硫元素的化合价为负价,请从原子结构角度解释原因:___________ 。
工业上提取硒的过程如下:
第一步(未配平):X + Se + H2SO4 → Na2SO4 + H2SeO3 + ClO2↑+ H2O
已知该反应中氧化产物与还原产物的物质的量之比为1:4。
第二步:向H2SeO3溶液中通入SO2,可析出固体Se。
(4)第一步中X的化学式为___________ 。每溶解1 mol Se,转移电子数为___________ 个。
(5)写出第二步反应的化学方程式___________ ;该反应中被氧化的元素是___________ 。
(1)二硫化硒(SeS2)具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。硒与硫在元素周期表中的相对位置如图所示。

硒在元素周期表中的位置是
(2)已知SeS2分子比例模型如所示,推测SeS2为

(3)SeS2中硫元素的化合价为负价,请从原子结构角度解释原因:
工业上提取硒的过程如下:
第一步(未配平):X + Se + H2SO4 → Na2SO4 + H2SeO3 + ClO2↑+ H2O
已知该反应中氧化产物与还原产物的物质的量之比为1:4。
第二步:向H2SeO3溶液中通入SO2,可析出固体Se。
(4)第一步中X的化学式为
(5)写出第二步反应的化学方程式
2021·上海虹口·一模 查看更多[1]
更新时间:2020-12-20 12:07:52
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知A、B、C、D、E五种短周期元素,原子序数大小顺序为:C>A>B>D>E,A、C同周期,B、C同主族,A和B形成的离子化合物A2B中离子的电子数相同,其电子总数为30,D和E可形成4核10电子分子。请回答下面的问题:
(1)写出五种元素的符号:A___________ ;B___________ ;C___________ ;D___________ ;E___________ 。
(2)写出A2B的电子式:___________ 。
(3)写出下列物质的电子式:
D元素的单质___________ ;
E和B元素形成的化合物___________ 。
A、B、E三种元素形成的化合物___________ ;
D和E元素形成的化合物___________ 。
(1)写出五种元素的符号:A
(2)写出A2B的电子式:
(3)写出下列物质的电子式:
D元素的单质
E和B元素形成的化合物
A、B、E三种元素形成的化合物
D和E元素形成的化合物
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】现有A、B、C、D四种短周期主族元素,其相关性质信息如下。
请回答下列问题:
(1)元素D在元素周期表中的位置为___________ 。
(2)元素A和元素B形成的某种分子中含有18个电子,则该分子的电子式为___________ 。
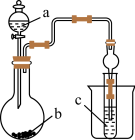
(3)若用如下装置证明元素C的非金属性强于D的非金属性,a、b、c均为化学药品,a为稀硫酸,那么c为___________ ,试管内发生的反应的离子方程式为___________ 。
| 元素编号 | 元素性质与原子结构 |
| A | 常温下,有 、 、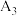 型两种气体单质存在 型两种气体单质存在 |
| B | 形成的常见离子核外电子数为0 |
| C | 最外层电子数是次外层的两倍 |
| D | 氧化物常被用来制造“光纤” |
(1)元素D在元素周期表中的位置为
(2)元素A和元素B形成的某种分子中含有18个电子,则该分子的电子式为
(3)若用如下装置证明元素C的非金属性强于D的非金属性,a、b、c均为化学药品,a为稀硫酸,那么c为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E、M、N六种短周期主族元素,它们的核电荷数依次增大。A可与D、E形成10电子分子,其中B的最外层电子数等于次外层电子数,C原子最外层电子数是次外层电子数的2倍,M的L层电子数为K层和M层电子数之和,D和M同主族。回答下列问题:
(1)元素B的符号和名称分别是______ ,_____ ;在周期表中的位置是____________ 。
(2)元素C的原子结构示意图为______________________________ 。
(3)元素C与M可形成CM2,C与N可形成CN4,这两种化合物均可做溶剂,其电子式分别为:_________ 和_________ 。
(4)元素A与D、E形成10电子分子的结构式分别为:__________ 和__________ 。
(5)元素C和M相比,非金属性较强的是_________ (用元素符号表示)。
(6)元素D、M的氢化物的沸点高低顺序为:_________ (用化学式表示)。
(7)在一定条件下,A、D的单质和M的最高价氧化物对应水化物的溶液可构成原电池,该电池在放电过程中,电解质溶液的酸性将_________ (填“增大”“减小”或“不变”)。
(8)1 mol CA4与D2完全反应生成两种气体时放出热量802kJ,则该反应的热化学方程式为__________________________________________________________________ 。
(1)元素B的符号和名称分别是
(2)元素C的原子结构示意图为
(3)元素C与M可形成CM2,C与N可形成CN4,这两种化合物均可做溶剂,其电子式分别为:
(4)元素A与D、E形成10电子分子的结构式分别为:
(5)元素C和M相比,非金属性较强的是
(6)元素D、M的氢化物的沸点高低顺序为:
(7)在一定条件下,A、D的单质和M的最高价氧化物对应水化物的溶液可构成原电池,该电池在放电过程中,电解质溶液的酸性将
(8)1 mol CA4与D2完全反应生成两种气体时放出热量802kJ,则该反应的热化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】硫酸亚铁铵晶体 俗称莫尔盐,是分析化学中的重要试剂,其化学性质与
俗称莫尔盐,是分析化学中的重要试剂,其化学性质与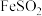 相近,但在空气中比一般的亚铁盐稳定。某同学在实验室中以铁粉与硫酸铵为原料按如下流程制备莫尔盐并测其产率(产率=
相近,但在空气中比一般的亚铁盐稳定。某同学在实验室中以铁粉与硫酸铵为原料按如下流程制备莫尔盐并测其产率(产率= )。
)。
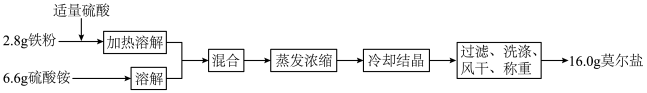
请回答下列问题:
(1)向莫尔盐溶液中加入氨水,久置后产生红褐色沉淀,该红褐色沉淀为___________ (填化学式)。莫尔盐溶液也能使酸性 溶液褪色,反应的离子方程式为
溶液褪色,反应的离子方程式为___________ 。
(2)用适量硫酸溶解铁粉时,还原产物是___________ (填化学式)。
(3)蒸发浓缩时,溶液应装在___________ 中(填仪器名称)。蒸发时不能蒸干溶液,而要在有晶体析出时立刻停止加热,原因是___________
(4)某同学通过上述流程制得莫尔盐16.0g,则实验产率为___________ (保留1位小数)。
 俗称莫尔盐,是分析化学中的重要试剂,其化学性质与
俗称莫尔盐,是分析化学中的重要试剂,其化学性质与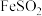 相近,但在空气中比一般的亚铁盐稳定。某同学在实验室中以铁粉与硫酸铵为原料按如下流程制备莫尔盐并测其产率(产率=
相近,但在空气中比一般的亚铁盐稳定。某同学在实验室中以铁粉与硫酸铵为原料按如下流程制备莫尔盐并测其产率(产率= )。
)。
请回答下列问题:
(1)向莫尔盐溶液中加入氨水,久置后产生红褐色沉淀,该红褐色沉淀为
 溶液褪色,反应的离子方程式为
溶液褪色,反应的离子方程式为(2)用适量硫酸溶解铁粉时,还原产物是
(3)蒸发浓缩时,溶液应装在
(4)某同学通过上述流程制得莫尔盐16.0g,则实验产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】亚硝酞氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如下图I、II、III所示:

图中A导管的作用是___________ 为制备纯净干燥的气体,下表中缺少的药品是:
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:

①装置连接顺序为a→_____ (按气流自左向右方向,用小写字母表示)。
②装置IV、V除可进一步干燥NO、Cl2外,另一个作用是______ 。
③装置VII的作用是______________ 。
④装置VIII中吸收尾气时,NOCl发生反应的化学方程式为_________________ 。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为________ 。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如下图I、II、III所示:

图中A导管的作用是
| 装置I | 装置II | ||
| 烧瓶中 | 分液漏斗中 | ||
| 制备纯净Cl2 | ① | 浓盐酸 | ② |
| 制备纯净NO | Cu | 稀硝酸 | ③ |

①装置连接顺序为a→
②装置IV、V除可进一步干燥NO、Cl2外,另一个作用是
③装置VII的作用是
④装置VIII中吸收尾气时,NOCl发生反应的化学方程式为
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氢氧化钴[Co(OH)2]是锂电池正极材料钴酸锂(LiCoO2)的前驱体,以废旧锂电池正极材料(含LiCoO2及少量Al、Fe等)为原料制备CoSO4溶液,以CoSO4溶液、NaOH溶液、氨水和水合肼为原料可制得微米级Co(OH)2。
已知:①Co2+、Co3+易与NH3形成络合物,[Co(NH3)6]2+的还原性强于Co(OH)2和Co2+;
②水合肼(N2H4·H2O)为无色油状液体,具有强还原性,氧化产物为N2;
③沉淀的生成速率越快,颗粒越小,呈凝乳状成胶体,不易过滤。
(1)以废旧锂电池正极材料为原料制备CoSO4溶液。取一定量废旧锂电池正极材料,粉碎后与Na2SO3溶液混合配成悬浊液,边搅拌边加入1 mol/LH2SO4溶液充分反应。LiCoO2转化为CoSO4、Li2SO4的化学方程式为_______ 。从分液漏斗中滴入1 mol/LH2SO4时,滴加速率不能太快且需要快速搅拌的原因是_______ 。
(2)60℃时在搅拌下向CoSO4溶液中加入氨水,调节pH至6后,再加入NaOH溶液,调节pH至9.5左右,一段时间后,过滤、洗涤,真空烘干得微米级Co(OH)2。制备时,在加入NaOH溶液前必须先加氨水的原因是_______ 。
(3)经仪器分析,测得按题(2)步骤制得的Co(OH)2晶体结构中含有Co(III),进一步用碘量法测得Co(II)的氧化程度为8%。因此制备时必须加入一定量的还原剂。
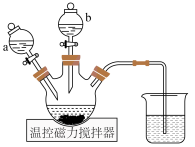
将500 mL1 mol/L的CoSO4溶液与氨水配成pH为6的溶液,加入三颈烧瓶中(装置如图),滴液漏斗a装有NaOH溶液、b中装有水合肼,60℃时依次将两种溶液加入三颈烧瓶,充分反应后,过滤,实验时应先打开滴液漏斗_______ (填“a”成“b”)。
(4)利用含钴废料(主要成分为Co3O4,还含有少量的石墨、LiCoO2等杂质)制备碳酸钴CoCO3。
已知:①CoCO3几乎不溶于水,Li2CO3微溶于水,Co2+(以0.1 mol/L)开始沉淀的pH为7.6;
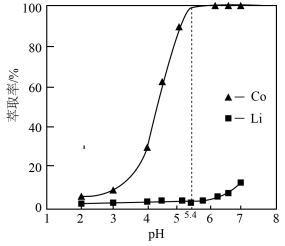
②钴、锂在有机磷萃取剂(HR)中的萃取率与pH的关系如图所示;
③酸性条件下的氧化性强弱顺序为:Co3+>H2O2。
请补充完整实验方案:取一定量含钴废料,粉碎后_______ ,充分反应后,静置后过滤,洗涤、干燥得到CoCO3。
实验中可选用的试剂:2 mol/L H2SO4溶液、2 mol/LNaOH溶液、有机磷(HR)、5 mol/L Na2CO3溶液、0.5 mol/LNa2CO3溶液、30%H2O2溶液。
已知:①Co2+、Co3+易与NH3形成络合物,[Co(NH3)6]2+的还原性强于Co(OH)2和Co2+;
②水合肼(N2H4·H2O)为无色油状液体,具有强还原性,氧化产物为N2;
③沉淀的生成速率越快,颗粒越小,呈凝乳状成胶体,不易过滤。
(1)以废旧锂电池正极材料为原料制备CoSO4溶液。取一定量废旧锂电池正极材料,粉碎后与Na2SO3溶液混合配成悬浊液,边搅拌边加入1 mol/LH2SO4溶液充分反应。LiCoO2转化为CoSO4、Li2SO4的化学方程式为
(2)60℃时在搅拌下向CoSO4溶液中加入氨水,调节pH至6后,再加入NaOH溶液,调节pH至9.5左右,一段时间后,过滤、洗涤,真空烘干得微米级Co(OH)2。制备时,在加入NaOH溶液前必须先加氨水的原因是
(3)经仪器分析,测得按题(2)步骤制得的Co(OH)2晶体结构中含有Co(III),进一步用碘量法测得Co(II)的氧化程度为8%。因此制备时必须加入一定量的还原剂。
将500 mL1 mol/L的CoSO4溶液与氨水配成pH为6的溶液,加入三颈烧瓶中(装置如图),滴液漏斗a装有NaOH溶液、b中装有水合肼,60℃时依次将两种溶液加入三颈烧瓶,充分反应后,过滤,实验时应先打开滴液漏斗

(4)利用含钴废料(主要成分为Co3O4,还含有少量的石墨、LiCoO2等杂质)制备碳酸钴CoCO3。
已知:①CoCO3几乎不溶于水,Li2CO3微溶于水,Co2+(以0.1 mol/L)开始沉淀的pH为7.6;
②钴、锂在有机磷萃取剂(HR)中的萃取率与pH的关系如图所示;

③酸性条件下的氧化性强弱顺序为:Co3+>H2O2。
请补充完整实验方案:取一定量含钴废料,粉碎后
实验中可选用的试剂:2 mol/L H2SO4溶液、2 mol/LNaOH溶液、有机磷(HR)、5 mol/L Na2CO3溶液、0.5 mol/LNa2CO3溶液、30%H2O2溶液。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】有四种短周期元素,相关信息如下表。
请根据表中信息回答:
(1)用电子式表示B与C形成化合物的过程:___________ 。
(2)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是(填化学式)___________ 。
(3)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是___________ 。
a.其单质在常温下呈固态 b.SeO2既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为H2SeO3 d.非金属性比S元素的强
| 元素 | 相关信息 |
| A | 气态氢化物极易溶于水,可用作制冷剂 |
| B | 单质的焰色反应为黄色 |
| C | 单质是黄绿色气体,可用于自来水消毒 |
| D | –2价阴离子的电子层结构与Ar原子相同 |
(1)用电子式表示B与C形成化合物的过程:
(2)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是(填化学式)
(3)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
a.其单质在常温下呈固态 b.SeO2既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为H2SeO3 d.非金属性比S元素的强
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】I.甲元素的原子序数是19,乙元素原子核外有两个电子层,最外电子层上有6个电子;丙是短周期元素中金属性最强的元素。由此推断:
(1)甲元素在周期表中位于第________ 周期;乙元素在周期表中位于第______ 族;丙元素的名称为________ ,丙的原子结构示意图为__________ 。
(2)甲的单质与水反应的离子方程式为________________ ;
乙单质与丙单质加热反应的化学方程式为________________ 。
II.最新报道,我国科学家通过与多个国家进行科技合作,成功研发出铯(Cs)原子喷泉钟,使我国时间频率基准的精度从30万年不差1秒提高到600万年不差1秒,标志着我国时间频率基准研究进入世界先进行列。已知铯位于元素周期表中第六周期第ⅠA族,根据铯在元素周期表中的位置,推断下列内容:
(1)铯的原子核外共有_________ 层电子,最外层电子数为_________ ,铯的原子序数为________ 。
(2)铯单质与水剧烈反应,放出________ 色气体,同时使紫色石蕊试液显________ 色,因为________________ (写出化学方程式)。
(3)预测铯单质的还原性比钠单质的还原性________ (填“弱”或“强”)。
(1)甲元素在周期表中位于第
(2)甲的单质与水反应的离子方程式为
乙单质与丙单质加热反应的化学方程式为
II.最新报道,我国科学家通过与多个国家进行科技合作,成功研发出铯(Cs)原子喷泉钟,使我国时间频率基准的精度从30万年不差1秒提高到600万年不差1秒,标志着我国时间频率基准研究进入世界先进行列。已知铯位于元素周期表中第六周期第ⅠA族,根据铯在元素周期表中的位置,推断下列内容:
(1)铯的原子核外共有
(2)铯单质与水剧烈反应,放出
(3)预测铯单质的还原性比钠单质的还原性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下图是元素周期表的一部分,元素①~⑨在周期表中的位置如图所示,请回答下列问题:
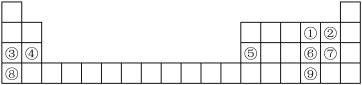
(1)元素⑨在周期表中的位置是_______ 。
(2)元素①~⑨中,非金属性最强的元素是_______ (填元素符号)。
(3)元素①~⑨中,最高价氧化物对应的水化物中,碱性最强的是_______ (填化学式),它与元素⑤的最高价氧化物对应水化物反应的离子方程式为_______ 。
(4)元素⑨的简单氢化物与元素⑦的简单氢化物中更稳定的是_______ (填化学式)。
(5)元素③与元素①形成的淡黄色化合物的电子式为_______ 。
(6)元素①的简单氢化物比元素⑥的简单氢化物的沸点_______ (填“高”或“低”),原因是_______ 。
(7)元素④与元素⑦形成的化合物是_______ (填“离子”或“共价”)化合物,用电子式表示其形成过程_______ 。

(1)元素⑨在周期表中的位置是
(2)元素①~⑨中,非金属性最强的元素是
(3)元素①~⑨中,最高价氧化物对应的水化物中,碱性最强的是
(4)元素⑨的简单氢化物与元素⑦的简单氢化物中更稳定的是
(5)元素③与元素①形成的淡黄色化合物的电子式为
(6)元素①的简单氢化物比元素⑥的简单氢化物的沸点
(7)元素④与元素⑦形成的化合物是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】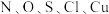 五种元素的单质及其化合物在现代工业生产中有着广泛应用。请回答下列问题:
五种元素的单质及其化合物在现代工业生产中有着广泛应用。请回答下列问题:
(1)第一电离能:N_______ (填“>”或“<”,下同)O,电负性:O_______ S。
(2) 极易溶于水的原因是
极易溶于水的原因是_______ ; 属于
属于_______ (填“极性”或“非极性”)分子,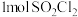 含有
含有 的键为
的键为_______  。
。
(3) 的空间构型是
的空间构型是_______ , 的中心原子的杂化方式为
的中心原子的杂化方式为_______ 。
(4)与 互为等电子体的微粒有
互为等电子体的微粒有_______ (任写两种)。
(5) 与
与 形成化合物的晶胞如图所示。
形成化合物的晶胞如图所示。
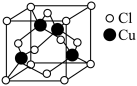
该晶体的化学式为_______ .已知该晶体中 原子和
原子和 原子之间的最短距离为
原子之间的最短距离为 ,且恰好为体对角线的
,且恰好为体对角线的 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体的密度为
,则该晶体的密度为_______ (只写计算式) 。
。
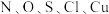 五种元素的单质及其化合物在现代工业生产中有着广泛应用。请回答下列问题:
五种元素的单质及其化合物在现代工业生产中有着广泛应用。请回答下列问题:(1)第一电离能:N
(2)
 极易溶于水的原因是
极易溶于水的原因是 属于
属于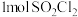 含有
含有 的键为
的键为 。
。(3)
 的空间构型是
的空间构型是 的中心原子的杂化方式为
的中心原子的杂化方式为(4)与
 互为等电子体的微粒有
互为等电子体的微粒有(5)
 与
与 形成化合物的晶胞如图所示。
形成化合物的晶胞如图所示。
该晶体的化学式为
 原子和
原子和 原子之间的最短距离为
原子之间的最短距离为 ,且恰好为体对角线的
,且恰好为体对角线的 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体的密度为
,则该晶体的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】研究发现,在 低压合成甲醇反应(
低压合成甲醇反应(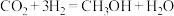 )中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)基态Co原子的价电子排布式为_______ 。基态Mn原子核外有_______ 个未成对电子。
(2)在 低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_______ ,原因是_______ 。
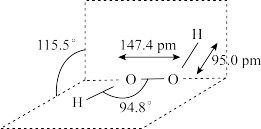
(3) 是一种无色液体,其结构如图所示。根据“相似相溶规则”,
是一种无色液体,其结构如图所示。根据“相似相溶规则”, 在水中的溶解度
在水中的溶解度_______ (填“大于”“小于”或“等于”)其在 中的溶解度。
中的溶解度。
 低压合成甲醇反应(
低压合成甲醇反应(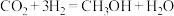 )中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:(1)基态Co原子的价电子排布式为
(2)在
 低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为(3)
 是一种无色液体,其结构如图所示。根据“相似相溶规则”,
是一种无色液体,其结构如图所示。根据“相似相溶规则”, 在水中的溶解度
在水中的溶解度 中的溶解度。
中的溶解度。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
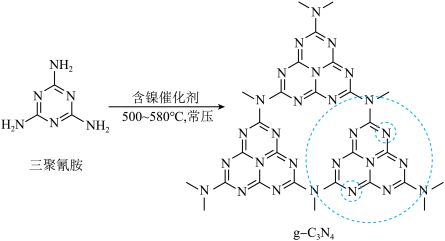
【推荐3】石墨相(类似石墨的二维层状结构)光催化材料 在光电池方面应用广泛,进一步研究发现,非金属掺杂(O、S等)能提高其光催化活性。
在光电池方面应用广泛,进一步研究发现,非金属掺杂(O、S等)能提高其光催化活性。
(1)若将基态氮原子的电子轨道表示式画为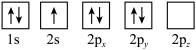 ,该排布图违背的规则或原理有
,该排布图违背的规则或原理有___________ 。
(2)N、O、S的第一电离能从大到小的顺序为___________ 。
(3)三聚氰胺属于___________ 晶体,属于___________ (填“极性”或“非极性”)分子。
(4)三聚氰胺难溶于冷水,但能溶于热水,原因可能为___________ (从氢键角度解释)。
(5)每个基本结构单元(图中虚线大圈部分)中两个N原子(图中虚线小圈部分)被O原子代替,形成O掺杂的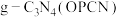 ,则OPCN中
,则OPCN中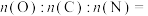
___________ 。
(6)镍的某种氧化物常用作催化剂,其立方晶胞结构如图所示:
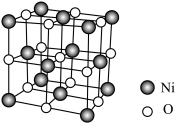
已知该晶体的密度为 ,
, 为阿伏加德罗常数的值,该晶胞的参数为
为阿伏加德罗常数的值,该晶胞的参数为___________ pm(用含 、
、 的代数式表示)。
的代数式表示)。
 在光电池方面应用广泛,进一步研究发现,非金属掺杂(O、S等)能提高其光催化活性。
在光电池方面应用广泛,进一步研究发现,非金属掺杂(O、S等)能提高其光催化活性。
(1)若将基态氮原子的电子轨道表示式画为
 ,该排布图违背的规则或原理有
,该排布图违背的规则或原理有(2)N、O、S的第一电离能从大到小的顺序为
(3)三聚氰胺属于
(4)三聚氰胺难溶于冷水,但能溶于热水,原因可能为
(5)每个基本结构单元(图中虚线大圈部分)中两个N原子(图中虚线小圈部分)被O原子代替,形成O掺杂的
 ,则OPCN中
,则OPCN中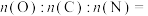
(6)镍的某种氧化物常用作催化剂,其立方晶胞结构如图所示:

已知该晶体的密度为
 ,
, 为阿伏加德罗常数的值,该晶胞的参数为
为阿伏加德罗常数的值,该晶胞的参数为 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次



