实验室用草酸与浓硫酸反应制备 ,其原理如下:
,其原理如下: 。某课题组同学设计实验探究
。某课题组同学设计实验探究 还原磷石膏(
还原磷石膏( )并检验气体产物[
)并检验气体产物[ 能被
能被 悬浊液吸收生成
悬浊液吸收生成 ],装置如图所示。
],装置如图所示。
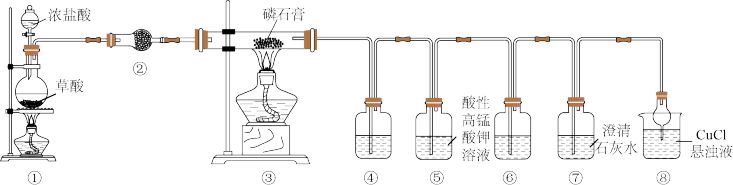
(1)在实验室中利用装置①还可制取的气体有__________ (填一种即可)。
(2)装置②中盛放的试剂为_________ ,装置④⑥中盛放的试剂均为品红溶液,其作用分别为________________ 、________________ 。
(3)若装置④中溶液褪色,装置⑥中溶液不褪色,装置⑦中溶液变浑浊,则装置③中发生反应的化学方程式为_________________________ 。
(4)装置⑤中发生反应的离子方程式为_________________________ 。
(5)实验结束时,先熄灭____________ (填“①”或“③”)处的酒精灯,其目的为_________________ 。
 ,其原理如下:
,其原理如下: 。某课题组同学设计实验探究
。某课题组同学设计实验探究 还原磷石膏(
还原磷石膏( )并检验气体产物[
)并检验气体产物[ 能被
能被 悬浊液吸收生成
悬浊液吸收生成 ],装置如图所示。
],装置如图所示。
(1)在实验室中利用装置①还可制取的气体有
(2)装置②中盛放的试剂为
(3)若装置④中溶液褪色,装置⑥中溶液不褪色,装置⑦中溶液变浑浊,则装置③中发生反应的化学方程式为
(4)装置⑤中发生反应的离子方程式为
(5)实验结束时,先熄灭
更新时间:2020-12-11 11:22:49
|
相似题推荐
【推荐1】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。(已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O)

(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是___________ 、___________ 。
(2)反应后,装置B中反应的离子方程式 为___________ ;装置C中发生反应的化学方程式 为___________ ;装置D中发生反应的化学方程式 为___________ 。
(3)装置E的目的是探究SO2与品红作用的可逆性, 请写出实验操作 及现象 _________ 。
(4)F装置的作用是___________ ,其中漏斗的作用是___________ 。

(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是
(2)反应后,装置B中反应的
(3)装置E的目的是探究SO2与品红作用的
(4)F装置的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室为探究铁与浓硫酸的反应,并验证SO2的性质,设计如图所示装置进行实验。
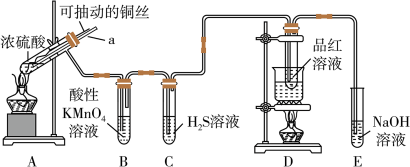
请回答下列问题:
(1)装置A中的反应,浓硫酸体现了___________ 性和___________ 性。
(2)装置B中酸性KMnO4溶液逐渐褪色,证明SO2具有___________ 性;装置C中发生反应的化学方程式___________ 。
(3)装置D的作用是___________ ;实验结束时需从导管a通入大量空气,其目的是___________ 。
(4)装置E中NaOH溶液足量,写出E中反应的离子方程式___________ 。
(5)SO2溶于水生成H2SO3,已知酸性H2SO3>H2CO3>HClO,为了证明酸性H2SO3>HClO,将SO2通入到下列试剂,下列试剂排序正确的是___________(填选项)。
①小苏打溶液 ②品红溶液 ③酸性KMnO4溶液 ④漂白粉溶液

请回答下列问题:
(1)装置A中的反应,浓硫酸体现了
(2)装置B中酸性KMnO4溶液逐渐褪色,证明SO2具有
(3)装置D的作用是
(4)装置E中NaOH溶液足量,写出E中反应的离子方程式
(5)SO2溶于水生成H2SO3,已知酸性H2SO3>H2CO3>HClO,为了证明酸性H2SO3>HClO,将SO2通入到下列试剂,下列试剂排序正确的是___________(填选项)。
①小苏打溶液 ②品红溶液 ③酸性KMnO4溶液 ④漂白粉溶液
| A.②①③④ | B.③②①④ | C.①③②④ | D.④③②① |
您最近一年使用:0次
【推荐3】 2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:
2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:
(1)硫酸亚铁加热至高温会分解,生成三种氧化物。为探究硫酸亚铁的分解产物,将无水硫酸亚铁装入反应管A并连接如图所示的装置,打开 1和
1和 2,缓缓通入
2,缓缓通入 2,加热。实验后反应管A中残留的固体为红色粉末
2,加热。实验后反应管A中残留的固体为红色粉末
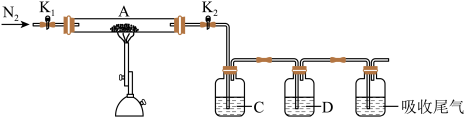
①装置C的溶液为_______ (填标号)。装置D可观察到的实验现象为_______ 。
a.品红 b.NaOH c. 2 d.
2 d. e.浓硫酸
e.浓硫酸
②写出硫酸亚铁高温分解的化学方程式_______ 。
(2)某兴趣小组用如图所示装置模拟测定空气中的二氧化硫的含量。当注入标准状况下VmL空气时,酸性 4溶液恰好褪色,停止实验。
4溶液恰好褪色,停止实验。
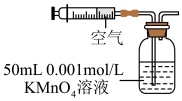
①二氧化硫和酸性 4溶液反应的离子方程式为
4溶液反应的离子方程式为_______ 。
②该空气中二氧化硫的体积分数为_______ (用含Ⅴ的代数式表示)。
(3)某化工厂用如图所示工艺流程除去燃煤产生的 2。
2。

①过程I发生的反应中,氧化剂与还原剂的物质的量之比为_______ 。
②过程Ⅱ发生反应的化学方程式为_______ 。
 2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:
2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:(1)硫酸亚铁加热至高温会分解,生成三种氧化物。为探究硫酸亚铁的分解产物,将无水硫酸亚铁装入反应管A并连接如图所示的装置,打开
 1和
1和 2,缓缓通入
2,缓缓通入 2,加热。实验后反应管A中残留的固体为红色粉末
2,加热。实验后反应管A中残留的固体为红色粉末
①装置C的溶液为
a.品红 b.NaOH c.
 2 d.
2 d. e.浓硫酸
e.浓硫酸②写出硫酸亚铁高温分解的化学方程式
(2)某兴趣小组用如图所示装置模拟测定空气中的二氧化硫的含量。当注入标准状况下VmL空气时,酸性
 4溶液恰好褪色,停止实验。
4溶液恰好褪色,停止实验。
①二氧化硫和酸性
 4溶液反应的离子方程式为
4溶液反应的离子方程式为②该空气中二氧化硫的体积分数为
(3)某化工厂用如图所示工艺流程除去燃煤产生的
 2。
2。
①过程I发生的反应中,氧化剂与还原剂的物质的量之比为
②过程Ⅱ发生反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
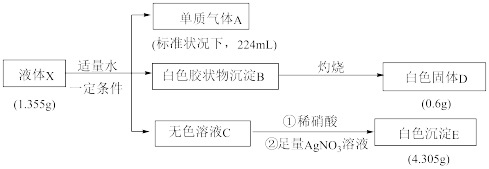
【推荐1】某同学用固体X(四种元素组成的纯净物)进行了如下实验:
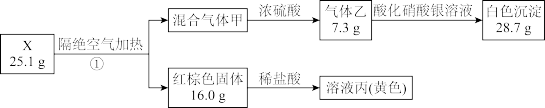
请回答:
(1)混合气体甲的化学成分为_______ 。
(2)步骤①的化学方程式是_______ 。
(3)已知往溶液丙中通入二氧化硫气体黄色会褪去,写出该反应的离子方程式_______ 。

请回答:
(1)混合气体甲的化学成分为
(2)步骤①的化学方程式是
(3)已知往溶液丙中通入二氧化硫气体黄色会褪去,写出该反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】《物理小识·金石类》记载:“青矾厂气熏人,衣服当之易烂,载木不盛”,“青矾强热,得赤色固体,气凝即得矾油”。“青矾”是指FeSO4·7H2O,“青矾厂气”是指SO2和SO3,“矾油”是指硫酸溶液。实验室模拟古法制硫酸并进行SO2性质探究。

已知:SO2熔点-75.5℃,沸点-10℃;SO3熔点16.8℃,沸点44.8℃。
回答下列问题:
Ⅰ.制取硫酸
实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活塞K3,用酒精喷灯高温加热青矾。
(1)A装置中反应后所得固体的化学式为______ 。玻璃纤维的作用是______ 。
(2)B装置的作用_____ 。
(3)D装置的作用是______ 。
Ⅱ.探究SO2的性质
在装置C中先后使用同体积的蒸馏水(①已预先煮沸,②未预先煮沸),控制食用油油层厚度一致、通入SO2流速一致。两次实验分别得到如图pH-t图:

(4)C装置中覆盖食用油的目的是______ 。
(5)pH-t图中,②的曲线出现骤降,这是因为______ (用化学方程式表示)。对比分析上述两组数据,可得出的结论是______ 。

已知:SO2熔点-75.5℃,沸点-10℃;SO3熔点16.8℃,沸点44.8℃。
回答下列问题:
Ⅰ.制取硫酸
实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活塞K3,用酒精喷灯高温加热青矾。
(1)A装置中反应后所得固体的化学式为
(2)B装置的作用
(3)D装置的作用是
Ⅱ.探究SO2的性质
在装置C中先后使用同体积的蒸馏水(①已预先煮沸,②未预先煮沸),控制食用油油层厚度一致、通入SO2流速一致。两次实验分别得到如图pH-t图:

(4)C装置中覆盖食用油的目的是
(5)pH-t图中,②的曲线出现骤降,这是因为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某化学小组用如图所示装置制取连二亚硫酸钠( )。
)。

已知:①连二亚硫酸钠:淡黄色粉末,具有较强的还原性,不溶于醇,遇水会分解,在碱性介质中较稳定。
②在碱性溶液中,低于52℃时 以
以 形态结晶,高于52℃时
形态结晶,高于52℃时 脱水成无水盐。
脱水成无水盐。
回答下列问题:
(1)Ⅰ.安装好装置,并检验装置气密性,然后再加入相应的试剂。橡胶管a的作用是_______ ,单向阀的作用是_______ ,下列装置不能代替单向阀的是_______ (填字母)。
A. B.
B. C.
C. D.
D.
Ⅱ.打开B装置的活塞,向三颈烧瓶中滴加_______ (填“少量”或“过量”)的 溶液;
溶液;
Ⅲ.打开A装置的活塞,控制B装置内溶液的温度在60~70℃之间,即可生成 。写出此步骤中生成
。写出此步骤中生成 的化学方程式为:
的化学方程式为:_______ 。
Ⅳ.过滤,经洗涤、_______ (填操作名称)后获得 。简述洗涤步骤:在无氧环境中
。简述洗涤步骤:在无氧环境中_______ 。
(2) 在潮湿空气中被氧化,生成
在潮湿空气中被氧化,生成 和
和_______ 两种常见酸式盐。
 )。
)。
已知:①连二亚硫酸钠:淡黄色粉末,具有较强的还原性,不溶于醇,遇水会分解,在碱性介质中较稳定。
②在碱性溶液中,低于52℃时
 以
以 形态结晶,高于52℃时
形态结晶,高于52℃时 脱水成无水盐。
脱水成无水盐。回答下列问题:
(1)Ⅰ.安装好装置,并检验装置气密性,然后再加入相应的试剂。橡胶管a的作用是
A.
 B.
B. C.
C. D.
D.
Ⅱ.打开B装置的活塞,向三颈烧瓶中滴加
 溶液;
溶液;Ⅲ.打开A装置的活塞,控制B装置内溶液的温度在60~70℃之间,即可生成
 。写出此步骤中生成
。写出此步骤中生成 的化学方程式为:
的化学方程式为:Ⅳ.过滤,经洗涤、
 。简述洗涤步骤:在无氧环境中
。简述洗涤步骤:在无氧环境中(2)
 在潮湿空气中被氧化,生成
在潮湿空气中被氧化,生成 和
和
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】绿矾(FeSO4·7H2O)可作还原剂、着色剂、制药等,在不同温度下易分解得各种铁的氧化物和硫的氧化物。已知SO3是一种无色晶体,熔点16.8℃,沸点44.8℃,氧化性及脱水性较浓硫酸强,能漂白某些有机染料,如品红等。回答下列问题:
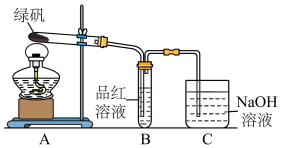
(1)甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置B中可观察到的现象是_____________________________________________ ,甲组由此得出绿矾的分解产物中含有SO2。装置C的作用是______________________________ 。
(2)乙组同学认为甲组同学的实验结论不严谨,认为需要补做实验。乙对甲组同学做完实验的装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中______ 。
A.不含SO2 B.可能含SO2 C.一定含有SO3
(3)丙组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,丙组同学选用甲组同学的部分装置 和下图部分装置 设计出了一套检验绿矾分解气态产物的装置:
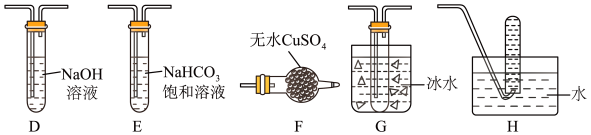
丙组同学的实验装置中,依次连接的合理顺序为A→_______ ;其中仪器F的名称___________ 。

(1)甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置B中可观察到的现象是
(2)乙组同学认为甲组同学的实验结论不严谨,认为需要补做实验。乙对甲组同学做完实验的装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中
A.不含SO2 B.可能含SO2 C.一定含有SO3
(3)丙组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,丙组同学选用

丙组同学的实验装置中,依次连接的合理顺序为A→
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】水蒸气通过的灼热的焦炭后,流出气体的主要成分是 CO 和 H2,还有 CO2和水蒸气等。现利用下图中提供实验装置,证明上述混合气体中有CO 和 H2。(A中加热装置在图中略去)回答下列问题:

(1) C装置的用途是____________
(2)仪器 E 中需加入的试剂是_____________
(3)仪器 F 中需加入的试剂是:______ ,其目的是_________________
(4)装置F和G的位置能否颠倒_____ ,(填“能”或“否”)理由是____________________
(5)能证明混合气中含有 CO 的实验现象是________________________
(6)有人认为该实验装置存在一个缺陷,你认为这个缺陷是___________

(1) C装置的用途是
(2)仪器 E 中需加入的试剂是
(3)仪器 F 中需加入的试剂是:
(4)装置F和G的位置能否颠倒
(5)能证明混合气中含有 CO 的实验现象是
(6)有人认为该实验装置存在一个缺陷,你认为这个缺陷是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】沉淀碳酸钙主要用于食品、医药等行业。以精选石灰石(含有少量MgCO3、FeCO3杂质)为原料制备沉淀碳酸钙的工艺流程如下:
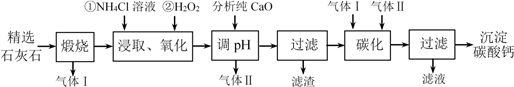
(1)流程中可以循环利用的物质有气体Ⅰ、气体Ⅱ和__________ (填化学式)。
(2)“碳化”时发生反应的离子方程式为________________ ,该过程中通入气体Ⅰ和气体Ⅱ的顺序是________________ 。
(3)工业上常用电解氯化钠和氯化钙熔融物来制备金属钠,原理如下图所示:

①电解过程中,加入氯化钙的目的是________________ 。
②石墨电极发生的电极反应方程式为________________ 。
③电解得到的Na中约含1%的Ca,除去其中少量Ca的方法为________________ 。
已知部分物质的熔沸点如下表:
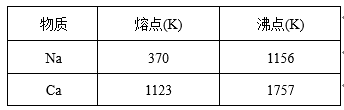

(1)流程中可以循环利用的物质有气体Ⅰ、气体Ⅱ和
(2)“碳化”时发生反应的离子方程式为
(3)工业上常用电解氯化钠和氯化钙熔融物来制备金属钠,原理如下图所示:

①电解过程中,加入氯化钙的目的是
②石墨电极发生的电极反应方程式为
③电解得到的Na中约含1%的Ca,除去其中少量Ca的方法为
已知部分物质的熔沸点如下表:

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】MnSO4∙H2O是一种易溶于水的微红色斜方晶体,实验室用SO2还原MnO2制备MnSO4。甲同学设计如图所示装置制备硫酸锰。
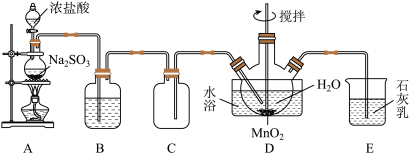
请回答下列有关问题:
(1)仪器组装好后首先进行的操作是___________ 。
(2)装置B中的试剂为___________ ,装置E的作用为___________ 。
(3)装置D中发生反应的化学方程式为___________ 。要从D中获得纯净的MnSO4∙H2O,应在观察到___________ 现象时停止通入SO2。
(4)装置D中水浴温度应控制在80°C左右,温度不能过高的原因是___________ 。
(5)将MnSO4∙H2O配成溶液测定NaBiO3产品的纯度。取3.2 g NaBiO3产品,用足量硫酸和MnSO4溶液使其还原为Bi3+,再将其准确配制成100 mL溶液,取出25.00 mL,用0.1000 mol·L-1 H2C2O4标准溶液滴定生成的MnO4-,滴定终点时消耗25.00 mL H2C2O4标准溶液,则滴定过程发生反应的离子方程式为___________ ,该产品的纯度为___________ 。

请回答下列有关问题:
(1)仪器组装好后首先进行的操作是
(2)装置B中的试剂为
(3)装置D中发生反应的化学方程式为
(4)装置D中水浴温度应控制在80°C左右,温度不能过高的原因是
(5)将MnSO4∙H2O配成溶液测定NaBiO3产品的纯度。取3.2 g NaBiO3产品,用足量硫酸和MnSO4溶液使其还原为Bi3+,再将其准确配制成100 mL溶液,取出25.00 mL,用0.1000 mol·L-1 H2C2O4标准溶液滴定生成的MnO4-,滴定终点时消耗25.00 mL H2C2O4标准溶液,则滴定过程发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】苯甲酸乙酯可由苯甲酸与乙醇在浓硫酸共热下反应制得,反应装置如图(部分装置省 略),反应原理如下:
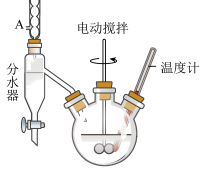
 +C2H5OH
+C2H5OH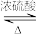
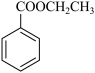 +H2O
+H2O
实验操作步骤:
向三颈烧瓶内加入12.2g 苯甲酸、25mL乙醇、20mL 苯及4mL浓硫酸,摇匀,加入沸石。
①装上分水器、电动搅拌器和温度计,加热至分水器下层液体接近支管时将下层液体放入量筒 中,继续蒸馏,蒸出过量的乙醇,至瓶内有白烟(约3h),停止加热。
②将反应液倒入盛有80mL冷水的烧瓶中,在搅拌下分批加入碳酸钠粉末溶液至溶液无二氧化 碳逸出,用 pH 试纸检验至中性。
③用分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层,用无水CaCl2干燥,粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接受210-213℃的馏分,最终通过蒸馏得到纯净苯甲酸乙酯12.8mL。
可能用到的有关数据如下:
(1)反应装置中分水器上方的仪器名称是_______ ,其作用是______ 。
(2)步骤①中加入浓硫酸的作用是______ ,步骤②中电动搅拌棒的作用是_______ 。
(3)步骤②中使用分水器除水的目的是______ 。
(4)步骤③中加入碳酸钠的目的是______ 。
(5)有机层从分液漏斗的_______ (选填“上口倒出”或“下口放出”)
(6)本实验所得到的苯甲酸乙酯的产率是_______ 。

 +C2H5OH
+C2H5OH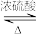
 +H2O
+H2O实验操作步骤:
向三颈烧瓶内加入12.2g 苯甲酸、25mL乙醇、20mL 苯及4mL浓硫酸,摇匀,加入沸石。
①装上分水器、电动搅拌器和温度计,加热至分水器下层液体接近支管时将下层液体放入量筒 中,继续蒸馏,蒸出过量的乙醇,至瓶内有白烟(约3h),停止加热。
②将反应液倒入盛有80mL冷水的烧瓶中,在搅拌下分批加入碳酸钠粉末溶液至溶液无二氧化 碳逸出,用 pH 试纸检验至中性。
③用分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层,用无水CaCl2干燥,粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接受210-213℃的馏分,最终通过蒸馏得到纯净苯甲酸乙酯12.8mL。
可能用到的有关数据如下:
| 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
| 苯甲酸 | 122 | 1.27 | 249 | 微溶于水,易溶于乙醇、乙醚 |
| 苯甲酸乙酯 | 150 | 1.05 | 211-213 | 微溶于热水,易溶于乙醇、乙醚 |
| 乙醇 | 46 | 0.79 | 78.5 | 易溶于水 |
| 乙醚 | 74 | 0.73 | 34.5 | 微溶于水 |
(2)步骤①中加入浓硫酸的作用是
(3)步骤②中使用分水器除水的目的是
(4)步骤③中加入碳酸钠的目的是
(5)有机层从分液漏斗的
(6)本实验所得到的苯甲酸乙酯的产率是
您最近一年使用:0次