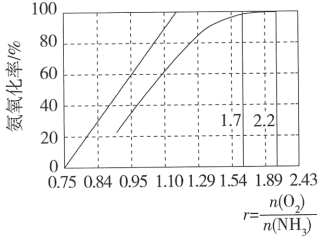
FePO4 是制备锂离子电池的原料。向 FeSO4 溶液中先加入 H3PO4 溶液,再加入 NaOH、NaClO 的混合液可制取 FePO4。
(1)配平下列反应方程式:FeSO4+H3PO4+NaClO+NaOH→FePO4↓+Na2SO4+NaCl+H2O,____________________ 。
(2)NaOH、NaClO 的混合液可通过 Cl2 与 NaOH 溶液反应制取。若 NaOH、NaClO混合液中NaClO含量偏低,则制得的 FePO4 中含有的不溶性杂质主要是_______ 。
(3)现有 500 mL 1.2mol/LNaOH 溶液,若要制取反应所需的混合液,则需通入标准状况下 Cl2 的体积为__________ 。
(1)配平下列反应方程式:FeSO4+H3PO4+NaClO+NaOH→FePO4↓+Na2SO4+NaCl+H2O,
(2)NaOH、NaClO 的混合液可通过 Cl2 与 NaOH 溶液反应制取。若 NaOH、NaClO混合液中NaClO含量偏低,则制得的 FePO4 中含有的不溶性杂质主要是
(3)现有 500 mL 1.2mol/LNaOH 溶液,若要制取反应所需的混合液,则需通入标准状况下 Cl2 的体积为
2021·上海闵行·一模 查看更多[1]
更新时间:2020-12-23 02:00:28
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】填空:
(1)在1 L 0.1 mol/L的AlCl3溶液中加入240 mL 1 mol/L的NaOH溶液,则铝元素中的存在形式___________ 生成Al(OH)3___________ mol;
(2)在1 L 0.1 mol/L的AlCl3溶液中加入340 mL 1 mol/L的NaOH溶液,则铝元素中的存在形式___________ 生成Al(OH)3___________ mol;
(3)在1 L 0.1 mol/L的AlCl3溶液中加入440 mL 1 mol/L的NaOH溶液,则铝元素中的存在形式___________ 生成Al(OH)3___________ mol。
(1)在1 L 0.1 mol/L的AlCl3溶液中加入240 mL 1 mol/L的NaOH溶液,则铝元素中的存在形式
(2)在1 L 0.1 mol/L的AlCl3溶液中加入340 mL 1 mol/L的NaOH溶液,则铝元素中的存在形式
(3)在1 L 0.1 mol/L的AlCl3溶液中加入440 mL 1 mol/L的NaOH溶液,则铝元素中的存在形式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀的物质的量(n)和加入溶液B的体积(V)关系如图。

(1)当加入B溶液110mL时,溶液中的沉淀为(化学式)_______
(2)溶液B中Na2SO4与NaOH的物质的量浓度之比_______ ,从90mL至100mL之间加入10mLB溶液时发生的离子反应方程式_______
(3)将A、B溶液中各溶质的物质的量浓度填入下表

(1)当加入B溶液110mL时,溶液中的沉淀为(化学式)
(2)溶液B中Na2SO4与NaOH的物质的量浓度之比
(3)将A、B溶液中各溶质的物质的量浓度填入下表
| 溶质 | Na2SO4 | BaCl2 | FeCl3 |
| c(mol/L) |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.ClO2可由KClO3在H2SO4存在的条件下与Na2SO3反应制得。则该反应的氧化产物与还原产物的物质的量之比是______ 。
Ⅱ.已知一定条件下可以发生下列反应:H2O2+2Fe2++2H+=2Fe3++2H2O、H2O2+2Fe3+=2Fe2++2H++O2↑
(1)与上述反应类比,I2也能与H2O2发生类似反应。请在空格处填入合适的化学方程式:H2O2+I2=2HIO;____ ;总反应的化学方程式为_______ 。
(2)在H2SO4和KI的混合溶液中加入过量的H2O2,放出大量的无色气体,溶液呈棕色,并可以使淀粉溶液变蓝。有同学认为该反应的离子方程式为H2O2+2I-=I2+O2↑+2H+,该离子方程式是否正确____ (填“正确”或“不正确”),理由是______ 。
(3)在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式为____ 。
Ⅱ.已知一定条件下可以发生下列反应:H2O2+2Fe2++2H+=2Fe3++2H2O、H2O2+2Fe3+=2Fe2++2H++O2↑
(1)与上述反应类比,I2也能与H2O2发生类似反应。请在空格处填入合适的化学方程式:H2O2+I2=2HIO;
(2)在H2SO4和KI的混合溶液中加入过量的H2O2,放出大量的无色气体,溶液呈棕色,并可以使淀粉溶液变蓝。有同学认为该反应的离子方程式为H2O2+2I-=I2+O2↑+2H+,该离子方程式是否正确
(3)在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮的氢化物种类繁多,其中联氨(又称肼,N2H4,无色油状液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为__________________ ,其中氮的化合价为 _________ 。
(2) ①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2(g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=____________________ ,联氨和N2O4可作为火箭推进剂的主要原因为_________________________________________ 。
(3)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是固体逐渐变黑,并且有气泡产生,写出该反应的化学方程式__________________ 。
(4)联氨还可以用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2_____ kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是__________ 。
(1)联氨分子的电子式为
(2) ①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2(g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=
(3)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是固体逐渐变黑,并且有气泡产生,写出该反应的化学方程式
(4)联氨还可以用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)在一个绝热、容积不变的密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g)△H<0。下列各项能说明该反应已经达到平衡状态的是
2NH3(g)△H<0。下列各项能说明该反应已经达到平衡状态的是
B、容器内温度不再变化
C、断裂1mol N≡N键的同时,生成6mol N﹣H键
D、反应消耗N2、H2与产生NH3的速率之比1:3:2
(2)已知:①Zn(s)+1/2O2(g) = ZnO(s) △H =-348.3 kJ/mol
②2Ag(s)+1/2O2(g) = Ag2O(s) △H =-31.0 kJ/mol
则Zn(s)+Ag2O(s) = ZnO(s)+2Ag(s)的△H=
(3)已知两个热化学方程式:
C(s)+O2(g)==CO2(g) △H = -393.5kJ/mol
2H2(g)+O2(g)==2H2O(g)△H = -483.6kJ/mol
现有0.2mol炭粉和H2组成悬浮气,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是
(4)在水溶液中,YO3n-和S2-发生反应的离子方程式如下:YO3n- + 3S2- + 6H+ = Y-+ 3S↓+ 3H2O
①YO3n-中Y的化合价是
②Y元素原子的最外层电子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】写出下列反应的离子方程式:
(1)向碳酸钠溶液中滴加少量醋酸(CH3COOH):______ 。
(2)向碳酸氢钠溶液中滴加少量澄清石灰水:______ 。
(3)制漂白液:______ 。
(4)工业上制作印刷电路板的原理:______ 。
(1)向碳酸钠溶液中滴加少量醋酸(CH3COOH):
(2)向碳酸氢钠溶液中滴加少量澄清石灰水:
(3)制漂白液:
(4)工业上制作印刷电路板的原理:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】含氯消毒剂、过氧化物能有效灭活病毒,是常用消毒剂。请回答下列问题:
(1)消毒剂次氯酸钠可由氯气和NaOH溶液反应制得,反应的化学方程式为________ 。
(2)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可由Cl2O与ClO2按一定比例混合后在NaOH溶液中反应制得。
①NaClO2中氯元素的化合价是________ 。
②制备时Cl2O与ClO2完全反应的物质的量理论比为________ 。
(3)兴趣小组设计如下图实验装置制取少量消毒液。
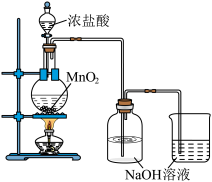
①MnO2与浓HCl反应的离子方程式为________ 。
②充分反应后,测得消毒液中NaCl与NaClO的物质的量之比大于1。可能的原因有________ (用文字简述)。
(4)Na2O2在呼吸面具中作供氧剂使用,若有7.8 g Na2O2参加反应,则转移的电子的物质的量为________ 。
(1)消毒剂次氯酸钠可由氯气和NaOH溶液反应制得,反应的化学方程式为
(2)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可由Cl2O与ClO2按一定比例混合后在NaOH溶液中反应制得。
①NaClO2中氯元素的化合价是
②制备时Cl2O与ClO2完全反应的物质的量理论比为
(3)兴趣小组设计如下图实验装置制取少量消毒液。

①MnO2与浓HCl反应的离子方程式为
②充分反应后,测得消毒液中NaCl与NaClO的物质的量之比大于1。可能的原因有
(4)Na2O2在呼吸面具中作供氧剂使用,若有7.8 g Na2O2参加反应,则转移的电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验室制备氯酸钾、次氯酸钠和氯水的装置如图所示。
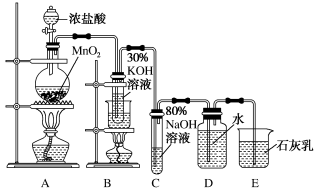
制备KClO3需在70~80℃进行,写出制备KClO3的离子方程式:___ 。

制备KClO3需在70~80℃进行,写出制备KClO3的离子方程式:
您最近一年使用:0次