含氯消毒剂、过氧化物能有效灭活病毒,是常用消毒剂。请回答下列问题:
(1)消毒剂次氯酸钠可由氯气和NaOH溶液反应制得,反应的化学方程式为________ 。
(2)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可由Cl2O与ClO2按一定比例混合后在NaOH溶液中反应制得。
①NaClO2中氯元素的化合价是________ 。
②制备时Cl2O与ClO2完全反应的物质的量理论比为________ 。
(3)兴趣小组设计如下图实验装置制取少量消毒液。
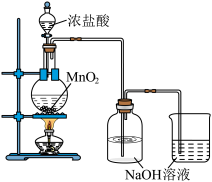
①MnO2与浓HCl反应的离子方程式为________ 。
②充分反应后,测得消毒液中NaCl与NaClO的物质的量之比大于1。可能的原因有________ (用文字简述)。
(4)Na2O2在呼吸面具中作供氧剂使用,若有7.8 g Na2O2参加反应,则转移的电子的物质的量为________ 。
(1)消毒剂次氯酸钠可由氯气和NaOH溶液反应制得,反应的化学方程式为
(2)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可由Cl2O与ClO2按一定比例混合后在NaOH溶液中反应制得。
①NaClO2中氯元素的化合价是
②制备时Cl2O与ClO2完全反应的物质的量理论比为
(3)兴趣小组设计如下图实验装置制取少量消毒液。

①MnO2与浓HCl反应的离子方程式为
②充分反应后,测得消毒液中NaCl与NaClO的物质的量之比大于1。可能的原因有
(4)Na2O2在呼吸面具中作供氧剂使用,若有7.8 g Na2O2参加反应,则转移的电子的物质的量为
更新时间:2023-05-04 15:33:14
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。是目前国际上公认的新一代高效、广谱、安全的杀菌、保鲜剂,在水处理等方面有广泛应用的高效安全消毒剂。与Cl2相比ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
(1)实验室用二氧化锰制备氯气的化学方程式为____ ,氯气和水反应的离子方程式为____ 。
(2)在ClO2的制备方法中,比较实用的有数十种,实验室常用氯酸钠(NaClO3)、亚硫酸钠(Na2SO3)和硫酸共热制备二氧化氯,此化学反应方程式为____ 。
(3)我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:
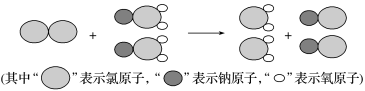
该反应的化学方程式为____ 。
(4)含氯消毒剂的消毒能力可以用氧化性来衡量。每克ClO2的氧化能力相当于____ 克Cl2的氧化能力。(计算结果保留两位小数)
(1)实验室用二氧化锰制备氯气的化学方程式为
(2)在ClO2的制备方法中,比较实用的有数十种,实验室常用氯酸钠(NaClO3)、亚硫酸钠(Na2SO3)和硫酸共热制备二氧化氯,此化学反应方程式为
(3)我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:

该反应的化学方程式为
(4)含氯消毒剂的消毒能力可以用氧化性来衡量。每克ClO2的氧化能力相当于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在抗击新冠肺炎疫情的战役中,消毒剂发挥了重要的作用。
(1)常用的消毒剂有双氧水、医用酒精以及含氯消毒剂等,其中含氯消毒剂的家族最庞大、应用最广泛。实验室制备Cl2有三种常用方法:
a.MnO2与浓盐酸反应
b.2KMnO4+16HCl (浓)=2KCl+2MnCl2+5Cl2↑+8H2O
c.KClO3+6HCl (浓)=KCl+3Cl2↑+3H2O
①酒精、Cl2、KMnO4、浓盐酸中属于电解质的是_______ ,属于非电解质的是_______ 。
②写出反应a的化学方程式_______ 。反应a装置还可用于实验室制取_______ 气体。
③反应b中被氧化的元素为_______ ,氧化剂为_______ 。当15.8 g KMnO4参与反应时,发生电子转移的HCl有_______ mol。
④当参与三个反应的HCl的质量相同时,得到Cl2的质量最多的是_______ (填字母序号)。
(2)“84”消毒液的有效成分为NaClO,常温下用烧碱溶液吸收Cl2可制备“84”消毒液。若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO、NaClO3的混合溶液。当混合溶液中的Cl-和 的个数比为15∶2时,混合液中的ClO-和
的个数比为15∶2时,混合液中的ClO-和 的个数比为
的个数比为_______ 。
(3)“洁厕灵”的有效成分为较浓的盐酸。“洁厕灵”和“84”消毒液不可以混合使用,否则会产生有毒气体。请用离子方程式解释原因:_______ 。
(4)高铁酸钠(Na2FeO4))是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:
请配平该化学方程式并用单线桥表示电子转移的方向和数目。_________
(1)常用的消毒剂有双氧水、医用酒精以及含氯消毒剂等,其中含氯消毒剂的家族最庞大、应用最广泛。实验室制备Cl2有三种常用方法:
a.MnO2与浓盐酸反应
b.2KMnO4+16HCl (浓)=2KCl+2MnCl2+5Cl2↑+8H2O
c.KClO3+6HCl (浓)=KCl+3Cl2↑+3H2O
①酒精、Cl2、KMnO4、浓盐酸中属于电解质的是
②写出反应a的化学方程式
③反应b中被氧化的元素为
④当参与三个反应的HCl的质量相同时,得到Cl2的质量最多的是
(2)“84”消毒液的有效成分为NaClO,常温下用烧碱溶液吸收Cl2可制备“84”消毒液。若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO、NaClO3的混合溶液。当混合溶液中的Cl-和
 的个数比为15∶2时,混合液中的ClO-和
的个数比为15∶2时,混合液中的ClO-和 的个数比为
的个数比为(3)“洁厕灵”的有效成分为较浓的盐酸。“洁厕灵”和“84”消毒液不可以混合使用,否则会产生有毒气体。请用离子方程式解释原因:
(4)高铁酸钠(Na2FeO4))是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:

请配平该化学方程式并用单线桥表示电子转移的方向和数目。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下图图1为氮元素及其化合物的转化关系,图2为实验室制取某气体的装置。完成下列填空:

(1)图1中X的化学式为_______ 。从化合价上看,X具有_______ (填“氧化”或“还原”)性。
(2)实验室常用图2中的发生装置制备氨气,该反应化学方程式为_______ 。若要收集一瓶氨气,图2虚框中的连接图应为_______ (选填编号,气体均从左面导管进入)。

(3)下列试剂不能用于干燥 的是
的是_______ (选填字母)。
a.浓硫酸 b.碱石灰 c.NaOH固体 d.
(4)汽车排气管上装有催化转换器可减少尾气对环境的污染,汽车尾气中的有害气体CO和NO在催化下可相互反应转化为无毒无害气体排放,写出该反应的化学方程式_______ 。

(1)图1中X的化学式为
(2)实验室常用图2中的发生装置制备氨气,该反应化学方程式为

(3)下列试剂不能用于干燥
 的是
的是a.浓硫酸 b.碱石灰 c.NaOH固体 d.

(4)汽车排气管上装有催化转换器可减少尾气对环境的污染,汽车尾气中的有害气体CO和NO在催化下可相互反应转化为无毒无害气体排放,写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氯是重要的非金属元素,研究它的性质及用途对生产, 生活、科研具有重要意义。
(1)一氯胺(NH2Cl)是一种长效缓释水消毒剂,在中性或酸性环境中会发生反应,生成一种具有强烈杀菌作用的物质,该物质为_______ 。工业上可利用NH3和Cl2反应制备一氯胺; 生成1molNH2Cl时,转移的电子数目为_______ 。
(2)Cl2 与NaOH溶液反应可制取“84消毒液。
用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO3), 此时ClO-的浓度为c0mol/L;加热时NaClO能转化为NaClO3,测得t时刻溶液中ClO-的浓度为c1 mol/L (不考虑加热前后溶液体积的变化)。
①用24gNaOH配成250mL溶液时,c(NaOH)=_______ mol/L。
②写出溶液中NaClO分解生成NaClO3的化学方程式:_______ 。
③t时刻溶液中c(Cl-)=_______ mol/L(用含c0、c1的代数式表示)。
(1)一氯胺(NH2Cl)是一种长效缓释水消毒剂,在中性或酸性环境中会发生反应,生成一种具有强烈杀菌作用的物质,该物质为
(2)Cl2 与NaOH溶液反应可制取“84消毒液。
用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO3), 此时ClO-的浓度为c0mol/L;加热时NaClO能转化为NaClO3,测得t时刻溶液中ClO-的浓度为c1 mol/L (不考虑加热前后溶液体积的变化)。
①用24gNaOH配成250mL溶液时,c(NaOH)=
②写出溶液中NaClO分解生成NaClO3的化学方程式:
③t时刻溶液中c(Cl-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】NaCl是一种化工原料,可以制备多种物质,如图所示。
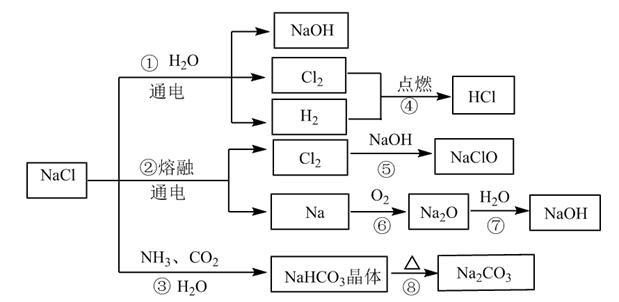
请回答下列问题:
(1)图所列物质中属于电解质的有___________ 种,转化反应中属于氧化还原反应的有___________ (填图中序号)
(2)工业上制取NaOH主要采用反应①,而不采用反应⑦的方法,主要原因是___________ 。
(3)反应④的现象是___________ ;反应⑤的化学方程式为___________ 。
(4)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。某同学购买了一瓶某品牌的“84消毒液”,查看相关资料及包装说明可获得以下信息:原液净含量为600g、密度约为1.1g/cm3、有效成分NaClO的质量分数约为1.9%(通过有效氯含量折算而得)。该同学从中取出100mL原液,按包装说明稀释30倍(体积之比)后用于家庭一般物体表面消毒,稀释后的溶液中c(NaClO)=___________ mol/L(结果保留两位小数);“84消毒液”不能与“洁厕灵(主要成分是HCl)”混合使用,否则会产生黄绿色的有毒气体引起安全事故,其反应的离子方程式是___________ 。

请回答下列问题:
(1)图所列物质中属于电解质的有
(2)工业上制取NaOH主要采用反应①,而不采用反应⑦的方法,主要原因是
(3)反应④的现象是
(4)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。某同学购买了一瓶某品牌的“84消毒液”,查看相关资料及包装说明可获得以下信息:原液净含量为600g、密度约为1.1g/cm3、有效成分NaClO的质量分数约为1.9%(通过有效氯含量折算而得)。该同学从中取出100mL原液,按包装说明稀释30倍(体积之比)后用于家庭一般物体表面消毒,稀释后的溶液中c(NaClO)=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组进行了如下实验。请回答:
(1)用一氧化碳还原氧化铁,反应的化学方程式为_______ 。反应完毕后,他们将得到的铁屑装入下图所示装置进行实验,A中的玻璃丝可以阻止固体离开A管,B中碱石灰的作用是_______ 。一段时间后,他们将A中的固体溶于水,并向所得溶液中滴入几滴KSCN溶液。
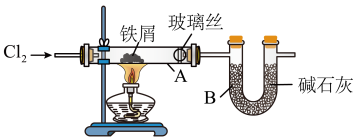
①若观察到溶液出现红色,证明溶液中含有_______ (填离子符号)。
②若未观察到溶液出现红色,可能的原因是_______ 。
(2)用足量的稀盐酸溶解一定量的Fe2O3,得到棕黄色溶液。甲同学向溶液中加入铜粉欲获得铁,他_______ (填“能”或“不能”)成功,原因是_______
(3)已知铝粉与氧化铁能发生反应2Al+Fe2O3 2Fe+Al2O3小组成员将反应的产物用足量的NaOH溶液浸泡,除去其中的Al2O3,分离得到Fe,反应的化学方程式为
2Fe+Al2O3小组成员将反应的产物用足量的NaOH溶液浸泡,除去其中的Al2O3,分离得到Fe,反应的化学方程式为_______ 。某同学认为用足量稀盐酸浸泡也能达到相同的结果,他的观点_______ (填“正确”或“不正确”)。
(1)用一氧化碳还原氧化铁,反应的化学方程式为

①若观察到溶液出现红色,证明溶液中含有
②若未观察到溶液出现红色,可能的原因是
(2)用足量的稀盐酸溶解一定量的Fe2O3,得到棕黄色溶液。甲同学向溶液中加入铜粉欲获得铁,他
(3)已知铝粉与氧化铁能发生反应2Al+Fe2O3
 2Fe+Al2O3小组成员将反应的产物用足量的NaOH溶液浸泡,除去其中的Al2O3,分离得到Fe,反应的化学方程式为
2Fe+Al2O3小组成员将反应的产物用足量的NaOH溶液浸泡,除去其中的Al2O3,分离得到Fe,反应的化学方程式为
您最近一年使用:0次
【推荐1】氧化还原反应知识的学习,为我们研究化学物质和化学反应提供了新的视角
(1)下列粒子中,只有还原性的是_______ 。
①S2-②Fe2+③Fe3+④S⑤H+⑥Na+⑦Mg
(2)吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体内的活性氧,由此推断Na2SeO3的作用是_______ 。
(3)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了_______ 性,若生成的气体在标准状况下所占的体积为11.2L时,转移电子数为_______
(4)已知反应:①6HCl+KClO3=KCl+3H2O+3Cl2↑
②Cl2+2KI=2KCl+I2
③I2+Cl2+H2O→HIO3+HCl(未配平)
反应①中若有3mol盐酸参与反应,转移的电子数目为____ ,对于反应③下列说法正确的是______ 。
A.反应③中氧化剂和还原剂的物质的量之比为1∶5
B.结合反应②③,若将Cl2通入含有淀粉的KI溶液中,可能会观察到先变蓝后褪色
C.还原性由强到弱顺序:Cl->I-
D.氧化性由强到弱顺序:KClO3>Cl2>I2
(5)反应①是制取Cl2的方法,除此之外反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O也常用来制备Cl2,若反应生成22.4LCl2(标准状况),转移电子的物质的量是_______ ,被氧化的HCl和参加反应的HCl的质量之比_______ 。
(1)下列粒子中,只有还原性的是
①S2-②Fe2+③Fe3+④S⑤H+⑥Na+⑦Mg
(2)吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体内的活性氧,由此推断Na2SeO3的作用是
(3)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
(4)已知反应:①6HCl+KClO3=KCl+3H2O+3Cl2↑
②Cl2+2KI=2KCl+I2
③I2+Cl2+H2O→HIO3+HCl(未配平)
反应①中若有3mol盐酸参与反应,转移的电子数目为
A.反应③中氧化剂和还原剂的物质的量之比为1∶5
B.结合反应②③,若将Cl2通入含有淀粉的KI溶液中,可能会观察到先变蓝后褪色
C.还原性由强到弱顺序:Cl->I-
D.氧化性由强到弱顺序:KClO3>Cl2>I2
(5)反应①是制取Cl2的方法,除此之外反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O也常用来制备Cl2,若反应生成22.4LCl2(标准状况),转移电子的物质的量是
您最近一年使用:0次
【推荐2】KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆ClO2。其变化可表示为KClO3 +HCl(浓) →KCl +ClO2↑ +Cl2↑ +H2O。
(1)请完成该化学方程式并配平:
___ KClO3 +____ HCl(浓) →___ KCl +___ ClO2↑ +___ Cl2↑ +___ H2O
(2)此反应的还原剂是_________ ,它的氧化产物是_____________ ;
(3)浓盐酸在反应中显示出来的性质是______________ 。标准状况下,产生33.6L的Cl2,则转移的电子的物质的量为___________ mol。
(1)请完成该化学方程式并配平:
(2)此反应的还原剂是
(3)浓盐酸在反应中显示出来的性质是
您最近一年使用:0次
【推荐3】对于4NH3+5O2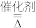 4NO+6H2O反应。
4NO+6H2O反应。
(1)被氧化的元素是________ ,被还原的元素是________ 。
(2)发生氧化反应的物质是________ ,发生还原反应的物质是________ ,还原产物是________ ,氧化产物是________ 。
(3)该反应是置换反应吗?________ (选填“是”或“不是”)。
(4)当生成30 g NO时,转移电子数为________ 。
(5)从单线桥表示电子转移的方向和数目________ 。
(6)查阅资料可知:铜和浓硫酸共热,发生反应Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为
CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为________ ,其中H2SO4在反应中体现____________________ 作用。
(7)请配平下列反应方程式:
_____ K2Cr2O7+____ HCl
_______ KCl+_____ CrCl3+_____ Cl2↑+______ H2O
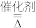 4NO+6H2O反应。
4NO+6H2O反应。(1)被氧化的元素是
(2)发生氧化反应的物质是
(3)该反应是置换反应吗?
(4)当生成30 g NO时,转移电子数为
(5)从单线桥表示电子转移的方向和数目
(6)查阅资料可知:铜和浓硫酸共热,发生反应Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为
CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为(7)请配平下列反应方程式:

您最近一年使用:0次



