现有 ,请通过计算填空:
,请通过计算填空:
(1)该气体的摩尔质量是多少?___________ 它的密度是相同条件下氢气密度的___________ 倍
(2)该气体物质的量为___________ ,所含H原子数目为___________ 。
(3)该气体在标准状况下的体积为___________ 。
(4)若将该气体溶于水配成V L溶液,所得溶液溶质的物质的量浓度为___________ 。
 ,请通过计算填空:
,请通过计算填空:(1)该气体的摩尔质量是多少?
(2)该气体物质的量为
(3)该气体在标准状况下的体积为
(4)若将该气体溶于水配成V L溶液,所得溶液溶质的物质的量浓度为
更新时间:2020-12-25 10:20:29
|
相似题推荐
计算题
|
较易
(0.85)
名校
【推荐1】物质的量是高中化学常用的物理量,请完成以下有关计算。
(1)含0.3 mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是___________ 。
(2)___________ g H2O2所含原子数与0.2 mo lH3PO4所含原子数相等。
(3)质量相同的H2、NH3、SO2、O3四种气体中,含有原子数目最少的是_____ (填写化学式)。
(4)如果规定,1mol粒子集合体所含的粒子数与0.024 kg 12C中所含的碳原子数相同。那么将36.5 g HCl溶于水中配成溶液500mL,则溶液的浓度为_________ mol/L。
(5)同温同压下,某容器充满氧气重116g,若充满二氧化碳重122g,现充满某气体重114g,则该气体的摩尔质量为___________
(1)含0.3 mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是
(2)
(3)质量相同的H2、NH3、SO2、O3四种气体中,含有原子数目最少的是
(4)如果规定,1mol粒子集合体所含的粒子数与0.024 kg 12C中所含的碳原子数相同。那么将36.5 g HCl溶于水中配成溶液500mL,则溶液的浓度为
(5)同温同压下,某容器充满氧气重116g,若充满二氧化碳重122g,现充满某气体重114g,则该气体的摩尔质量为
您最近半年使用:0次
计算题
|
较易
(0.85)
名校
【推荐2】(1)同温、同压下,A容器中充满O2,B容器中充满O3。若两容器中所含原子总数相等,则A容器和B容器的体积比是__ 。
(2)在25℃、101kPa的条件下,等质量的CH4和A气体的体积之比为15:8,则A的摩尔质量为__ 。
(3)设NA为阿伏加德罗常数的数值,如果ag气体A中含有的分子数为b,则cg气体A在标准状况下的体积约是__ (用含NA的式子表示)。
(4)相同物质的量浓度的氯化钠、氯化镁、氯化铝溶液,分别与硝酸银溶液反应,当生成沉淀的质量之比为3:2:1时,消耗三种盐溶液的体积比为__ 。
(5)在质量分数为28%的KOH水溶液中,OH-与H2O数目之比是_ (忽略水的电离)。
(2)在25℃、101kPa的条件下,等质量的CH4和A气体的体积之比为15:8,则A的摩尔质量为
(3)设NA为阿伏加德罗常数的数值,如果ag气体A中含有的分子数为b,则cg气体A在标准状况下的体积约是
(4)相同物质的量浓度的氯化钠、氯化镁、氯化铝溶液,分别与硝酸银溶液反应,当生成沉淀的质量之比为3:2:1时,消耗三种盐溶液的体积比为
(5)在质量分数为28%的KOH水溶液中,OH-与H2O数目之比是
您最近半年使用:0次
计算题
|
较易
(0.85)
名校
【推荐3】完成下列填空:
(1)3.01×1023个氯气分子的物质的量是_______ ,0.5mol的H2O中含有的电子数为_______ (用NA表示)。
(2)同温同压下,同体积的甲烷(CH4)和CO2物质的量之比为_______ ,密度之比为_______ 。
(3)3.1g Na2X含有Na+ 0.1mol,则Na2X的摩尔质量为_______ ,X的相对原子质量为_______ 。
(4)在标准状况下,CO和CO2的混合气体共6.72L,质量为12g,则两种气体的物质的量之比为_______ ,混合气体的平均摩尔质量为_______ 。
(1)3.01×1023个氯气分子的物质的量是
(2)同温同压下,同体积的甲烷(CH4)和CO2物质的量之比为
(3)3.1g Na2X含有Na+ 0.1mol,则Na2X的摩尔质量为
(4)在标准状况下,CO和CO2的混合气体共6.72L,质量为12g,则两种气体的物质的量之比为
您最近半年使用:0次
计算题
|
较易
(0.85)
【推荐1】计算
(1)标准状况下,112 mL某气体的质量为0.14 g,则其摩尔质量为_______ ,相对分子质量为_______ ;
(2)将4gNaOH溶解在100mL水中其物质的量浓度是_______ ,稀至1L后取出10mL,其物质的量浓度是_______ 。
(3)计算10克碳酸钙与足量稀盐酸反应生成二氧化碳的在标况下的体积为多少?_______
(1)标准状况下,112 mL某气体的质量为0.14 g,则其摩尔质量为
(2)将4gNaOH溶解在100mL水中其物质的量浓度是
(3)计算10克碳酸钙与足量稀盐酸反应生成二氧化碳的在标况下的体积为多少?
您最近半年使用:0次
计算题
|
较易
(0.85)
【推荐2】辛烷值是衡量汽油抵抗震爆能力的指标。请计算114g辛烷(C8H18)完全燃烧至少需要氧气的体积(标准状况下)_______ 。
您最近半年使用:0次
计算题
|
较易
(0.85)
【推荐1】某工厂排出的废水,经测定含0.012mol·L-1的游离Br2和8×10-4mol·L-1的H+离子。若用加Na2SO3的方法除去Br2,化学反应为:Na2SO3+Br2+H2O—Na2SO4+HBr(方程式未配平),现处理这种废水5L,问①需加入0.05mol·L-1的Na2SO3溶液多少升才能把Br2除尽?②除尽后的废水中H+离子的物质的量浓度是多少?(溶液的体积变化忽略不计)
您最近半年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】标准状况下11.2LHCl气体溶于水形成500mL溶液。
(1)所得盐酸的物质的量浓度为________ 。
(2)向其中加入________ gNaOH才能中和完全。
(3)若不考虑加入NaOH对体积造成的影响,所得NaCl的物质的量浓度为________ 。取出其中50mlNaCl溶液,其物质的量浓度为________ ;若再加水稀释至500ml,则所得稀溶液中NaCl的物质的量浓度为________ 。
(1)所得盐酸的物质的量浓度为
(2)向其中加入
(3)若不考虑加入NaOH对体积造成的影响,所得NaCl的物质的量浓度为
您最近半年使用:0次
计算题
|
较易
(0.85)
名校
【推荐3】回答下列问题:
(1)写出 的电离方程式
的电离方程式_________ 。
(2) 个
个 含
含_________ mol氧原子,氧原子的质量为_________ 。
(3)在同温同压条件下, 和
和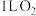 的物质的量之比为
的物质的量之比为_________ ,分子个数之比是_________ 。
(4)有 溶液,从该溶液中取出10mL,则
溶液,从该溶液中取出10mL,则
_________ ,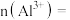
_________ 。
(5)用 氧化溶质质量分数为36.5%的盐酸。反应方程式如下:
氧化溶质质量分数为36.5%的盐酸。反应方程式如下: ;问题:
;问题: 至少能消耗HCl的物质的量为
至少能消耗HCl的物质的量为_________ mol?被氧化的HCl为_________ mol?
(6)在无土栽培中,配制1L内含 、
、 、
、 的某营养液。若用KCl、
的某营养液。若用KCl、 、
、 配制,则需这三种固体物质的量分别为
配制,则需这三种固体物质的量分别为_________ mol、_________ mol、_________ mol。
(1)写出
 的电离方程式
的电离方程式(2)
 个
个 含
含(3)在同温同压条件下,
 和
和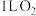 的物质的量之比为
的物质的量之比为(4)有
 溶液,从该溶液中取出10mL,则
溶液,从该溶液中取出10mL,则
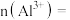
(5)用
 氧化溶质质量分数为36.5%的盐酸。反应方程式如下:
氧化溶质质量分数为36.5%的盐酸。反应方程式如下: ;问题:
;问题: 至少能消耗HCl的物质的量为
至少能消耗HCl的物质的量为(6)在无土栽培中,配制1L内含
 、
、 、
、 的某营养液。若用KCl、
的某营养液。若用KCl、 、
、 配制,则需这三种固体物质的量分别为
配制,则需这三种固体物质的量分别为
您最近半年使用:0次
计算题
|
较易
(0.85)
名校
【推荐1】现有14.4 g CO和CO2的混合气体,在标准状况下其体积为8.96 L。回答问题:
(1)该混合气体的平均摩尔质量为___________ 。
(2)混合气体中碳原子的个数为___________ (用NA表示阿伏加德罗常数的值)。
(3)将混合气体依次通过如图所示装置,最后收集在气球中。
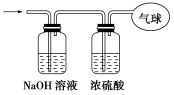
①气球中收集到的气体的摩尔质量为___________ 。
②气球中收集到的气体中,电子总数为___________ (用NA表示阿伏加德罗常数的值)。
③标准状况下,气球中收集到的气体的体积为___________ L。
(1)该混合气体的平均摩尔质量为
(2)混合气体中碳原子的个数为
(3)将混合气体依次通过如图所示装置,最后收集在气球中。

①气球中收集到的气体的摩尔质量为
②气球中收集到的气体中,电子总数为
③标准状况下,气球中收集到的气体的体积为
您最近半年使用:0次
计算题
|
较易
(0.85)
名校
【推荐2】设NA表示阿伏加 德罗常数的值,请回答下列问题:
(1)12.4gNa2X含有0.4molNa+,则Na2X的摩尔质量为___ ,其相对分子质量为___ ;X的相对原子质量为____ 。
(2)a个X原子的总质量为b g,则X的相对原子质量可表示为___ 。
(1)12.4gNa2X含有0.4molNa+,则Na2X的摩尔质量为
(2)a个X原子的总质量为b g,则X的相对原子质量可表示为
您最近半年使用:0次
计算题
|
较易
(0.85)
名校
【推荐3】设NA表示阿伏加 德罗常数的值。回答下列问题:
(1)0.3molNH3分子中所含原子数与__ 个H2O分子中所含原子数相等。
(2)含0.4molAl3+的Al2(SO4)3中所含的SO 的物质的量是
的物质的量是__ 。
(3)—定条件下,16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为__ 。
(4)0.4molSiH4分子中所含原子数与__ gHCl分子中所含原子数相等。
(5)两个相同容积的密闭容器X、Y,在25℃下,X中充入agA气体,Y中充入agCH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为__ 。
(6)在某温度时,一定量的元素A的氢化物AH3,在恒温恒压的密闭容器中完全分解为两种气态单质,此时容器的体积变为原来的 ,则A单质的分子式为
,则A单质的分子式为__ 。
(1)0.3molNH3分子中所含原子数与
(2)含0.4molAl3+的Al2(SO4)3中所含的SO
 的物质的量是
的物质的量是(3)—定条件下,16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为
(4)0.4molSiH4分子中所含原子数与
(5)两个相同容积的密闭容器X、Y,在25℃下,X中充入agA气体,Y中充入agCH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为
(6)在某温度时,一定量的元素A的氢化物AH3,在恒温恒压的密闭容器中完全分解为两种气态单质,此时容器的体积变为原来的
 ,则A单质的分子式为
,则A单质的分子式为
您最近半年使用:0次



