已知几种元素的性质或原子结构的相关叙述如表所示,回答下列问题。
(1)元素X的一种同位素用作相对原子质量的标准,这种同位素的原子符号是___________ 。X的另一种同位素可用来测定文物所属年代,这种同位素的原子符号是___________ 。
(2)Y形成的另一种单质,主要存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是___________ 。
(3)画出T的原子结构示意图:___________ 。
(4)T与Y可以形成T2Y2的化合物,写出其与XY2反应的化学方程式___________ 。
元素编号 | 元素性质或原子结构的相关叙述 |
T | 失去一个电子后、形成与Ne相同的核外电子排布 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 其某种单质是空气的主要成分,也是最常见的助燃剂 |
Z | 原子核外有3个电子层,最外层比次外层少1个电子 |
(2)Y形成的另一种单质,主要存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是
(3)画出T的原子结构示意图:
(4)T与Y可以形成T2Y2的化合物,写出其与XY2反应的化学方程式
更新时间:2020-12-29 20:35:16
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】如图所示为两个实验转置(铁架台等辅助仪器已略去)。
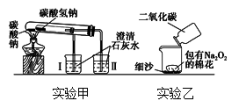
回答下列问题:
(1)实验甲在加热过程中能观察到有白色沉淀生成的是_______ (填“ I”或“II”)烧杯,该烧杯中发生反应的离子方程式是___________ 。
(2)实验乙用来验证Na2O2与CO2的反应,观察到的实验现象:包有Na2O2的棉花燃烧。写出Na2O2与CO2发生反应的化学方程式__________ ,棉花燃烧说明该反应的特点是______________ 。
(3)取10.0 g碳酸钠和碳酸氢钠的混合物加热,将生成的CO2通入足量澄清石灰水中完全吸收,测得生成沉淀4.0g。则原混合物中碳酸钠的质量分数为_________ 。

回答下列问题:
(1)实验甲在加热过程中能观察到有白色沉淀生成的是
(2)实验乙用来验证Na2O2与CO2的反应,观察到的实验现象:包有Na2O2的棉花燃烧。写出Na2O2与CO2发生反应的化学方程式
(3)取10.0 g碳酸钠和碳酸氢钠的混合物加热,将生成的CO2通入足量澄清石灰水中完全吸收,测得生成沉淀4.0g。则原混合物中碳酸钠的质量分数为
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】以不同类别物质间转化为线索,认识钠及其化合物。请回答下列问题:
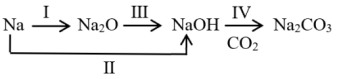
(1)转化Ⅰ的产物 属于
属于_______ (填“酸”或“碱”)性氧化物。
(2)若改变转化Ⅰ的反应条件,可得到钠的另一种氧化物 ,写出其与
,写出其与 反应的化学方程式
反应的化学方程式_______ 。
(3)某同学为探究转化Ⅱ,将钠投入足量水中,记录了如下实验现象和实验结论:①有碱生成 ②溶液变红 ③钠四处游动 ④钠浮在水面上 ⑤有气体产生 ⑥钠的密度比水小 ⑦钠熔成光亮的小球 ⑧反应放热,钠熔点低。

补齐下表(从①~⑧中选择,填序号):
写出转化Ⅱ中反应的化学方程式_______ 。
(4)某同学设计了如下两个对照实验,对比碳酸钠与碳酸氢钠热稳定性的差异。
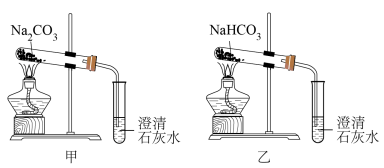
通过实验,该同学得出结论,热稳定性: 。该同学依据的现象是
。该同学依据的现象是_______ 。

(1)转化Ⅰ的产物
 属于
属于(2)若改变转化Ⅰ的反应条件,可得到钠的另一种氧化物
 ,写出其与
,写出其与 反应的化学方程式
反应的化学方程式(3)某同学为探究转化Ⅱ,将钠投入足量水中,记录了如下实验现象和实验结论:①有碱生成 ②溶液变红 ③钠四处游动 ④钠浮在水面上 ⑤有气体产生 ⑥钠的密度比水小 ⑦钠熔成光亮的小球 ⑧反应放热,钠熔点低。

补齐下表(从①~⑧中选择,填序号):
| 实验现象 | ④ | ③ | ② | |
| 实验结论 | ⑧ | ⑤ |
(4)某同学设计了如下两个对照实验,对比碳酸钠与碳酸氢钠热稳定性的差异。

通过实验,该同学得出结论,热稳定性:
 。该同学依据的现象是
。该同学依据的现象是
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】X、Y、Z是短周期的三种元素,它们在周期表中的位置如下表所示:
请回答:
⑴X元素的名称是____ 。
⑵Y元素的原子序数是____ ,它所在的周期数是____ 。
⑶Z在元素周期表中的位置是________ 。
| X | ||
| Y | ||
| Z |
请回答:
⑴X元素的名称是
⑵Y元素的原子序数是
⑶Z在元素周期表中的位置是
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】原子序数小于36的X、Y、Z、W、J五种元素,原子序数依次增大,其中X元素原子半径是所有元素原子中最小的,Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,W元素原子最外层电子数是内层电子数的3倍,J元素原子序数为24。(用元素符号或化学式表示)。
(1)Y、Z、W的第一电离能由小到大的顺序为___________ 。
(2)J原子的核外电子排布式为_________________ 。
(3)Y2X2分子中Y原子轨道的杂化类型为_____________ 。
1mol Y2X2分子中含有σ键与π键的数目之比为__________________ 。
(4)Z与W形成的一种Z2W分子,与该分子互为等电子体的阴离子为______ (任写一种)。
(5)JCl3能与Z、W的氢化物形成配位数为6的络合物,且相应两种配体的物质的量之比为2:1,氯离子全部位于外界。则该配合物的化学式为_________ 。
(1)Y、Z、W的第一电离能由小到大的顺序为
(2)J原子的核外电子排布式为
(3)Y2X2分子中Y原子轨道的杂化类型为
1mol Y2X2分子中含有σ键与π键的数目之比为
(4)Z与W形成的一种Z2W分子,与该分子互为等电子体的阴离子为
(5)JCl3能与Z、W的氢化物形成配位数为6的络合物,且相应两种配体的物质的量之比为2:1,氯离子全部位于外界。则该配合物的化学式为
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】根据短周期元素的信息回答问题。
(1)写出A、B的元素符号____________ 、_________ ,C、D的元素的名称__________ 、_____________ 。
(2)写出B、C单质在加热时反应的方程式____________________________________
(3)从原子结构角度分析A与B的______________ 相同,C与D的_______________ 相同。
| 元素信息 | |
| A | 第3周期第ⅥA族 |
| B | 族序数是周期数的3倍 |
| C | 原子序数是11 |
| D | D3+与Ne电子数相同 |
(1)写出A、B的元素符号
(2)写出B、C单质在加热时反应的方程式
(3)从原子结构角度分析A与B的
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,A形成的单质为密度最小的气体,B、W同周期,A、D同主族,A与W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。回答下列问题:
(1)E元素在周期表中的位置为_______ 。
(2)D的一种氧化物可与B的最高价氧化物反应生成W的单质,试写出反应的化学方程式:_______ 。
(3)D形成的单质在一定条件下能与A形成的单质化合生成一种化合物DA,DA能与水反应放出氢气,写出该反应的化学方程式:_______ 。
(1)E元素在周期表中的位置为
(2)D的一种氧化物可与B的最高价氧化物反应生成W的单质,试写出反应的化学方程式:
(3)D形成的单质在一定条件下能与A形成的单质化合生成一种化合物DA,DA能与水反应放出氢气,写出该反应的化学方程式:
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表列出了①~⑤五种元素在周期表中的位置:

请按要求回答下列问题:
(1)元素④元素名称___________ 。
(2)元素②和④形成的化合物中的化学键是___________ 键(填“离子”或“共价”)。
(3)元素①单质的电子式为___________ 。
(4)元素②~⑤的原子半径由大到小的顺序为(填元素符号)___________ ,它们的最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式)。
(5) 元素②和⑤的最高价氧化物对应的水化物反应的离子方程式___________ 。
(6)元素④和⑤形成的氢化物中稳定性___________ >___________
(7) 元素①~⑤中,金属性最强的是(填元素符号)___________ ,非金属性最强的是(填元素符号)___________ 。

请按要求回答下列问题:
(1)元素④元素名称
(2)元素②和④形成的化合物中的化学键是
(3)元素①单质的电子式为
(4)元素②~⑤的原子半径由大到小的顺序为(填元素符号)
(5) 元素②和⑤的最高价氧化物对应的水化物反应的离子方程式
(6)元素④和⑤形成的氢化物中稳定性
(7) 元素①~⑤中,金属性最强的是(填元素符号)
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】已知M、W、X、Y、Z中是原子序数依次增大的短周期主族元素,M的单质是空气中含量最多的气体,W与Z同主族,W原子最外层电子数是6,含X元素的物质灼烧时火焰呈黄色,Y是地壳中含量最高的金属元素。回答下列问题:
(1)W在元素周期表中的位置是___________ 。
(2)X的单质与水反应的离子方程式为___________ 。
(3)X和Y的最高价氧化物的水化物中碱性较强的是___________ (填化学式)。
(4)Y与M的原子半径较大的是___________ (填化学式),X与Z分别形成的简单离子中,半径较大的是___________ (填离子符号)。
(5)ZW2与Z的气态氢化物发生反应产生淡黄色固体,写出反应的化学方程式并用双线桥法标出电子转移的方向与数目___________ 。
(6)化合物YM与X氢氧化物的水溶液反应生成一种盐和一种碱性气体。该反应的化学方程式为___________ 。
(1)W在元素周期表中的位置是
(2)X的单质与水反应的离子方程式为
(3)X和Y的最高价氧化物的水化物中碱性较强的是
(4)Y与M的原子半径较大的是
(5)ZW2与Z的气态氢化物发生反应产生淡黄色固体,写出反应的化学方程式并用双线桥法标出电子转移的方向与数目
(6)化合物YM与X氢氧化物的水溶液反应生成一种盐和一种碱性气体。该反应的化学方程式为
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】下表是元素周期表的一部分(注意:用元素符号或化学式填空)
(1)C的离子的结构示意图____ ,G元素的氧化物化学式___ ,H的氢化物的化学式__________ 。
(2)H元素的单质的电子式_____ ;
(3)A-H八种元素中(a)原子半径最大的元素是____ ,(b)单质的还原性最强的元素是____ ,(c)最高价氧化物对应水化物酸性最强的是_____ ;(d)最高价氧化物对应水化物碱性最强的是_______ 。
(4)用电子式表示AE 2的形成过程_______________ 。
(5)B与C的最高价氧化物对应水化物反应的离子方程式_______________ 。
 族 族周期 | ⅠA | ⅡA | ⅢA | IVA | VA | VIA | VIIA | O族 |
| 1 | ||||||||
| 2 | G | H | D | |||||
| 3 | B | C | E | |||||
| 4 | F | A | ||||||
(2)H元素的单质的电子式
(3)A-H八种元素中(a)原子半径最大的元素是
(4)用电子式表示AE 2的形成过程
(5)B与C的最高价氧化物对应水化物反应的离子方程式
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】几种主族元素在周期表中的位置如下
根据上表回答下列问题:
(1)⑥元素的氢化物是_______ (填化学式)。
(2)①③⑦三种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为_______ ,该元素在周期表中的位置是_______ 。
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是_______ (填化学式),①与水反应的化学方程式为_______ 。
(5)⑦的非金属性强于⑧,从原子结构的角度解释其原因:_______ 。下列表述中能证明这一事实的是_______ (填字母,下同)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(6)④与⑤元素形成的分子可能是_______ 。

族 周期 | I A | 0 | ||||||
| 1 | ④ | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑦ | |||||
| 4 | ② | ⑧ |
(1)⑥元素的氢化物是
(2)①③⑦三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是
(5)⑦的非金属性强于⑧,从原子结构的角度解释其原因:
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(6)④与⑤元素形成的分子可能是

您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】2022年是门捷列夫发现元素周期律 153 周年,下图为元素周期表的一部分。门捷列夫预言了多种当时未知的元素,T 为其中之一、L在地壳中含量排第二位,广泛应用于信息技术等领域。
(1)写出J的原子结构示意图___________ 。
(2)下列说法不正确的是___________。
(3)已知JQ2结构中只含有极性共价键,试画出其结构式:___________ (用元素符号表示)。
(4)非金属性Q___________ M(用<、=、>来表示),判断依据是(试用一个化学方程式来表示)___________ 。
| X | Y | Z | ||
| L | J | Q | ||
| T | M |
(2)下列说法不正确的是___________。
| A.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ2 |
| B.Q、J的氧化物的水化物酸性:J<Q |
| C.用pH试纸测得Q单质的水溶液pH=3 |
| D.原子半径大小:L>J>Z |
(4)非金属性Q
您最近半年使用:0次




