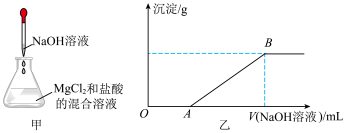
某同学称取一定质量的MgCl2固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液(如图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示。
请回答下列问题:
(1)溶解MgCl2固体所用的玻璃仪器有___ 。
A.天平 B.烧杯 C.漏斗 D.玻璃棒
(2)OA段反应的离子方程式为___ 。
(3)AB段反应的离子方程式为___ 。
(4)B点对应的溶液中的溶质为___ ,往B点溶液中滴加AgNO3溶液,发生反应的离子方程式为___ 。

请回答下列问题:
(1)溶解MgCl2固体所用的玻璃仪器有
A.天平 B.烧杯 C.漏斗 D.玻璃棒
(2)OA段反应的离子方程式为
(3)AB段反应的离子方程式为
(4)B点对应的溶液中的溶质为
更新时间:2020-12-24 13:09:45
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是元素周期表的一部分,表中所列字母分别代表某一元素。根据表中所列元素,回答下列问题:
(1)A元素在周期表中的位置_______ 化学性质最稳定的是_______ (填元素符号);
(2)A元素中子数为8的核素的符号:_______ ,写出E的离子结构示意图:_______ ;
(3)上表短周期元素中,金属性最强的是_______ (填元素符号);最高价氧化物对应水化物中酸性最强的物质_______ (填化学式);A、B、C的的气态氢化物稳定性由强到弱的顺序_______ (填化学式)
(4)表中E、F、G三元素可形成与Ar具有相同电子层结构的简单离子,这些离子的半径最大的是_______ (用离子符号表示):
(5)O、D的最高价氧化物对应水化物之间能发生反应,其离子方程式为。_______ 。
(6)用一个离子方程式说明元素E、F非金属性强弱_______ 。
| A | B | C | |||||||||||||||
| D | O | E | F | M | |||||||||||||
| G | H | I |
(2)A元素中子数为8的核素的符号:
(3)上表短周期元素中,金属性最强的是
(4)表中E、F、G三元素可形成与Ar具有相同电子层结构的简单离子,这些离子的半径最大的是
(5)O、D的最高价氧化物对应水化物之间能发生反应,其离子方程式为。
(6)用一个离子方程式说明元素E、F非金属性强弱
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某科研小组设计出利用工业废酸(主要成分为稀硫酸)浸取某废弃的氧化铜锌矿(主要含CuO、ZnO和 )的方案,实现废物综合利用,如图所示。
)的方案,实现废物综合利用,如图所示。
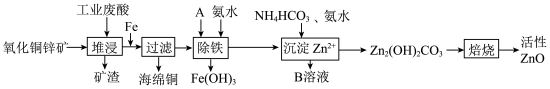
已知:各离子开始沉淀及完全沉淀时的pH如下表所示。
请回答下列问题:
(1)堆浸时,为了提高浸出效率可采取的措施有(任写1种):______ 。
(2)堆浸时产生的矿渣主要成分是______ 。
(3)物质A的作用是______ ,可使用下列物质中的______ 。
A. B.
B. C.
C. D.
D.
(4)除铁过程中加入氨水的目的是调节溶液的PH,PH应控制在______ 范围。
(5)物质B可直接用作氮肥,则B的化学式是______ 。
(6)除铁后得到的 可用KClO溶液在碱性环境下将其氧化得到一种高效的多功能水处理剂―
可用KClO溶液在碱性环境下将其氧化得到一种高效的多功能水处理剂― ,写出该反应的离子方程式
,写出该反应的离子方程式______ 。
 )的方案,实现废物综合利用,如图所示。
)的方案,实现废物综合利用,如图所示。
已知:各离子开始沉淀及完全沉淀时的pH如下表所示。
离子 |
|
|
|
开始沉淀时的PH | 6.34 | 1.48 | 6.2 |
完全沉淀时的PH | 9.7 | 3.2 | 8.0 |
(1)堆浸时,为了提高浸出效率可采取的措施有(任写1种):
(2)堆浸时产生的矿渣主要成分是
(3)物质A的作用是
A.
 B.
B. C.
C. D.
D.
(4)除铁过程中加入氨水的目的是调节溶液的PH,PH应控制在
(5)物质B可直接用作氮肥,则B的化学式是
(6)除铁后得到的
 可用KClO溶液在碱性环境下将其氧化得到一种高效的多功能水处理剂―
可用KClO溶液在碱性环境下将其氧化得到一种高效的多功能水处理剂― ,写出该反应的离子方程式
,写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有A、B、C、D四种化合物,分别由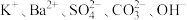 中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断化学式:A_____ ;B_____ ;C_____ ;D_____ 。
(2)写出下列反应的离子方程式。
①D与氯化钙溶液反应_____ ;
②B与盐酸反应:_____ ;
③C与少量的D的酸式盐溶液反应:_____ 。
④C与过量的D的酸式盐溶液反应:_____ 。
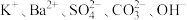 中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。(1)推断化学式:A
(2)写出下列反应的离子方程式。
①D与氯化钙溶液反应
②B与盐酸反应:
③C与少量的D的酸式盐溶液反应:
④C与过量的D的酸式盐溶液反应:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】通过海水晾晒可得粗盐,粗盐中除NaCl外,还含有 、
、 、
、 以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、
以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、 溶液、
溶液、 溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
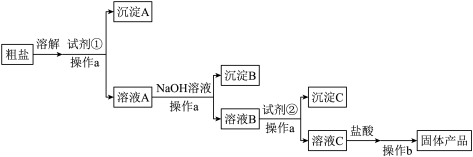
请回答:
(1)操作a名称是_______ 。
(2)试剂①是_______ 溶液(填化学式)。
(3)加入NaOH后,得到的主要沉淀B是_______ 。
(4)加入试剂②后,发生反应的离子方程式有_______ 。
(5)如果加入试剂②后直接加盐酸,产生的后果是_______ (用离子方程式表示)。
 、
、 、
、 以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、
以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、 溶液、
溶液、 溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
请回答:
(1)操作a名称是
(2)试剂①是
(3)加入NaOH后,得到的主要沉淀B是
(4)加入试剂②后,发生反应的离子方程式有
(5)如果加入试剂②后直接加盐酸,产生的后果是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O]是一种重要的无机化工产品。一种由白云石[主要成分为CaMg(CO3)2,含少量SiO2、Fe2O3等]为原料制备碱式碳酸镁(国家标准中CaO的质量分数≤0.43%)的实验流程如下:
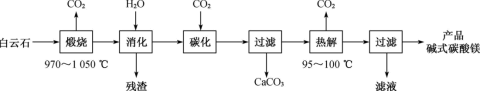
(1)“煅烧”时发生主要反应的化学方程式为___ 。
(2)常温常压下,“碳化”可使镁元素转化为Mg(HCO3)2,“碳化”时终点pH对最终产品中CaO含量及碱式碳酸镁产率的影响如图1和图2所示。
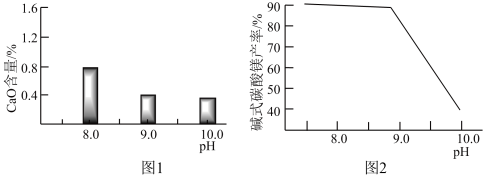
①应控制“碳化”终点pH约为___ ,钙元素的主要存在形式是___ (填化学式)。
②根据图2,当pH=10.0时,镁元素的主要存在形式是___ (填化学式)。
(3)“热解”生成碱式碳酸镁的化学方程式为___ 。
(4)该工艺为达到清洁生产,可以循环利用的物质是___ (填化学式)。

(1)“煅烧”时发生主要反应的化学方程式为
(2)常温常压下,“碳化”可使镁元素转化为Mg(HCO3)2,“碳化”时终点pH对最终产品中CaO含量及碱式碳酸镁产率的影响如图1和图2所示。

①应控制“碳化”终点pH约为
②根据图2,当pH=10.0时,镁元素的主要存在形式是
(3)“热解”生成碱式碳酸镁的化学方程式为
(4)该工艺为达到清洁生产,可以循环利用的物质是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】硫酸镁晶体(MgSO4·7H2O)是一种重要的化工原料。以菱镁矿(主要成分是MgCO3,含少量FeCO3和不溶性杂质)为原料制取硫酸镁晶体的过程如下:
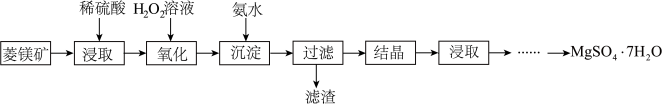
(1)MgCO3溶于稀硫酸的离子方程式是___________ 。
(2)“氧化”步骤中,加入H2O2溶液的目的是___________ (用离子方程式表示)。
(3)“沉淀”步骤中,用氨水调节溶液pH的范围是___________ 。
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(4)“过滤”所得滤液中含有的阳离子是___________ 。

(1)MgCO3溶于稀硫酸的离子方程式是
(2)“氧化”步骤中,加入H2O2溶液的目的是
(3)“沉淀”步骤中,用氨水调节溶液pH的范围是
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Mg2+ | Fe2+ | Fe3+ |
开始沉淀 | 9.1 | 7.6 | 1.9 |
完全沉淀 | 11.1 | 9.7 | 3.2 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】I.实验室要用98%(ρ=1.84g·cm-3)的硫酸配制3.68mol·L-1的硫酸溶液500mL
(1)需准确量取98%的硫酸 mL。
(2)准确量取一定体积的98%的硫酸后,要配制3.68mol·L-1的硫酸溶液500mL,必须用到的实验仪器是(填写序号): .
①500mL量筒 ②烧杯 ③1000mL容量瓶 ④500mL 容量瓶 ⑤天平 ⑥胶头滴管 ⑦锥形瓶 ⑧玻璃棒 ⑨酸式滴定管
(3)若配制3.68mol·L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,将使所配制的硫酸溶液浓度偏低的是 。
II. 某同学在探究废干电池内的黑色固体回收利用时,进行如图所示实验:
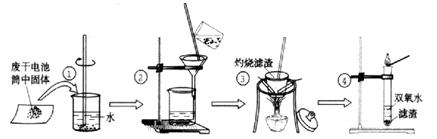
普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
⑴.操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为 (填化学式);
(2)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:(答案写在答题卷上)
(1)需准确量取98%的硫酸 mL。
(2)准确量取一定体积的98%的硫酸后,要配制3.68mol·L-1的硫酸溶液500mL,必须用到的实验仪器是(填写序号): .
①500mL量筒 ②烧杯 ③1000mL容量瓶 ④500mL 容量瓶 ⑤天平 ⑥胶头滴管 ⑦锥形瓶 ⑧玻璃棒 ⑨酸式滴定管
(3)若配制3.68mol·L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,将使所配制的硫酸溶液浓度偏低的是 。
| A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒。 |
| B.烧杯内的稀硫酸未冷却至室温就转移至容量瓶中 |
| C.用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切。 |
| D.用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切。 |

普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
⑴.操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为 (填化学式);
(2)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:(答案写在答题卷上)
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1.检验Cl— | 取少许滤液于试管中,加入 | 产生白色沉淀 | 含有Cl— |
| 2.检验NH4+ | 取少许滤液于试管中,加入 | | 含有NH4+ |
| 3.检验Zn2+ | 取少许滤液于试管中,加入稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】用沉淀滴定法 快速测定NaI等碘化物溶液中c(I-),实验过程包括准备标准溶液和滴定待测溶液。
I.准备标准溶液
a.准确称取AgNO3基准物4.2468g(0.0250mol)后,配制成250mL标准溶液放在棕色试剂瓶中避光保存备用。
b.配制并标定100mL0.1000mol•L-1NH4SCN标准溶液,备用。
II.滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中。
b.加入25.00mL0.1000mol•L-1AgNO3溶液(过量),使I-完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.1000mol•L-1NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如表:
f.数据处理。
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯、玻璃棒、胶头滴管外还有___ 。
(2)滴定应在pH<0.5的条件下进行,其原因是抑制Fe3+的水解。Fe3+的水解离子方程式为:___ 。
(3)测得c(I—)=___ mol•L-1。(结果保留小数点后四位)
(4)在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为___ 。
(5)判断下列操作对c(I-)测定结果的影响(填“偏高”、“偏低”或“无影响”)
若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果___ 。
I.准备标准溶液
a.准确称取AgNO3基准物4.2468g(0.0250mol)后,配制成250mL标准溶液放在棕色试剂瓶中避光保存备用。
b.配制并标定100mL0.1000mol•L-1NH4SCN标准溶液,备用。
II.滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中。
b.加入25.00mL0.1000mol•L-1AgNO3溶液(过量),使I-完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.1000mol•L-1NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如表:
| 实验序号 | 1 | 2 | 3 |
| 消耗NH4SCN标准溶液体积/mL | 10.24 | 10.02 | 9.98 |
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯、玻璃棒、胶头滴管外还有
(2)滴定应在pH<0.5的条件下进行,其原因是抑制Fe3+的水解。Fe3+的水解离子方程式为:
(3)测得c(I—)=
(4)在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为
(5)判断下列操作对c(I-)测定结果的影响(填“偏高”、“偏低”或“无影响”)
若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室用密度为1.84 g•cm﹣3、溶质的质量分数为98 %的硫酸,配制250 mL物质的量浓度为0.46 mol•L﹣1的硫酸。
(1)98 %的浓硫酸的物质的量浓度为_____ 。
(2)现有下列几种规格的量筒,应选用_____ (填序号)。
①5 mL量筒 ②10 mL量筒 ③50 mL量筒 ④100 mL量筒
(3)实验需要以下步骤:①定容②量取③摇匀④洗涤⑤转移⑥冷却⑦计算⑧装瓶⑨稀释进行顺序为_____ 。
A. ⑦②④⑨⑥③⑤①⑧ B.⑦②⑥⑨⑤④③①⑧
C.⑦②⑨⑥⑤④①③⑧ D. ⑦②⑨⑥④⑤③①⑧
(4)下列操作使所配溶液的物质的量浓度偏高的是______ 。
A.往容量瓶中转移溶液时有少量液体溅出
B.未洗涤稀释浓H2SO4的小烧杯
C.定容时俯视刻度线
D.洗净容量瓶未干燥即用来配制溶液
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
(1)98 %的浓硫酸的物质的量浓度为
(2)现有下列几种规格的量筒,应选用
①5 mL量筒 ②10 mL量筒 ③50 mL量筒 ④100 mL量筒
(3)实验需要以下步骤:①定容②量取③摇匀④洗涤⑤转移⑥冷却⑦计算⑧装瓶⑨稀释进行顺序为
A. ⑦②④⑨⑥③⑤①⑧ B.⑦②⑥⑨⑤④③①⑧
C.⑦②⑨⑥⑤④①③⑧ D. ⑦②⑨⑥④⑤③①⑧
(4)下列操作使所配溶液的物质的量浓度偏高的是
A.往容量瓶中转移溶液时有少量液体溅出
B.未洗涤稀释浓H2SO4的小烧杯
C.定容时俯视刻度线
D.洗净容量瓶未干燥即用来配制溶液
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
您最近一年使用:0次






