根据元素周期表和元素周期律,回答下列问题。
Ⅰ.将NaOH溶液和NH4Cl溶液混合生成NH3·H2O,验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:_______ 。
Ⅱ.A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图为: ,B、C可形成两种离子化合物B2C和B2C2.据此填空:
,B、C可形成两种离子化合物B2C和B2C2.据此填空:
(1)A的元素名称为_______ ,位于第_______ 周期_______ 族。
(2)A、C、D气态氢化物稳定性由强到弱的顺序是(填化学式)_______ 。
(3)A、B形成的含氧酸盐与D最高价氧化物对应的水化物反应的方程式是_______ 。
(4)利用下图装置若要证明非金属性:C>Si,则A中加_______ ,B中加Na2CO3、C中加_______ ,观察到C中溶液的现象为_______ 。

Ⅰ.将NaOH溶液和NH4Cl溶液混合生成NH3·H2O,验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:
Ⅱ.A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图为:
 ,B、C可形成两种离子化合物B2C和B2C2.据此填空:
,B、C可形成两种离子化合物B2C和B2C2.据此填空:(1)A的元素名称为
(2)A、C、D气态氢化物稳定性由强到弱的顺序是(填化学式)
(3)A、B形成的含氧酸盐与D最高价氧化物对应的水化物反应的方程式是
(4)利用下图装置若要证明非金属性:C>Si,则A中加

更新时间:2020-12-24 17:09:48
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)四种元素的原子半径如下表:
由此可推理:决定原子半径大小的因素有_______
(2) 和
和 都是化工生产中的重要物质。
都是化工生产中的重要物质。
① 的沸点(-33.5℃)高于
的沸点(-33.5℃)高于 的沸点(-129℃)的主要原因是
的沸点(-129℃)的主要原因是_______
② 的一种下游产品三聚氟氰(分子式为:
的一种下游产品三聚氟氰(分子式为: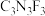 ),分子结构中显示有环状结构,请从价键理论和物质的相对稳定性角度写出三聚氟氰的结构式
),分子结构中显示有环状结构,请从价键理论和物质的相对稳定性角度写出三聚氟氰的结构式_______ 。
(1)四种元素的原子半径如下表:
| 元素符号 | Li | Be | Na | S | Cl |
| 原子半径/pm | 152 | 89 | 186 | 102 | 99 |
由此可推理:决定原子半径大小的因素有
(2)
 和
和 都是化工生产中的重要物质。
都是化工生产中的重要物质。①
 的沸点(-33.5℃)高于
的沸点(-33.5℃)高于 的沸点(-129℃)的主要原因是
的沸点(-129℃)的主要原因是②
 的一种下游产品三聚氟氰(分子式为:
的一种下游产品三聚氟氰(分子式为: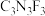 ),分子结构中显示有环状结构,请从价键理论和物质的相对稳定性角度写出三聚氟氰的结构式
),分子结构中显示有环状结构,请从价键理论和物质的相对稳定性角度写出三聚氟氰的结构式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位-构-性的关系,揭示了元素间的内在联系,下图是元素周期表的一部分,回答下列问题:

(1)根据元素周期律推断:
①阴影部分元素最高价氧化物对应的水化物酸性最强的是_______ (写化学式);
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4_______ H2SeO4(填“>”、“<”、“=”);
③氢化物的还原性:H2S_______ PH3(填“>”、“<”、“=”);
④半径比较:F_______ S(填“>”、“<”、“=”)。
(2)元素Tl的原子序数是_______ ;
(3)锡(Sn)是很早便被发现和使用的金属,完成下列填空:
①SnO2能与NaOH反应生成钠盐,写出反应的离子方程式_______ ;
②解释表中卤化锡的熔、沸点的变化规律_______ ;
③锡溶于盐酸得到溶液A,向A中通入氯气,氯气被还原。写出反应化学方程式_______ ;

(1)根据元素周期律推断:
①阴影部分元素最高价氧化物对应的水化物酸性最强的是
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4
③氢化物的还原性:H2S
④半径比较:F
(2)元素Tl的原子序数是
(3)锡(Sn)是很早便被发现和使用的金属,完成下列填空:
①SnO2能与NaOH反应生成钠盐,写出反应的离子方程式
②解释表中卤化锡的熔、沸点的变化规律
| 化学式 | SnCl4 | SnBr4 | SnI4 |
| 熔点/℃ | -33 | 31 | 144.5 |
| 沸点/℃ | 114.1 | 202 | 364 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知五种元素的原子序数的大小顺序为C>A>B>D>E,A,C同周期,B,C同主族。A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子的分子。试回答下列问题:
(1)写出五种元素的元素符号:A:________ 、B:________ 、C:________ 、D:________ 、E:________ 。
(2)用电子式表示离子化合物A2B的形成过程:______________________ 。
(3)写出下列物质的电子式:
①D元素形成的单质:_______________________________________________ 。
②E与B形成的化合物:_____________________________________________ 。
③A,B,E形成的化合物:___________________________________________ 。
④D与E形成的化合物:______________________________________________ 。
⑤C,D,E形成的离子化合物:________________________________________ 。
(1)写出五种元素的元素符号:A:
(2)用电子式表示离子化合物A2B的形成过程:
(3)写出下列物质的电子式:
①D元素形成的单质:
②E与B形成的化合物:
③A,B,E形成的化合物:
④D与E形成的化合物:
⑤C,D,E形成的离子化合物:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据图所示装置中的实验现象及元素周期表和元素周期律,完成下列各小题。

(1)若a为稀盐酸,b为 ,c为
,c为 ,a与b反应产生气泡,且
,a与b反应产生气泡,且 溶液中出现白色沉淀,下列叙述正确的是
溶液中出现白色沉淀,下列叙述正确的是__________ (填标号,下同)。
A.酸性:
B.元素的非金属性:
C.酸性:
(2)若a为浓盐酸,b为 ,c为
,c为 ,a与b反应产生黄绿色气体,且
,a与b反应产生黄绿色气体,且 溶液中出现淡黄色沉淀,下列叙述不正确的是
溶液中出现淡黄色沉淀,下列叙述不正确的是__________ 。
A.氧化性:
B.最高价氧化物对应水化物的酸性:
C.还原性:

(1)若a为稀盐酸,b为
 ,c为
,c为 ,a与b反应产生气泡,且
,a与b反应产生气泡,且 溶液中出现白色沉淀,下列叙述正确的是
溶液中出现白色沉淀,下列叙述正确的是A.酸性:

B.元素的非金属性:

C.酸性:

(2)若a为浓盐酸,b为
 ,c为
,c为 ,a与b反应产生黄绿色气体,且
,a与b反应产生黄绿色气体,且 溶液中出现淡黄色沉淀,下列叙述不正确的是
溶液中出现淡黄色沉淀,下列叙述不正确的是A.氧化性:

B.最高价氧化物对应水化物的酸性:

C.还原性:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
I.用元素符号表示
(1)将钠、镁、铝各2g分别投入盛足量0.05mol/L盐酸烧杯中,实验结果:____ 与盐酸反应最剧烈;_____ 与盐酸反应转移电子最多。钠、镁、铝中第一电离能由小到大的顺序是_____ 。
(2)向Na2SiO3溶液中通入CO2出现胶状沉淀,可证明____ 元素得电子能力强,反应的离子方程式为_______ 。实验结论:随原子序数增大,同周期元素失电子能力依次_______ (填“增强”或“减弱”,下同),得电子能力依次_______ 。
II.利用如图装置可验证同主族元素非金属性的变化规律。
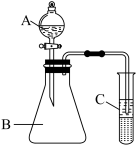
(3)仪器A的名称为_______ 。
(4)若要证明非金属性:Cl>Br,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加KBr溶液和CCl4反应一段时间后,将C振荡、静置,观察到C中现象是_______ ,此装置存在的不足之处是_______ 。
I.用元素符号表示
(1)将钠、镁、铝各2g分别投入盛足量0.05mol/L盐酸烧杯中,实验结果:
(2)向Na2SiO3溶液中通入CO2出现胶状沉淀,可证明
II.利用如图装置可验证同主族元素非金属性的变化规律。

(3)仪器A的名称为
(4)若要证明非金属性:Cl>Br,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加KBr溶液和CCl4反应一段时间后,将C振荡、静置,观察到C中现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图所示是部分短周期元素原子半径与原子序数的关系,回答下列问题: 在周期表中的位置是
在周期表中的位置是____________________ 。
(2) 、
、 的最高价氧化物对应的水化物中,酸性较强的物质是
的最高价氧化物对应的水化物中,酸性较强的物质是______ (填化学式)。
(3)用电子式表示化合物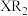 的形成过程
的形成过程________________________ 。
(4)在溶液中,元素 、
、 、
、 形成的某化合物与
形成的某化合物与 的最高价氧化物对应的水化合物稀溶液之间反应既能产生无色刺激性气味气体,又能产生淡黄色沉淀,请写出发生反应的离子方程式
的最高价氧化物对应的水化合物稀溶液之间反应既能产生无色刺激性气味气体,又能产生淡黄色沉淀,请写出发生反应的离子方程式_______________ 。
(5)为验证卤族部分元素单质氧化性的递变规律,设计如图装置进行实验,请回答: 与
与 的氧化性强弱:通入一定量
的氧化性强弱:通入一定量 的单质,充分反应后,将
的单质,充分反应后,将 中液体滴入试管内,取下试管,充分振荡、静置,可观察到
中液体滴入试管内,取下试管,充分振荡、静置,可观察到____________________ ;
该实验必须控制加入的 单质的量,否则得不出
单质的量,否则得不出 的氧化性比
的氧化性比 强。理由是
强。理由是______ 。
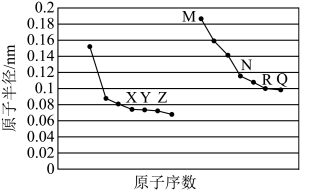
 在周期表中的位置是
在周期表中的位置是(2)
 、
、 的最高价氧化物对应的水化物中,酸性较强的物质是
的最高价氧化物对应的水化物中,酸性较强的物质是(3)用电子式表示化合物
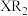 的形成过程
的形成过程(4)在溶液中,元素
 、
、 、
、 形成的某化合物与
形成的某化合物与 的最高价氧化物对应的水化合物稀溶液之间反应既能产生无色刺激性气味气体,又能产生淡黄色沉淀,请写出发生反应的离子方程式
的最高价氧化物对应的水化合物稀溶液之间反应既能产生无色刺激性气味气体,又能产生淡黄色沉淀,请写出发生反应的离子方程式(5)为验证卤族部分元素单质氧化性的递变规律,设计如图装置进行实验,请回答:
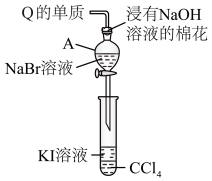
 与
与 的氧化性强弱:通入一定量
的氧化性强弱:通入一定量 的单质,充分反应后,将
的单质,充分反应后,将 中液体滴入试管内,取下试管,充分振荡、静置,可观察到
中液体滴入试管内,取下试管,充分振荡、静置,可观察到该实验必须控制加入的
 单质的量,否则得不出
单质的量,否则得不出 的氧化性比
的氧化性比 强。理由是
强。理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(I)小明同学想通过比较两种最高价氧化物水化物的酸性强弱来验证S与C的非金属性的强弱,他查阅了资料:可以利用强酸制备弱酸的原理来判断酸性强弱。于是小明采用了下图所示的装置进行实验。请回答:

(1)仪器A的名称是________ ,应盛放下列药品中的__________ 。
a.稀硫酸 b.亚硫酸 c.氢硫酸 d.盐酸
(2)仪器B的名称是________ ,应盛放下列药品中的__________ 。
a.碳酸钙 b.硫酸钠 c.氯化钠 d.碳酸钠
(3)仪器C中盛放的药品是澄清石灰水,如果看到的现象是澄清石灰水变浑浊,证明B中发生反应生成了_____________ ,即可说明H2SO4 比H2CO3 酸性强,非金属性S比C强,B中发生反应的离子方程式为______________________________ 。
(II)(1)用电子式表示下列化合物的形成过程:
CaF2:_____________________________________________
H2S:______________________________________________
(2)有下列物质:①NaOH ②I2 ③MgCl2 ④Na2O2 ⑤氩气 回答下列问题:
①不存在化学键的是_________________________ ,
②既存在离子键又存在极性键的是__________________ 。

(1)仪器A的名称是
a.稀硫酸 b.亚硫酸 c.氢硫酸 d.盐酸
(2)仪器B的名称是
a.碳酸钙 b.硫酸钠 c.氯化钠 d.碳酸钠
(3)仪器C中盛放的药品是澄清石灰水,如果看到的现象是澄清石灰水变浑浊,证明B中发生反应生成了
(II)(1)用电子式表示下列化合物的形成过程:
CaF2:
H2S:
(2)有下列物质:①NaOH ②I2 ③MgCl2 ④Na2O2 ⑤氩气 回答下列问题:
①不存在化学键的是
②既存在离子键又存在极性键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】设计一个简单的一次性完成实验的装置图,验证盐酸、碳酸、硅酸的酸性强弱。
(1)盐酸、碳酸、硅酸的酸性由强到弱的顺序是______ 。
(2)利用如图所示的仪器可以组装成实验装置,则仪器的连接顺序为______ 接______ ,______ 接______ ,______ 接______ 。

(3)有关反应的化学方程式为______ 、______ 。
(1)盐酸、碳酸、硅酸的酸性由强到弱的顺序是
(2)利用如图所示的仪器可以组装成实验装置,则仪器的连接顺序为

(3)有关反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】一定条件下,金属钠和CO2可制得金刚石:4Na+3CO2 2Na2CO3+C(s,金刚石)
2Na2CO3+C(s,金刚石)
完成下列填空:
(1)上述反应中涉及的元素的原子半径从大到小的顺序为____ 。
(2)能证明碳元素与氧元素非金属强弱的事实是___ (选填编号)。
a.最高价氧化物水化物的酸性 b.两种元素的气态氢化物的沸点
c.CO2中元素的化合价 d.气体氢化物受热分解的温度
(3)高压下,科学家成功地将CO2转化为具有类似SiO2结构的原子晶体,比较SiO2与CO2这两种原子晶体的熔沸点高低,并说明理由:___ 。
(4)若在2L密闭容器中,10min内金属钠减少了0.2mol,则CO2的平均反应速率为___ 。该反应在常压1000℃下进行,根据右表数据,该反应的平衡常数表达式K=___ 。
(5)若在2L密闭容器中,常压、1000℃下,起始时,下列物理量能说明该反应已达到平衡状态的是____ 。
a.气体的平均摩尔质量不变 b.3v消耗(Na)=4v生成(CO2)
c.气体的密度不变 d. 的比值不变
的比值不变
 2Na2CO3+C(s,金刚石)
2Na2CO3+C(s,金刚石)完成下列填空:
(1)上述反应中涉及的元素的原子半径从大到小的顺序为
(2)能证明碳元素与氧元素非金属强弱的事实是
a.最高价氧化物水化物的酸性 b.两种元素的气态氢化物的沸点
c.CO2中元素的化合价 d.气体氢化物受热分解的温度
(3)高压下,科学家成功地将CO2转化为具有类似SiO2结构的原子晶体,比较SiO2与CO2这两种原子晶体的熔沸点高低,并说明理由:
| 常压 | 熔点(℃) | 沸点(℃) |
| 钠 | 97.8 | 882.9 |
| Na2CO3 | 851 | 1850分解 |
| 金刚石 | 3550 | … |
| 石墨 | 3850 | 4250 |
(4)若在2L密闭容器中,10min内金属钠减少了0.2mol,则CO2的平均反应速率为
(5)若在2L密闭容器中,常压、1000℃下,起始时,下列物理量能说明该反应已达到平衡状态的是
a.气体的平均摩尔质量不变 b.3v消耗(Na)=4v生成(CO2)
c.气体的密度不变 d.
 的比值不变
的比值不变
您最近一年使用:0次



