某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:
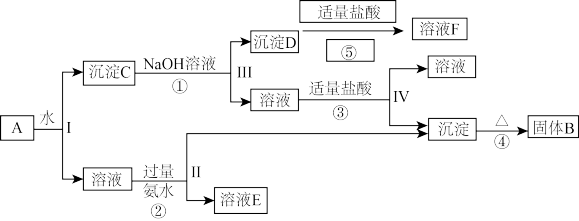
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是__ 。
(2)根据上述框图反应关系,写出下列B、D、E所含物质的化学式:
固体B__ ;沉淀D_ ;溶液E__ 。
(3)分别写出Al2O3和Fe2O3在工业上的一种主要用途:
Al2O3__ ;Fe2O3__ 。
(4)写出①、④两个反应的化学方程式:
①__ ;④__ 。
(5)写出②、③两个反应的离子方程式:
②__ ;③__ 。

据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是
(2)根据上述框图反应关系,写出下列B、D、E所含物质的化学式:
固体B
(3)分别写出Al2O3和Fe2O3在工业上的一种主要用途:
Al2O3
(4)写出①、④两个反应的化学方程式:
①
(5)写出②、③两个反应的离子方程式:
②
更新时间:2020/12/25 17:49:58
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】过氧化钙(CaO2)难溶于水,可与水缓慢反应;不溶于醇类、乙醚等,易与酸反应,常用作杀菌剂、防腐剂等。某小组设计实验利用氯化钙在碱性环境下和双氧水反应制备过氧化钙:
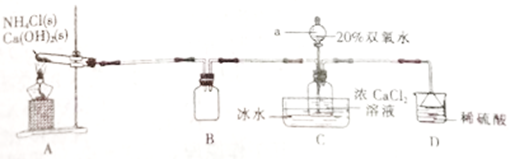
请回答下列问题:
(1)仪器a的名称是________________ ;B装置作用是____________________ 。
(2)写出A中发生反应的化学方程式:________________________________________ 。
(3)实验过程中,先启动A中反应,通入一段时间气体后,再向C中广口瓶里滴加双氧水。先通入气体的目的是____________ 。向C中广口瓶滴加双氧水的具体操作是________________ 。
(4)写出C中广口瓶里发生反应的主要离子方程式:______________________________ 。
(5)长途运输海鲜产品,常用CaO2作供氧剂,不用Na2O2,其主要原因是__________ 。
(6)实验完毕后,经过滤、乙醇洗涤低温烘干,得到CaO2·8H2O粗产品,在105℃脱水得到CaO2产品。已知:在350℃时CaO2迅速分解生成CaO和O2。利用如图装置测定产品纯度(夹持仪器和加热装置省略):
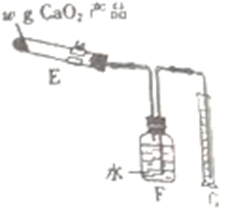
实验室收集到VmLO2(已折算为标准状况下),则该样品纯度为__________ %。若读数时G中液面高于F中液面,测得结果__________ (填“偏高”“偏低”或“无影响”)

请回答下列问题:
(1)仪器a的名称是
(2)写出A中发生反应的化学方程式:
(3)实验过程中,先启动A中反应,通入一段时间气体后,再向C中广口瓶里滴加双氧水。先通入气体的目的是
(4)写出C中广口瓶里发生反应的主要离子方程式:
(5)长途运输海鲜产品,常用CaO2作供氧剂,不用Na2O2,其主要原因是
(6)实验完毕后,经过滤、乙醇洗涤低温烘干,得到CaO2·8H2O粗产品,在105℃脱水得到CaO2产品。已知:在350℃时CaO2迅速分解生成CaO和O2。利用如图装置测定产品纯度(夹持仪器和加热装置省略):

实验室收集到VmLO2(已折算为标准状况下),则该样品纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】氧化还原反应与离子反应在生产生活与科学实验中有重要作用,回答下列问题。
I.过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。根据下列反应回答问题:
A.
B.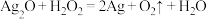
C.
D.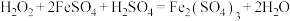
(1)上述反应中,H2O2仅体现氧化性的反应是_______ (填字母序号,下同),H2O2既体现氧化性又体现还原性的反应是_______ ,H2O2、Ag2O、Fe2(SO4)3的氧化性由强到弱的顺序是_______ 。
(2)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒: 、
、 、
、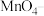 、
、 、
、 、
、 ,则反应的离子方程式为
,则反应的离子方程式为_______
Ⅱ.有一包固体粉末,其中可能含有NaCl、Ba(NO3)2、CuSO4、Na2CO3中的一种或几种,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色:
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③另取①中过滤后的滤液加入足量AgNO3溶液,产生白色沉淀。
根据上述实验事实,回答下列问题:
(3)原固体粉末中一定含有的物质是_______ ,一定不含有的物质是_______ ,可能含有的物质是_______ 。(写化学式)
(4)写出对应各步反应的离子方程式:①_______ ;②_______ 。
I.过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。根据下列反应回答问题:
A.

B.
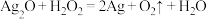
C.

D.
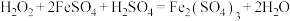
(1)上述反应中,H2O2仅体现氧化性的反应是
(2)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:
 、
、 、
、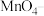 、
、 、
、 、
、 ,则反应的离子方程式为
,则反应的离子方程式为Ⅱ.有一包固体粉末,其中可能含有NaCl、Ba(NO3)2、CuSO4、Na2CO3中的一种或几种,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色:
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③另取①中过滤后的滤液加入足量AgNO3溶液,产生白色沉淀。
根据上述实验事实,回答下列问题:
(3)原固体粉末中一定含有的物质是
(4)写出对应各步反应的离子方程式:①
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.铸铁的主要成分为Fe和C,用下图所示实验研究铸铁与热的浓硫酸的反应(夹持和加热装置已略去)。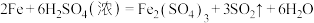 、
、________ 。
(2)实验现象:①________ ,证明确实有SO2生成。
②U型管b侧棉花的紫红色变化不明显、澄清石灰水中生成白色浑浊物。证明________ 。
(3)检测反应后A中所得溶液中含有 的实验方法为:取少量待测溶液,将其加入适量水中稀释,滴加
的实验方法为:取少量待测溶液,将其加入适量水中稀释,滴加________ ,现象为________ 证明有 。
。
(4)若取上述反应生成的0.56L(标准状况下)混合气体直接通入足量H2O2溶液中,反应完全后,向溶液中加入足量BaCl2溶液生成白色沉淀,分离、干燥后得到固体4.66g。混合气体中SO2的体积分数为________ 。
Ⅱ.纳米Fe具有很高的活性,易被氧化使其表面形成氧化层,对制备纳米Fe并对其还原去除水中的硝酸盐污染物进行研究,纳米Fe将 还原为
还原为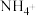 的转化关系如下:
的转化关系如下:

(5)纳米Fe制备原理: ,其中电负性H>B,反应中的氧化剂是
,其中电负性H>B,反应中的氧化剂是________ 。
(6)酸性条件下,纳米Fe和 反应生成
反应生成 和
和 的离子方程式是
的离子方程式是________ 。
(7)检验溶液中 的操作和现象是
的操作和现象是________ 。
(8)溶液初始pH较低有利于 的去除,可能的原因是
的去除,可能的原因是________ (答1条)。
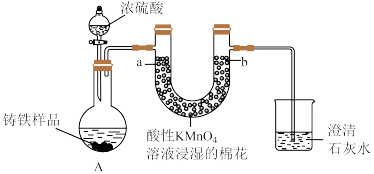
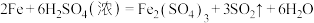 、
、(2)实验现象:①
②U型管b侧棉花的紫红色变化不明显、澄清石灰水中生成白色浑浊物。证明
(3)检测反应后A中所得溶液中含有
 的实验方法为:取少量待测溶液,将其加入适量水中稀释,滴加
的实验方法为:取少量待测溶液,将其加入适量水中稀释,滴加 。
。(4)若取上述反应生成的0.56L(标准状况下)混合气体直接通入足量H2O2溶液中,反应完全后,向溶液中加入足量BaCl2溶液生成白色沉淀,分离、干燥后得到固体4.66g。混合气体中SO2的体积分数为
Ⅱ.纳米Fe具有很高的活性,易被氧化使其表面形成氧化层,对制备纳米Fe并对其还原去除水中的硝酸盐污染物进行研究,纳米Fe将
 还原为
还原为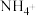 的转化关系如下:
的转化关系如下:
(5)纳米Fe制备原理:
 ,其中电负性H>B,反应中的氧化剂是
,其中电负性H>B,反应中的氧化剂是(6)酸性条件下,纳米Fe和
 反应生成
反应生成 和
和 的离子方程式是
的离子方程式是(7)检验溶液中
 的操作和现象是
的操作和现象是(8)溶液初始pH较低有利于
 的去除,可能的原因是
的去除,可能的原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
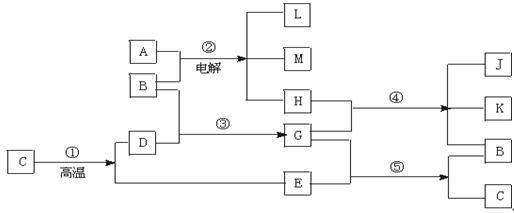
【推荐1】已知A是我们家庭中常见的一种调味剂,其焰色反应呈黄色; E是引起温室效应的主要气体之一;反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应。根据下列反应框图填空:
B_____________ ,C________________ ,H_____________ 。
(2)写出②发生反应的化学反应方程式
___________________________ 。
写出④发生反应的化学方程式,并用双线桥表示出电子转移的方向和数目______________________________________ 。
B
(2)写出②发生反应的化学反应方程式
写出④发生反应的化学方程式,并用双线桥表示出电子转移的方向和数目
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】在下列物质的转化关系中,A是一种固体单质,且常作半导体材料,E是一种白色沉淀,F是最轻的气体单质。
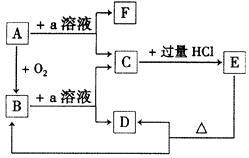
据此填写:
(1)B的化学式是____________ ,目前在现代通讯方面B已被用作_____________ 主要原料。
(2)B和a溶液反应的离子方程式是_____________________ 。
(3)A和a溶液反应的离子方程式是_____________________ 。
(4)C和过量盐酸反应的离子方程式是____________________ 。

据此填写:
(1)B的化学式是
(2)B和a溶液反应的离子方程式是
(3)A和a溶液反应的离子方程式是
(4)C和过量盐酸反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知X、Y均为有漂白性和刺激性气味的气体,有以下转化关系,部分产物未标出。

试回答:
(1)写出下列物质的化学式:X________ 、Y______ 、A______ 、B________ 、C________ 。
(2)反应①的化学方程式为____________________________ ,已知反应②的产物为FeCl2、HCl和H2SO4,试写出该反应的离子方程式:___________________________ 。

试回答:
(1)写出下列物质的化学式:X
(2)反应①的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】治疗胃酸过多的药物达喜(其式量不超过 700)由五种短周期元素组成,按如图流程进行实验以确定其组成。
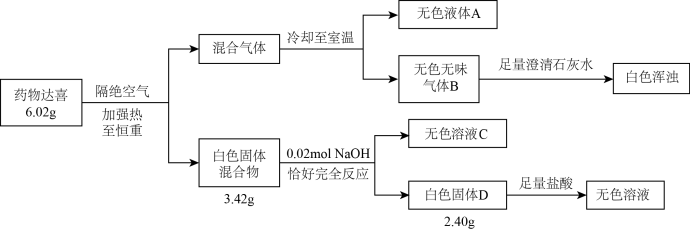
请回答:
(1)达喜的化学式是_________ 。
(2)达喜与胃酸(含稀盐酸)反应的化学方程式是_______ 。
(3)气体 B 与环氧丙烷(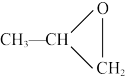 )可制得一种可降解高聚物,该反应的化学方程式是
)可制得一种可降解高聚物,该反应的化学方程式是_____ (有机物用结构简式表示)。

请回答:
(1)达喜的化学式是
(2)达喜与胃酸(含稀盐酸)反应的化学方程式是
(3)气体 B 与环氧丙烷(
 )可制得一种可降解高聚物,该反应的化学方程式是
)可制得一种可降解高聚物,该反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】将晶体X加热分解可得A、B、D、E、F和水六种产物,其中A、B、D都是中学化学中常见的氧化物,气体E是单质F所含元素的氢化物。
(1)A能溶于强酸、强碱,写出A与强碱溶液反应的离子方程式:____________________ 。
(2)B、D都是酸性氧化物且组成元素相同,D溶于水得强酸,则B、D分子中除氧元素外所含另一种元素在元素周期表中的位置是______________________ 。
(3)E能使湿润的红色石蕊试纸变蓝,实验室制取E气体的化学方程式为___________ ,制得的气体可用如图所示装置收集,则气体应从______ (填“A”或“B”)通入。
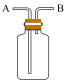
(4)由各分解产物的物质的量之比推测X的组成类似于明矾,若向X的浓溶液中滴加浓NaOH溶液至过量,现象依次为__________ 、____________ 、________ 。
(5)取一定量的X晶体分解,若生成1 mol F,则必同时生成____________ (填化学式)________ mol。
(1)A能溶于强酸、强碱,写出A与强碱溶液反应的离子方程式:
(2)B、D都是酸性氧化物且组成元素相同,D溶于水得强酸,则B、D分子中除氧元素外所含另一种元素在元素周期表中的位置是
(3)E能使湿润的红色石蕊试纸变蓝,实验室制取E气体的化学方程式为

(4)由各分解产物的物质的量之比推测X的组成类似于明矾,若向X的浓溶液中滴加浓NaOH溶液至过量,现象依次为
(5)取一定量的X晶体分解,若生成1 mol F,则必同时生成
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。_______ 、E_______ 、J_______ 、G_______ 。
(2)按要求写方程式:
①A+B→C+D的化学方程式:_______ ;
②F→G的化学方程式:_______ ;
③C→I的离子方程式:_______ ;
④B与过量NaOH溶液反应的离子方程式:_______ ;
⑤向E溶液中通入Cl2的离子方程式:_______
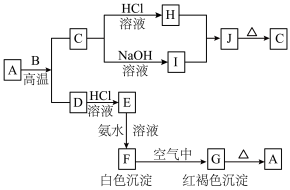
(2)按要求写方程式:
①A+B→C+D的化学方程式:
②F→G的化学方程式:
③C→I的离子方程式:
④B与过量NaOH溶液反应的离子方程式:
⑤向E溶液中通入Cl2的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】废旧锌锰电池中的黑锰粉含有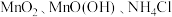 和少量
和少量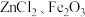 及炭黑等,为了保护环境、充分利用锰资源,通过如图所示流程制备
及炭黑等,为了保护环境、充分利用锰资源,通过如图所示流程制备 。
。
(1) 在元素周期表中的位置为
在元素周期表中的位置为_______ 。
(2)“滤液a”的主要成分为_______ (填化学式);部分物质溶解度曲线如图所示, “滤液a”经过“一系列操作”可以得到该溶质,“一系列操作”为:______ 、洗涤、干燥。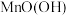 转化为
转化为 ,“焙烧”的目的是
,“焙烧”的目的是______ 。
(4)探究“酸浸”中 溶解的适宜操作。
溶解的适宜操作。
实验I.向 中加入
中加入 溶液,产生大量气泡;再加入稀
溶液,产生大量气泡;再加入稀 ,固体未明显溶解。
,固体未明显溶解。
实验Ⅱ.向 中加入稀
中加入稀 ,固体未溶解;再加入
,固体未溶解;再加入 溶液,产生大量气泡,固体完全溶解。
溶液,产生大量气泡,固体完全溶解。
①实验I中 的作用是
的作用是______ 。
②写出实验Ⅱ中发生反应的离子方程式:______ 。
③由实验可知,“酸浸”溶解 时试剂的添加顺序是
时试剂的添加顺序是_____ 。
(5)加入 调
调 ,使
,使 完全沉淀,如何证明得到的
完全沉淀,如何证明得到的 溶液中
溶液中 沉淀完全,写出实验的操作步骤:
沉淀完全,写出实验的操作步骤:_______ 。
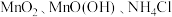 和少量
和少量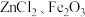 及炭黑等,为了保护环境、充分利用锰资源,通过如图所示流程制备
及炭黑等,为了保护环境、充分利用锰资源,通过如图所示流程制备 。
。
(1)
 在元素周期表中的位置为
在元素周期表中的位置为(2)“滤液a”的主要成分为

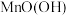 转化为
转化为 ,“焙烧”的目的是
,“焙烧”的目的是(4)探究“酸浸”中
 溶解的适宜操作。
溶解的适宜操作。实验I.向
 中加入
中加入 溶液,产生大量气泡;再加入稀
溶液,产生大量气泡;再加入稀 ,固体未明显溶解。
,固体未明显溶解。实验Ⅱ.向
 中加入稀
中加入稀 ,固体未溶解;再加入
,固体未溶解;再加入 溶液,产生大量气泡,固体完全溶解。
溶液,产生大量气泡,固体完全溶解。①实验I中
 的作用是
的作用是②写出实验Ⅱ中发生反应的离子方程式:
③由实验可知,“酸浸”溶解
 时试剂的添加顺序是
时试剂的添加顺序是(5)加入
 调
调 ,使
,使 完全沉淀,如何证明得到的
完全沉淀,如何证明得到的 溶液中
溶液中 沉淀完全,写出实验的操作步骤:
沉淀完全,写出实验的操作步骤:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】硫酸铁铵是分析化学中常用试剂,其晶体化学式为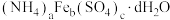 。实验室模拟用废铁屑[成分为铁和少量铁锈(用
。实验室模拟用废铁屑[成分为铁和少量铁锈(用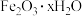 表示)]制取硫酸铁铵晶体,具体流程如下图所示:
表示)]制取硫酸铁铵晶体,具体流程如下图所示:

(1)步骤①中,铁锈与硫酸反应的离子方程式为_______ 。该步骤采用水浴加热,而不用明火加热,原因是_______ 。
(2)步骤②中加入足量 的目的是
的目的是_______ 。
(3)硫酸铁铵晶体组成的测定。
步骤1:准确称取质量为4.820g固体在酸性条件下溶于水配成100.00mL溶液A;
步骤2:取25.00mL溶液A,加入足量的 溶液,过滤得1.165g沉淀;
溶液,过滤得1.165g沉淀;
步骤3:取25.00mL溶液A,加入足量氢氧化钠溶液,过滤、洗涤并灼烧得到0.2g固体;
通过计算确定该晶体的化学式(写出计算过程)。_________
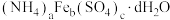 。实验室模拟用废铁屑[成分为铁和少量铁锈(用
。实验室模拟用废铁屑[成分为铁和少量铁锈(用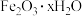 表示)]制取硫酸铁铵晶体,具体流程如下图所示:
表示)]制取硫酸铁铵晶体,具体流程如下图所示:
(1)步骤①中,铁锈与硫酸反应的离子方程式为
(2)步骤②中加入足量
 的目的是
的目的是(3)硫酸铁铵晶体组成的测定。
步骤1:准确称取质量为4.820g固体在酸性条件下溶于水配成100.00mL溶液A;
步骤2:取25.00mL溶液A,加入足量的
 溶液,过滤得1.165g沉淀;
溶液,过滤得1.165g沉淀;步骤3:取25.00mL溶液A,加入足量氢氧化钠溶液,过滤、洗涤并灼烧得到0.2g固体;
通过计算确定该晶体的化学式(写出计算过程)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】ZnSO4∙7H2O可用于测定钢铁及炉渣的含硫量。某工厂下脚料中含锌、镉(Cd)、铜、铁等金属,以该下脚料为原料制备ZnSO4∙7H2O并回收Cu、Cd的工艺流程如图所示:
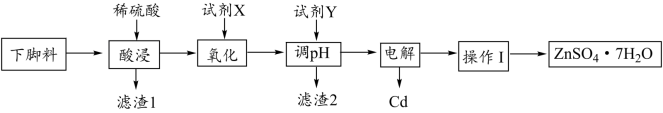
已知部分氢氧化物开始及完全沉淀的pH如表所示(起始时金属离子浓度按0.1mol∙L-1计算):
请回答下列问题:
(1)滤渣1中主要含有___________ (填化学式)。
(2)试剂X是双氧水时,写出氧化过程中发生反应的离子方程式___________ 。
(3)pH的调控范围是___________ 。
(4)操作I包括的操作是___________ 及过滤等,过滤后得到的滤液可以加入___________ (填“酸浸”或“氧化”)步骤循环利用。

已知部分氢氧化物开始及完全沉淀的pH如表所示(起始时金属离子浓度按0.1mol∙L-1计算):
| 氢氧化物 | Fe(OH)3 | Cd(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 1.9 | 7.4 | 6.2 |
| 完全沉淀的pH | 3.2 | 9.5 | 8.2 |
(1)滤渣1中主要含有
(2)试剂X是双氧水时,写出氧化过程中发生反应的离子方程式
(3)pH的调控范围是
(4)操作I包括的操作是
您最近一年使用:0次



