硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下,下列说法正确的是
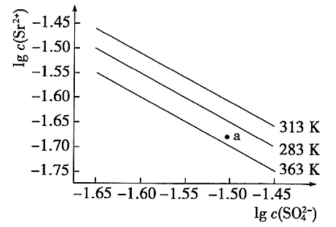

A.温度一定时,Ksp(SrSO4)随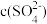 的增大而减小 的增大而减小 |
| B.三个不同温度中,313K时Ksp(SrSO4)最大 |
| C.283K时,图中a点对应的溶液是不饱和溶液 |
| D.283K下的SrSO4饱和溶液升温到363K后变为不饱和溶液 |
更新时间:2020-12-29 09:09:40
|
相似题推荐
【推荐1】要使工业废水中的 沉淀,可用硫酸盐、碳酸盐等作沉淀剂。已知某温度时,
沉淀,可用硫酸盐、碳酸盐等作沉淀剂。已知某温度时,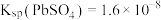 ,
,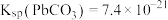 ,
,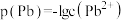 ,
,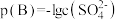 或
或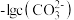 。为研究沉淀效果,在含物质的量浓度相同的
。为研究沉淀效果,在含物质的量浓度相同的 和
和 的混合溶液中滴加
的混合溶液中滴加 溶液产生两种沉淀(温度升高,
溶液产生两种沉淀(温度升高, 、
、 的
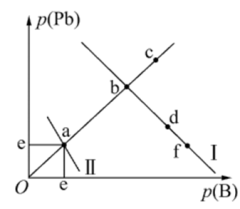
的 均增大),上述反应过程溶液中阳离子、阴离子浓度的负对数关系如图所示。下列说法错误的是。
均增大),上述反应过程溶液中阳离子、阴离子浓度的负对数关系如图所示。下列说法错误的是。
 沉淀,可用硫酸盐、碳酸盐等作沉淀剂。已知某温度时,
沉淀,可用硫酸盐、碳酸盐等作沉淀剂。已知某温度时,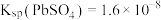 ,
,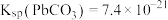 ,
,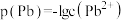 ,
,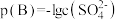 或
或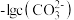 。为研究沉淀效果,在含物质的量浓度相同的
。为研究沉淀效果,在含物质的量浓度相同的 和
和 的混合溶液中滴加
的混合溶液中滴加 溶液产生两种沉淀(温度升高,
溶液产生两种沉淀(温度升高, 、
、 的
的 均增大),上述反应过程溶液中阳离子、阴离子浓度的负对数关系如图所示。下列说法错误的是。
均增大),上述反应过程溶液中阳离子、阴离子浓度的负对数关系如图所示。下列说法错误的是。
A.常温下 的溶解度大于 的溶解度大于 的溶解度 的溶解度 |
| B.向d点对应的溶液中加入对应阴离子的钠盐,溶液组成由d点向f点方向移动 |
C.e约为4且对应的阴离子是 |
| D.对于曲线Ⅰ,对b点的溶液加热(忽略水分蒸发),溶液组成由b点向c点移动 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】硫化锌(ZnS)和硫化铅(PbS)常用于光导体、半导体工业,它们在水中的沉淀溶解平衡曲线如图所示。已知: ,M为Zn或Pb,pM表示
,M为Zn或Pb,pM表示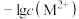 。下列说法正确的是
。下列说法正确的是

 ,M为Zn或Pb,pM表示
,M为Zn或Pb,pM表示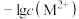 。下列说法正确的是
。下列说法正确的是
| A.曲线I代表PbS的沉淀溶解平衡曲线 |
B.n、q两点溶液中的 :n<q :n<q |
C.图中m点和n点对应的 关系为 关系为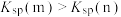 |
D.向m点对应的悬浊液中加入少量 固体,溶液组成由m沿mn曲线向n方向移动 固体,溶液组成由m沿mn曲线向n方向移动 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】还原沉淀法是处理含铬(Cr2O 和CrO
和CrO )废水常用方法,过程如下:CrO
)废水常用方法,过程如下:CrO
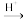 Cr2O
Cr2O
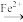 Cr3+
Cr3+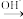 Cr(OH)3,已知废水中Cr的含量为26.0g/L,当溶液中离子浓度小于10-5mol/L时认为离子已经沉淀完全,常温下,Ksp[Cr(OH)3]=1×10-32, Ksp(FeS)=6.3×10-18;Ksp(CuS)=1.3×10-36;Ksp(ZnS)=1.6×10-24,有关叙述中不正确的是( )
Cr(OH)3,已知废水中Cr的含量为26.0g/L,当溶液中离子浓度小于10-5mol/L时认为离子已经沉淀完全,常温下,Ksp[Cr(OH)3]=1×10-32, Ksp(FeS)=6.3×10-18;Ksp(CuS)=1.3×10-36;Ksp(ZnS)=1.6×10-24,有关叙述中不正确的是( )
 和CrO
和CrO )废水常用方法,过程如下:CrO
)废水常用方法,过程如下:CrO
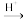 Cr2O
Cr2O
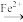 Cr3+
Cr3+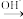 Cr(OH)3,已知废水中Cr的含量为26.0g/L,当溶液中离子浓度小于10-5mol/L时认为离子已经沉淀完全,常温下,Ksp[Cr(OH)3]=1×10-32, Ksp(FeS)=6.3×10-18;Ksp(CuS)=1.3×10-36;Ksp(ZnS)=1.6×10-24,有关叙述中不正确的是( )
Cr(OH)3,已知废水中Cr的含量为26.0g/L,当溶液中离子浓度小于10-5mol/L时认为离子已经沉淀完全,常温下,Ksp[Cr(OH)3]=1×10-32, Ksp(FeS)=6.3×10-18;Ksp(CuS)=1.3×10-36;Ksp(ZnS)=1.6×10-24,有关叙述中不正确的是( )| A.上述三个转化中只有一个涉及氧化还原反应 |
B.第二步离子方程式为Cr2O +4H++6Fe2+=2Cr3++7H2O+6Fe3+ +4H++6Fe2+=2Cr3++7H2O+6Fe3+ |
| C.足量CuSO4溶解在0.1mol/L的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35mol/L |
| D.在ZnS的饱和溶液中加入FeCl2溶液,一定不产生FeS沉淀 |
您最近一年使用:0次
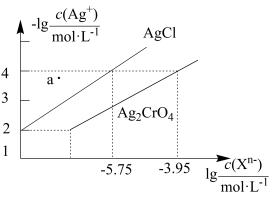
【推荐2】常温下,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的
的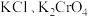 溶液,所得的沉淀溶解平衡图象如图所示(不考虑
溶液,所得的沉淀溶解平衡图象如图所示(不考虑 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是
 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的
的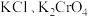 溶液,所得的沉淀溶解平衡图象如图所示(不考虑
溶液,所得的沉淀溶解平衡图象如图所示(不考虑 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是
A.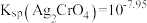 |
B.a点时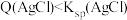 |
C.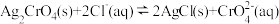 的平衡常数为 的平衡常数为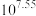 |
D.向等物质的量浓度的 与 与 混合液中逐滴滴加 混合液中逐滴滴加 溶液,先生成 溶液,先生成 沉淀 沉淀 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】25°C时,向10mL0.05mol·L-1的MgCl2溶液中通入氨气,测得溶液中的p(OH-)与p(Mg2+)之间的变化曲线如图所示,[已知:Kb(NH3·H2O)=1.8×10-5,p(X)=-lgc(X),忽略反应过程中溶液体积的变化]。下列说法正确为是


A.a点溶液满足:c(NH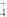 )>c(NH3·H2O)>c(Mg2+)>c(OH-) )>c(NH3·H2O)>c(Mg2+)>c(OH-) |
| B.b点溶液中无Mg(OH)2沉淀产生 |
C.c点溶液满足:2c(Mg2+)+c( )>c(Cl-) )>c(Cl-) |
| D.Ksp[Mg(OH)2]的数量级是10-12 |
您最近一年使用:0次
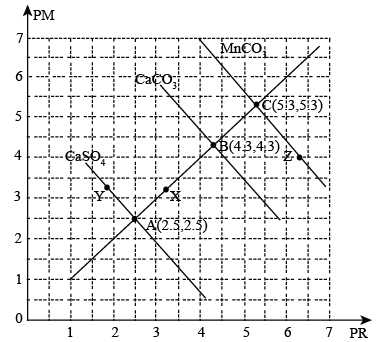
【推荐2】 时,难溶盐
时,难溶盐 、
、 、
、 溶液中阳离子浓度的负对数
溶液中阳离子浓度的负对数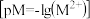 和阴离子浓度的负对数
和阴离子浓度的负对数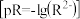 的关系如图所示,下列说法正确的是
的关系如图所示,下列说法正确的是
 时,难溶盐
时,难溶盐 、
、 、
、 溶液中阳离子浓度的负对数
溶液中阳离子浓度的负对数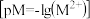 和阴离子浓度的负对数
和阴离子浓度的负对数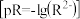 的关系如图所示,下列说法正确的是
的关系如图所示,下列说法正确的是
A.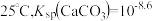 |
B.向A点对应的溶液中加入固体 ,可得到Y点对应的溶液 ,可得到Y点对应的溶液 |
C. ,三种物质的溶解度: ,三种物质的溶解度: |
D. ,向 ,向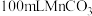 饱和溶液中加入 饱和溶液中加入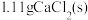 ,有 ,有 沉淀生成 沉淀生成 |
您最近一年使用:0次
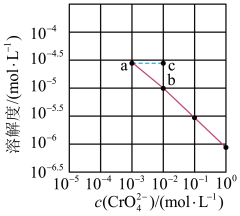
【推荐1】溶解度也可用物质的量浓度表示。已知25℃时, 在
在 浓度不同的溶液中的溶解度如图所示,下列说法正确的是
浓度不同的溶液中的溶解度如图所示,下列说法正确的是
 在
在 浓度不同的溶液中的溶解度如图所示,下列说法正确的是
浓度不同的溶液中的溶解度如图所示,下列说法正确的是
A.图中a、b两点 相同 相同 |
B.图中a点与b点对应的 的溶度积相等 的溶度积相等 |
C.在a点向溶液中加入少量 ,溶解度可变为c点 ,溶解度可变为c点 |
D.该温度下, 溶度积的数量级为 溶度积的数量级为 |
您最近一年使用:0次
【推荐2】要使工业废水中的 沉淀,可用硫酸盐、碳酸盐等作沉淀剂。已知某温度时,
沉淀,可用硫酸盐、碳酸盐等作沉淀剂。已知某温度时,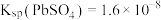 ,
,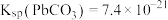 ,
,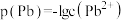 ,
,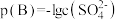 或
或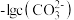 。为研究沉淀效果,在含物质的量浓度相同的
。为研究沉淀效果,在含物质的量浓度相同的 和
和 的混合溶液中滴加
的混合溶液中滴加 溶液产生两种沉淀(温度升高,
溶液产生两种沉淀(温度升高, 、
、 的
的 均增大),上述反应过程溶液中阳离子、阴离子浓度的负对数关系如图所示。下列说法错误的是。
均增大),上述反应过程溶液中阳离子、阴离子浓度的负对数关系如图所示。下列说法错误的是。

 沉淀,可用硫酸盐、碳酸盐等作沉淀剂。已知某温度时,
沉淀,可用硫酸盐、碳酸盐等作沉淀剂。已知某温度时,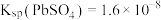 ,
,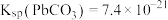 ,
,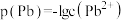 ,
,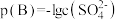 或
或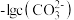 。为研究沉淀效果,在含物质的量浓度相同的
。为研究沉淀效果,在含物质的量浓度相同的 和
和 的混合溶液中滴加
的混合溶液中滴加 溶液产生两种沉淀(温度升高,
溶液产生两种沉淀(温度升高, 、
、 的
的 均增大),上述反应过程溶液中阳离子、阴离子浓度的负对数关系如图所示。下列说法错误的是。
均增大),上述反应过程溶液中阳离子、阴离子浓度的负对数关系如图所示。下列说法错误的是。
A.常温下 的溶解度大于 的溶解度大于 的溶解度 的溶解度 |
| B.向d点对应的溶液中加入对应阴离子的钠盐,溶液组成由d点向f点方向移动 |
C.e约为4且对应的阴离子是 |
| D.对于曲线Ⅰ,对b点的溶液加热(忽略水分蒸发),溶液组成由b点向c点移动 |
您最近一年使用:0次


 +2
+2 +3H2O=5
+3H2O=5 +2Mn2++6OH-
+2Mn2++6OH- +Ba2++OH-=BaSO4↓+H2O
+Ba2++OH-=BaSO4↓+H2O
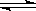 Ba2+(aq)+SO(aq) Ksp=c(Ba2+)·c(SO ),沉淀溶解平衡曲线如图所示。 下列说法正确的是
Ba2+(aq)+SO(aq) Ksp=c(Ba2+)·c(SO ),沉淀溶解平衡曲线如图所示。 下列说法正确的是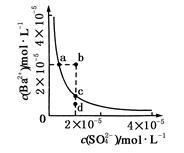
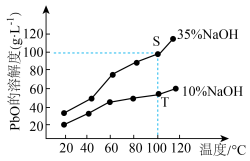
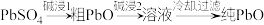 。已知:制备过程中杂质不溶于NaOH溶液,PbO溶解在NaOH溶液中,存在平衡:
。已知:制备过程中杂质不溶于NaOH溶液,PbO溶解在NaOH溶液中,存在平衡: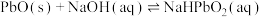 ,溶解度曲线如图所示。下列说法正确的是
,溶解度曲线如图所示。下列说法正确的是