按要求回答下列问题。
(1)为了防止 FeSO4 溶液变质,应在溶液中加入少量的___________ (元素符号表示)。
(2)人体血液中的下列物质不属于电解质的是___________ (填序号,下同)。
a.H2CO3 b.葡萄糖(C6H12O6) c.NaHCO3 d.NaCl
(3)区分 Na2CO3 和 NaHCO3 溶液可选用的方法或试剂是___________ 。
a.CaCl2 溶液 b.焰色试验 c.Ca(OH)2 溶液 d.NaOH 溶液
(4)下列过程必须加入氧化剂才能实现的是___________ 。
a.Cl2→ClO- b.NH3→NH c.KMnO4→MnO2 d.Fe2+→Fe3+
c.KMnO4→MnO2 d.Fe2+→Fe3+
(5)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
①用双线桥法表示电子的转移情况(只需标出电子得失和转移电子总数目)___________ 。
②上面反应中,参加氧化还原反应的硝酸占总硝酸的___________ (用百分数表示)。
(6)已知 16 g A 和 20 g B 恰好完全反应生成 0.04 mol C 和 31.76 g D,则 C 的摩尔质量为___________ 。
(1)为了防止 FeSO4 溶液变质,应在溶液中加入少量的
(2)人体血液中的下列物质不属于电解质的是
a.H2CO3 b.葡萄糖(C6H12O6) c.NaHCO3 d.NaCl
(3)区分 Na2CO3 和 NaHCO3 溶液可选用的方法或试剂是
a.CaCl2 溶液 b.焰色试验 c.Ca(OH)2 溶液 d.NaOH 溶液
(4)下列过程必须加入氧化剂才能实现的是
a.Cl2→ClO- b.NH3→NH
 c.KMnO4→MnO2 d.Fe2+→Fe3+
c.KMnO4→MnO2 d.Fe2+→Fe3+ (5)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
①用双线桥法表示电子的转移情况(只需标出电子得失和转移电子总数目)
②上面反应中,参加氧化还原反应的硝酸占总硝酸的
(6)已知 16 g A 和 20 g B 恰好完全反应生成 0.04 mol C 和 31.76 g D,则 C 的摩尔质量为
更新时间:2021-01-09 18:06:17
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】过氧化钙是一种优良的消毒剂、供氧剂。通常情况下用 在稀氨水中与
在稀氨水中与 反应可得到
反应可得到 沉淀,取实验得到的2.76g
沉淀,取实验得到的2.76g 样品在密闭容器中加热,其受热脱水过程的热重曲线(140℃时完全脱水,杂质受热不分解)如图所示。
样品在密闭容器中加热,其受热脱水过程的热重曲线(140℃时完全脱水,杂质受热不分解)如图所示。

(1)60℃时 中
中
_______ 。
(2)该样品中 的质量分数为
的质量分数为_______ (保留3位有效数字)。
 在稀氨水中与
在稀氨水中与 反应可得到
反应可得到 沉淀,取实验得到的2.76g
沉淀,取实验得到的2.76g 样品在密闭容器中加热,其受热脱水过程的热重曲线(140℃时完全脱水,杂质受热不分解)如图所示。
样品在密闭容器中加热,其受热脱水过程的热重曲线(140℃时完全脱水,杂质受热不分解)如图所示。
(1)60℃时
 中
中
(2)该样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】16gO2与标准状况下_______ LCH4所含原子数相同。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.已知1mol不同气体在不同条件下的体积:
(1)从表中分析得出的结论:
①1mol任何气体,在标准状况下的体积都约为_______ 。
②1mol不同的气体,在不同的条件下,体积_______ (填序号)。
A.一定相等 B.一定不相等 C.不一定相等
(2)理论依据:相同条件下,1mol任何气体的体积几乎相等,原因是①_______ ,②_______ 。
(3)应用:在标准状况下,4g氧气的体积是_______ ;0℃,202kPa时,4g氧气的体积是_______ 。
Ⅱ.在标准状况下15gCO与CO2的混合气体,体积为11.2L。则:
(4)混合气体的密度是_______ g/L。(取小数点后两位)
(5)CO2和CO的体积之比是_______ 。
(6)混合气体中所含碳原子的物质的量是_______ 。
| 化学式 | 条件 | 1mol气体的体积/L |
| H2 | 0℃,101kPa | 22.4 |
| O2 | 22.4 | |
| CO | 22.4 | |
| H2 | 0℃,202kPa | 11.2 |
| CO2 | 11.2 | |
| N2 | 11.2 | |
| NH3 | 273℃,202kPa | 22.4 |
①1mol任何气体,在标准状况下的体积都约为
②1mol不同的气体,在不同的条件下,体积
A.一定相等 B.一定不相等 C.不一定相等
(2)理论依据:相同条件下,1mol任何气体的体积几乎相等,原因是①
(3)应用:在标准状况下,4g氧气的体积是
Ⅱ.在标准状况下15gCO与CO2的混合气体,体积为11.2L。则:
(4)混合气体的密度是
(5)CO2和CO的体积之比是
(6)混合气体中所含碳原子的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.有以下物质:①石墨②铝③酒精④氨水⑤二氧化碳⑥碳酸钠固体⑦氢氧化钡溶液⑧纯醋酸⑨氧化钠固体⑩氯化氢气体⑪熔融氯化钠。
(1)其中能导电的是________ (填序号,下同);属于非电解质的是________ ;属于电解质的是________ 。
(2)写出物质⑥溶于水的电离方程式:__________
(3)写出物质⑥和⑩在水中反应的化学方程式:____________
II.(1)下列叙述正确的是________ 。
A.固体氯化钠不导电,所以氯化钠不是电解质
B.铜丝能导电,所以铜是电解质
C.氯化氢水溶液能导电,所以氯化氢是电解质
D.SO3 溶于水能导电,所以 SO3 是电解质
(2)关于酸、碱、盐的下列各种说法中,正确的是_______ 。
A.化合物电离时,生成的阳离子有氢离子的是酸
B.化合物电离时,生成的阴离子有氢氧根离子的是碱
C.化合物电离时,生成金属阳离子和酸根离子的是盐
D.NH4Cl电离的电离方程式是:NH4Cl=NH4++Cl-,所以NH4Cl不是盐
(1)其中能导电的是
(2)写出物质⑥溶于水的电离方程式:
(3)写出物质⑥和⑩在水中反应的化学方程式:
II.(1)下列叙述正确的是
A.固体氯化钠不导电,所以氯化钠不是电解质
B.铜丝能导电,所以铜是电解质
C.氯化氢水溶液能导电,所以氯化氢是电解质
D.SO3 溶于水能导电,所以 SO3 是电解质
(2)关于酸、碱、盐的下列各种说法中,正确的是
A.化合物电离时,生成的阳离子有氢离子的是酸
B.化合物电离时,生成的阴离子有氢氧根离子的是碱
C.化合物电离时,生成金属阳离子和酸根离子的是盐
D.NH4Cl电离的电离方程式是:NH4Cl=NH4++Cl-,所以NH4Cl不是盐
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有以下八种物质:
①石墨 ②CO2 ③稀盐酸 ④Ba(OH)2溶液
⑤熔融KNO3 ⑥NaHSO4溶液 ⑦CaCO3固体 ⑧酒精(C2H5OH)
(1)以上物质中能导电的是__________________________ (填写编号,下同)
(2)属于电解质的是__________________
(3)属于非电解质的是_______________
(4)写出下列反应的离子方程式:
③与④反应___________________________________________________
③与⑦反应____________________
(5)溶液的导电能力由溶液中自由移动的离子浓度及其所带电荷数决定,向④中缓慢通入②至过量,溶液的导电能力的变化为_____________
A.先慢慢增强后又逐渐减弱
B.不变
C.先慢慢减弱后又逐渐增强
①石墨 ②CO2 ③稀盐酸 ④Ba(OH)2溶液
⑤熔融KNO3 ⑥NaHSO4溶液 ⑦CaCO3固体 ⑧酒精(C2H5OH)
(1)以上物质中能导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)写出下列反应的离子方程式:
③与④反应
③与⑦反应
(5)溶液的导电能力由溶液中自由移动的离子浓度及其所带电荷数决定,向④中缓慢通入②至过量,溶液的导电能力的变化为
A.先慢慢增强后又逐渐减弱
B.不变
C.先慢慢减弱后又逐渐增强
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】生活中常见的离子反应
(1)“胃舒平”消耗胃酸过多时发生反应的离子反应为:______ 。
(2)硬水形成所发生的主要反应为:______ ;______ 。
(3)加热使硬水软化所发生的离子反应为______ ;______ 。
(4)在硬水中加入Na2CO3等沉淀剂软化硬水的______ ;______ 。
(1)“胃舒平”消耗胃酸过多时发生反应的离子反应为:
(2)硬水形成所发生的主要反应为:
(3)加热使硬水软化所发生的离子反应为
(4)在硬水中加入Na2CO3等沉淀剂软化硬水的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】纯净的过氧化钙(CaO2)是白色的粉末,难溶于水,不溶于乙醇、乙醚,常温下较为稳定,是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室可用钙盐制取CaO2·8H2O,再经脱水制得CaO2。CaO2·8H2O在0℃时稳定,在室温时经过几天就分解,加热至130℃时逐渐变为无水CaO2。
其制备过程如下:
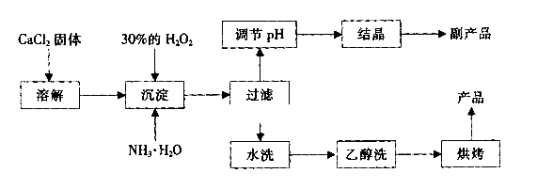
(1)用化学方程式表示出过氧化钙用做水产养殖增氧剂的原理:_______________ 。
(2)为了控制沉淀温度为0℃左右,在实验室宜采取的方法是__________________ 。
(3)该制法的副产品为___________ (填化学式),为了提高副产品的产率,结晶前要将溶液的pH调整到合适范围,可加入下列试剂中的____________ (填写A或B)。
A.盐酸 B.氨水
(4)为了检验“水洗”是否合格,可取少量洗涤液于试管中,再滴加__________ 进行检查。
(5)测定产品中CaO2的含量的实验步骤是:
第一步,准确称取ag产品于有塞锥形瓶中,加入适量蒸馏水和过量的bgKI晶体,再滴入少量2 mol·L—1的H2SO4溶液,充分反应。
第二步,向上述锥形瓶中加入几滴淀粉溶液。
第三步,逐滴加入浓度为c mol/L的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液VmL。 (已知:I2+2S2O32-=2I-+S4O62-(无色))
①第三步中说明反应恰好完全的现象是___________________________________ ;
②CaO2的质量分数为______________________________________ (用字母表示)
其制备过程如下:

(1)用化学方程式表示出过氧化钙用做水产养殖增氧剂的原理:
(2)为了控制沉淀温度为0℃左右,在实验室宜采取的方法是
(3)该制法的副产品为
A.盐酸 B.氨水
(4)为了检验“水洗”是否合格,可取少量洗涤液于试管中,再滴加
(5)测定产品中CaO2的含量的实验步骤是:
第一步,准确称取ag产品于有塞锥形瓶中,加入适量蒸馏水和过量的bgKI晶体,再滴入少量2 mol·L—1的H2SO4溶液,充分反应。
第二步,向上述锥形瓶中加入几滴淀粉溶液。
第三步,逐滴加入浓度为c mol/L的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液VmL。 (已知:I2+2S2O32-=2I-+S4O62-(无色))
①第三步中说明反应恰好完全的现象是
②CaO2的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.写出下列反应的离子方程式
(1)用稀硫酸清洗铁锈(Fe2O3)_____________ 。
(2)硫酸铜溶液和氢氧化钡溶液混合________ 。
(3)向足量澄清石灰水中通入二氧化碳__________ 。
II.根据下列离子方程式,各写一个符合条件的化学方程式
(4)Mg+2H+==Mg2++H2↑__________ 。
(5) +2H+==CO2↑+H2O
+2H+==CO2↑+H2O__________ 。
(1)用稀硫酸清洗铁锈(Fe2O3)
(2)硫酸铜溶液和氢氧化钡溶液混合
(3)向足量澄清石灰水中通入二氧化碳
II.根据下列离子方程式,各写一个符合条件的化学方程式
(4)Mg+2H+==Mg2++H2↑
(5)
 +2H+==CO2↑+H2O
+2H+==CO2↑+H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请用双线桥法或单线桥法分析该反应中电子转移的方向和数目:
(1)实验室制取氯气的化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。单线桥标出该反应电子转移的方向和数目:
MnCl2+Cl2↑+2H2O。单线桥标出该反应电子转移的方向和数目:_____ 。反应中氧化剂与还原剂的个数比是_____ 。
(2)写出Fe2O3与CO在高温下反应的化学方程式,并用线桥标出电子转移的方向和数目_____ 。
(3)NaHSO4溶液中滴加Ba(OH)2溶液,是 恰好完全沉淀,写出该反应的离子方程式:
恰好完全沉淀,写出该反应的离子方程式:_____ ,此时溶液呈_____ 性(填“酸性、中性或碱性”)
(4)向NaHCO3溶液中加入Ca(OH)2至过量,写出该反应的离子方程式:_____ 。
(1)实验室制取氯气的化学方程式为:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O。单线桥标出该反应电子转移的方向和数目:
MnCl2+Cl2↑+2H2O。单线桥标出该反应电子转移的方向和数目:(2)写出Fe2O3与CO在高温下反应的化学方程式,并用线桥标出电子转移的方向和数目
(3)NaHSO4溶液中滴加Ba(OH)2溶液,是
 恰好完全沉淀,写出该反应的离子方程式:
恰好完全沉淀,写出该反应的离子方程式:(4)向NaHCO3溶液中加入Ca(OH)2至过量,写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空。
(1)配平氧化还原离子方程式:_____Cu+______ +_____
+_____ =_____NO↑+_____
=_____NO↑+_____ +_____
+_____
___________
(2)已知 与浓盐酸室温下可发生如下反应:
与浓盐酸室温下可发生如下反应: 
①用“双线桥法”标出上述反应的电子转移情况___________ 。
②此反应体现HCl的___________ 性和___________ 性,氧化物是___________ ,生成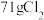 时消耗的还原剂的质量为
时消耗的还原剂的质量为___________ g。
③若分别用① (还原产物是
(还原产物是 );②
);②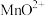 (还原产物是
(还原产物是 );③
);③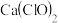 (还原产物是
(还原产物是 )氧化浓盐酸制备氯气,当浓盐酸足量且消耗这三种氧化剂的数目相同时,生成氯气分子的数目之比是
)氧化浓盐酸制备氯气,当浓盐酸足量且消耗这三种氧化剂的数目相同时,生成氯气分子的数目之比是___________ 。
(3)油画所用颜料含有某种白色铅化合物,置于空气中天长日久就会变成黑色,从而使油画色彩变暗。若用 来“清洗”,则可将PbS转变成白色的
来“清洗”,则可将PbS转变成白色的 ,从而使油画的色彩“复原”。上述“清洗”反应的化学方程式为
,从而使油画的色彩“复原”。上述“清洗”反应的化学方程式为___________ ,此反应中 为
为___________ 剂。
(1)配平氧化还原离子方程式:_____Cu+______
 +_____
+_____ =_____NO↑+_____
=_____NO↑+_____ +_____
+_____
(2)已知
 与浓盐酸室温下可发生如下反应:
与浓盐酸室温下可发生如下反应: 
①用“双线桥法”标出上述反应的电子转移情况
②此反应体现HCl的
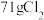 时消耗的还原剂的质量为
时消耗的还原剂的质量为③若分别用①
 (还原产物是
(还原产物是 );②
);②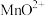 (还原产物是
(还原产物是 );③
);③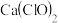 (还原产物是
(还原产物是 )氧化浓盐酸制备氯气,当浓盐酸足量且消耗这三种氧化剂的数目相同时,生成氯气分子的数目之比是
)氧化浓盐酸制备氯气,当浓盐酸足量且消耗这三种氧化剂的数目相同时,生成氯气分子的数目之比是(3)油画所用颜料含有某种白色铅化合物,置于空气中天长日久就会变成黑色,从而使油画色彩变暗。若用
 来“清洗”,则可将PbS转变成白色的
来“清洗”,则可将PbS转变成白色的 ,从而使油画的色彩“复原”。上述“清洗”反应的化学方程式为
,从而使油画的色彩“复原”。上述“清洗”反应的化学方程式为 为
为
您最近一年使用:0次
【推荐3】氧化还原反应在生产生活中应用十分广泛,回答下列问题:
(1)在S2-、Fe2+、Mg2+、I-、H+、S粒子中,只有氧化性的是__ ,只有还原性的是__ ,既有氧化性又有还原性的是__ 。
(2)有下列三个在溶液中发生的氧化还原反应:
Ⅰ.2FeCl3+2KI=2FeCl2+2KCl+I2;
Ⅱ.2FeCl2+Cl2=2FeCl3;
Ⅲ.K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑,则
①FeCl3、I2、Cl2、K2Cr2O7的氧化性由强到弱依次是__ 。
②Cr2O 、I-在强酸性溶液中能否大量共存?
、I-在强酸性溶液中能否大量共存?___ (请先回答“能”或“否”,“能”不用解释,“否”需要加以解释)。
(3)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为3Cl2+8NH3=6NH4Cl+N2,该反应中氧化剂为__ (填化学式),标准状况下,每生成2.24LN2,反应中转移的电子的物质的量为__ mol。
(4)Mn2+、Bi3+、BiO 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程,将以上物质组成一个正确的离子方程式,并用单线桥标出电子转移方向和数目:
→Bi3+的反应过程,将以上物质组成一个正确的离子方程式,并用单线桥标出电子转移方向和数目:__ 。
(1)在S2-、Fe2+、Mg2+、I-、H+、S粒子中,只有氧化性的是
(2)有下列三个在溶液中发生的氧化还原反应:
Ⅰ.2FeCl3+2KI=2FeCl2+2KCl+I2;
Ⅱ.2FeCl2+Cl2=2FeCl3;
Ⅲ.K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑,则
①FeCl3、I2、Cl2、K2Cr2O7的氧化性由强到弱依次是
②Cr2O
 、I-在强酸性溶液中能否大量共存?
、I-在强酸性溶液中能否大量共存?(3)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为3Cl2+8NH3=6NH4Cl+N2,该反应中氧化剂为
(4)Mn2+、Bi3+、BiO
 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程,将以上物质组成一个正确的离子方程式,并用单线桥标出电子转移方向和数目:
→Bi3+的反应过程,将以上物质组成一个正确的离子方程式,并用单线桥标出电子转移方向和数目:
您最近一年使用:0次

 NaOH
NaOH  NH3·H2O
NH3·H2O

