中国传统的农具、兵器曾大量使用铁,铁器的修复是文物保护的重要课题。

(1)分析腐蚀原理
一般认为,铁器腐蚀经过了如下循环:
①Fe转化为 ;
;
② 在自然环境中形成
在自然环境中形成 ,该物质中铁元素的化合价为
,该物质中铁元素的化合价为_______ ,
③ 和
和 反应形成致密的
反应形成致密的 保护层;
保护层;
④ 保护层被氧化为
保护层被氧化为 ,如此往复。写出
,如此往复。写出 保护层被氧化为
保护层被氧化为 反应的化学方程式
反应的化学方程式_______ 。
(2)铁器表面氧化层的成分有多种,性质如下:
在有氧条件下, 在含
在含 溶液中会转化为FeOCl,将相关反应的离子方程式补充完整:
溶液中会转化为FeOCl,将相关反应的离子方程式补充完整:_______
4Fe3O4+O2+ _______+
_______+ H2O=
H2O= FeOCl+
FeOCl+ _______。
_______。
(3)化学修复可以使FeOCl转化为 致密保护层:用Na2SO3和NaOH混合溶液浸泡锈蚀的铁器,一段时间后取出,再用NaOH溶液反复洗涤。
致密保护层:用Na2SO3和NaOH混合溶液浸泡锈蚀的铁器,一段时间后取出,再用NaOH溶液反复洗涤。
①FeOCl在NaOH的作用下转变为不溶于水的 ,反应的离子方程式是
,反应的离子方程式是_______ 。
②Na2SO3的作用是_______ 。
(4)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前,模具必须进行_______ ,不得留有水。原因是_______ (用化学方程式表示)。

(1)分析腐蚀原理
一般认为,铁器腐蚀经过了如下循环:
①Fe转化为
 ;
;②
 在自然环境中形成
在自然环境中形成 ,该物质中铁元素的化合价为
,该物质中铁元素的化合价为③
 和
和 反应形成致密的
反应形成致密的 保护层;
保护层;④
 保护层被氧化为
保护层被氧化为 ,如此往复。写出
,如此往复。写出 保护层被氧化为
保护层被氧化为 反应的化学方程式
反应的化学方程式(2)铁器表面氧化层的成分有多种,性质如下:
| 成分 |  |  | FeOCl | |
| 性质 | 致密 | 疏松 | 疏松 |
在有氧条件下,
 在含
在含 溶液中会转化为FeOCl,将相关反应的离子方程式补充完整:
溶液中会转化为FeOCl,将相关反应的离子方程式补充完整:4Fe3O4+O2+
 _______+
_______+ H2O=
H2O= FeOCl+
FeOCl+ _______。
_______。(3)化学修复可以使FeOCl转化为
 致密保护层:用Na2SO3和NaOH混合溶液浸泡锈蚀的铁器,一段时间后取出,再用NaOH溶液反复洗涤。
致密保护层:用Na2SO3和NaOH混合溶液浸泡锈蚀的铁器,一段时间后取出,再用NaOH溶液反复洗涤。①FeOCl在NaOH的作用下转变为不溶于水的
 ,反应的离子方程式是
,反应的离子方程式是②Na2SO3的作用是
(4)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前,模具必须进行
更新时间:2021-01-27 22:57:29
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】在 胶体中,逐滴加入
胶体中,逐滴加入 稀溶液,会出现一系列变化。
稀溶液,会出现一系列变化。
(1)先出现红褐色沉淀,原因是_____ 。
(2)随后沉淀溶解,溶液呈黄色,写出此反应的离子方程式_____ 。
(3)最后溶液颜色加深,原因是_____ ,此反应的离子方程式是_____ 。
(4)若用稀盐酸代替 稀溶液,能出现上述哪些相同的变化现象?
稀溶液,能出现上述哪些相同的变化现象?_____ 。(写序号)
 胶体中,逐滴加入
胶体中,逐滴加入 稀溶液,会出现一系列变化。
稀溶液,会出现一系列变化。(1)先出现红褐色沉淀,原因是
(2)随后沉淀溶解,溶液呈黄色,写出此反应的离子方程式
(3)最后溶液颜色加深,原因是
(4)若用稀盐酸代替
 稀溶液,能出现上述哪些相同的变化现象?
稀溶液,能出现上述哪些相同的变化现象?
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某无色透明溶液中可能存在大量Cl-、Mg2+、Fe3+、K+、Cu2+中的一种或几种,请回答下列问题:
(1)不用做任何实验就可以肯定溶液中不存在的离子是______ 。
(2)取少量原溶液,加入过量硝酸银溶液,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是______ ,反应的离子方程式为______ 。
(3)取少量原溶液,向其中加入过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是______ ,生成沉淀的离子方程式为______ 。
(4)检验原溶液中可能存在的阳离子的实验方法(写出实验操作、现象及结论)______ ,原溶液中还可能大量存在的阴离子是______ (填字母)。
A.SO B.NO
B.NO C.CO
C.CO D.OH-
D.OH-
(1)不用做任何实验就可以肯定溶液中不存在的离子是
(2)取少量原溶液,加入过量硝酸银溶液,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取少量原溶液,向其中加入过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是
(4)检验原溶液中可能存在的阳离子的实验方法(写出实验操作、现象及结论)
A.SO
 B.NO
B.NO C.CO
C.CO D.OH-
D.OH-
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。_______ (填字母序号)。
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为_______ 。
(3)硝化过程中,含氮物质发生_______ (填“氧化”或“还原”)反应。
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02 mol 氮气时,转移的电子的物质的量为_______ mol。
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:将2L气样通入适量酸化的H2O2溶液中,使NO完全被氧化为 。向上述反应后溶液中加入30 mL0.1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与3.5 mL、0.1 mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为
。向上述反应后溶液中加入30 mL0.1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与3.5 mL、0.1 mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为 的离子方程式是
的离子方程式是______ 。上述过程中发生下列反应:3Fe2++ +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O; + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。则气样中NO的含量为
+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。则气样中NO的含量为_______ mg /L。(保留计算过程)
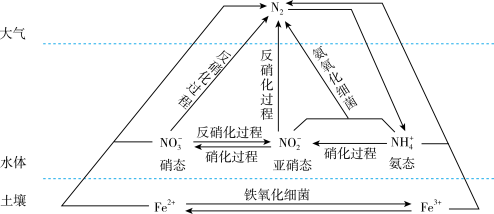
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
(3)硝化过程中,含氮物质发生
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02 mol 氮气时,转移的电子的物质的量为
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:将2L气样通入适量酸化的H2O2溶液中,使NO完全被氧化为
 。向上述反应后溶液中加入30 mL0.1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与3.5 mL、0.1 mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为
。向上述反应后溶液中加入30 mL0.1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与3.5 mL、0.1 mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为 的离子方程式是
的离子方程式是 +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O; + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。则气样中NO的含量为
+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。则气样中NO的含量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】Ⅰ.下列物质能导电的是___________ ,属于电解质的是___________ ,属于非电解质的是___________ 。(填序号)
①铜 ②烧碱溶液 ③BaSO4固体 ④氯化钠晶体 ⑤盐酸 ⑥干冰 ⑦蔗糖
Ⅱ.在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应中,___________ 是氧化剂;___________ 是还原剂;___________ 是氧化产物;___________ 是还原产物。
①铜 ②烧碱溶液 ③BaSO4固体 ④氯化钠晶体 ⑤盐酸 ⑥干冰 ⑦蔗糖
Ⅱ.在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应中,
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】完成下列反应的化学方程式,并指明其中的氧化剂和还原剂。
(1)

__________ 、氧化剂__________ 、还原剂__________ 。
(2)
__________ 、氧化剂__________ 、还原剂__________ 。
(3)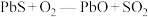
__________ 、氧化剂__________ 、还原剂__________ 。
(4)
__________ 、氧化剂__________ 、还原剂__________ 。
(1)


(2)

(3)
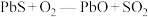
(4)

您最近一年使用:0次
【推荐3】如下图在衬白纸的玻璃片中央放置适量的KMnO4颗粒,在周围分别滴加一滴含有酚酞的澄清石灰水、FeCl2溶液,然后在KMnO4晶体上滴加适量的浓盐酸,迅速盖好表面皿。提示:实验室中所用的少量氯气可以用下述原理制取:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,此反应在常温下即能进行。
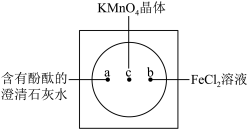
(1)氧化剂与还原剂物质的量之比为____________ ,氧化产物为_______ 。
(2)产生0.1molCl2,则转移电子的物质的量为______ mol。
(3)b处离子方程式是___________ 。
(4)高锰酸钾标准溶液经常用来滴定测量物质的含量。配平并完成下列高锰酸钾滴定草酸反应的离子方程式:_____  +
+______ H2C2O4+______  =
=____  +
+_____ CO2↑+___________

(1)氧化剂与还原剂物质的量之比为
(2)产生0.1molCl2,则转移电子的物质的量为
(3)b处离子方程式是
(4)高锰酸钾标准溶液经常用来滴定测量物质的含量。配平并完成下列高锰酸钾滴定草酸反应的离子方程式:
 +
+ =
= +
+
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】化学上用分类法学习化学物质的共性,用比较法学习化学物质的特性,物质的氧化性与还原性尤为重要。回答下列问题:
(1)磷元素的含氧酸有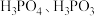 (亚磷酸)、
(亚磷酸)、 (次磷酸)等多种,其中已知:
(次磷酸)等多种,其中已知:
 (过量)
(过量)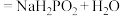 。
。 属于
属于_______ (填“一”、“二”或“三”)元酸。 属于
属于_______ (填“正盐”或“酸式盐”)。
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式,并用单线桥表示电子转移的方向和数目:______

(3)某种钇矿石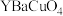 (其中化合价分别为
(其中化合价分别为 )溶于稀盐酸不产生污染,其中
)溶于稀盐酸不产生污染,其中 的价态不变,
的价态不变,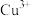 全部被还原为
全部被还原为 ,写出该反应的离子方程式
,写出该反应的离子方程式_______ 。
(4) (B为+3价)、
(B为+3价)、 与相同氧化剂反应时,
与相同氧化剂反应时,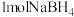 的还原能力相当于
的还原能力相当于_______  的还原能力(B元素化合价不变,氧化产物中氢元素化合价相同)。
的还原能力(B元素化合价不变,氧化产物中氢元素化合价相同)。
(5)已知酸性 ,少量
,少量 与
与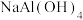 反应的离子方程式为
反应的离子方程式为_______ ,漂白液在空气中放置一段时间后漂白效果更佳的原理的离子方程式为_______ 。
(1)磷元素的含氧酸有
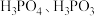 (亚磷酸)、
(亚磷酸)、 (次磷酸)等多种,其中已知:
(次磷酸)等多种,其中已知: (过量)
(过量)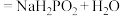 。
。 属于
属于 属于
属于(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式,并用单线桥表示电子转移的方向和数目:

(3)某种钇矿石
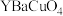 (其中化合价分别为
(其中化合价分别为 )溶于稀盐酸不产生污染,其中
)溶于稀盐酸不产生污染,其中 的价态不变,
的价态不变,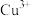 全部被还原为
全部被还原为 ,写出该反应的离子方程式
,写出该反应的离子方程式(4)
 (B为+3价)、
(B为+3价)、 与相同氧化剂反应时,
与相同氧化剂反应时,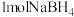 的还原能力相当于
的还原能力相当于 的还原能力(B元素化合价不变,氧化产物中氢元素化合价相同)。
的还原能力(B元素化合价不变,氧化产物中氢元素化合价相同)。(5)已知酸性
 ,少量
,少量 与
与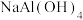 反应的离子方程式为
反应的离子方程式为
您最近一年使用:0次
【推荐2】回答下列问题:
(1)中国古代著作中有“银针验毒”的记录,其原理为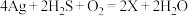 ,则X的化学式是
,则X的化学式是_______ ,其中 在该反应中
在该反应中_______ (填标号)。
A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(2)按如图所示操作,充分反应后:
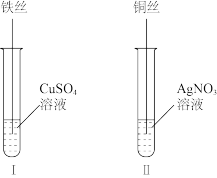
①Ⅱ中铜丝上观察到的现象是_______ 。
②结合Ⅰ、Ⅱ实验现象可知 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______ 。
(3)已知 可发生反应:
可发生反应: 。
。
①该反应中被还原的元素是_______ (填化学式,下同),氧化产物是_______ 。
②某温度下,将 通入
通入 溶液中,反应后得到
溶液中,反应后得到 、
、 、
、 的混合溶液,经测定
的混合溶液,经测定 与
与 的数目之比为1:2,该反应的化学反应方程式为
的数目之比为1:2,该反应的化学反应方程式为_______ 。
(1)中国古代著作中有“银针验毒”的记录,其原理为
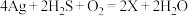 ,则X的化学式是
,则X的化学式是 在该反应中
在该反应中A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(2)按如图所示操作,充分反应后:

①Ⅱ中铜丝上观察到的现象是
②结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(3)已知
 可发生反应:
可发生反应: 。
。①该反应中被还原的元素是
②某温度下,将
 通入
通入 溶液中,反应后得到
溶液中,反应后得到 、
、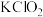 、
、 的混合溶液,经测定
的混合溶液,经测定 与
与 的数目之比为1:2,该反应的化学反应方程式为
的数目之比为1:2,该反应的化学反应方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】金属和非金属在人类生产生活中得到了广泛应用,请你回答下列问题。
(1)面包发酵粉的主要成分之一是一种钠盐,其俗称为________ ;漂白粉的有效成分为__________ (写化学式);FeCl3常用作净水剂,其原理为_________ (用离子方程式表示)。
(2)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是_________ 。
(3)人体血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化Fe3+而中毒,服用维生素C可以解毒.对上述的分析正确的是____________
A.亚硝酸盐是还原剂B.维生素C是氧化剂
C.维生素C被氧化D.亚硝酸盐发生氧化反应
(1)面包发酵粉的主要成分之一是一种钠盐,其俗称为
(2)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是
(3)人体血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化Fe3+而中毒,服用维生素C可以解毒.对上述的分析正确的是
A.亚硝酸盐是还原剂B.维生素C是氧化剂
C.维生素C被氧化D.亚硝酸盐发生氧化反应
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)鉴别NaCl溶液和KCl溶液的实验方法是______ 。
(2)铁与水蒸气反应的方程式为______ 。
(3)除去CO2中混有的HCl气体所用试剂为______ 。
(2)铁与水蒸气反应的方程式为
(3)除去CO2中混有的HCl气体所用试剂为
您最近一年使用:0次

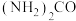 水溶液吸收
水溶液吸收 ,吸收过程中存在
,吸收过程中存在 与
与 和
和 的反应。写出该反应的化学方程式:
的反应。写出该反应的化学方程式: 与
与 生成
生成

