(1)用酸性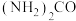 水溶液吸收
水溶液吸收 ,吸收过程中存在
,吸收过程中存在 与
与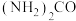 生
生 和
和 的反应。写出该反应的化学方程式:
的反应。写出该反应的化学方程式:________ 。
(2)在有氧条件下,新型催化剂M能催化 与
与 反应生成
反应生成 。
。 与
与 生成
生成 的反应中,当生成1mol
的反应中,当生成1mol  时,转移的电子为
时,转移的电子为______ mol。
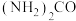 水溶液吸收
水溶液吸收 ,吸收过程中存在
,吸收过程中存在 与
与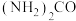 生
生 和
和 的反应。写出该反应的化学方程式:
的反应。写出该反应的化学方程式:(2)在有氧条件下,新型催化剂M能催化
 与
与 反应生成
反应生成 。
。 与
与 生成
生成 的反应中,当生成1mol
的反应中,当生成1mol  时,转移的电子为
时,转移的电子为
更新时间:2020/09/17 14:27:15
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】Na2FeO4 的制备方法有次氯酸盐氧化法(湿法):该法是在碱性条件下,利用可溶性次氯酸盐氧化氢氧化铁,试写出并配平这一离子方程式_____________ ,每生成 1molNa2FeO4,转移的电子数目是___________ 。
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似,有咸味,容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似,有咸味,容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:_______
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:_______ _______KI+_______=_______
_______KI+_______=_______ _______
_______ _______
_______ _______
_______ _______
_______
(1)请完成该化学方程式并配平_______ 。
(2)上述反应的还原剂为_______ ,氧化产物与还原产物的个数比为_______ 。
(3)写出 与
与 反应的离子方程式:
反应的离子方程式:_______ 。
(4)误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列_______(填字母)反应中
表现出的性质与下列_______(填字母)反应中 表现出的性质相同。
表现出的性质相同。
(5)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:_______ 。
 )是一种用途广泛的工业盐,因其外观和食盐相似,有咸味,容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似,有咸味,容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:_______
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:_______ _______KI+_______=_______
_______KI+_______=_______ _______
_______ _______
_______ _______
_______ _______
_______
(1)请完成该化学方程式并配平
(2)上述反应的还原剂为
(3)写出
 与
与 反应的离子方程式:
反应的离子方程式:(4)误食
 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列_______(填字母)反应中
表现出的性质与下列_______(填字母)反应中 表现出的性质相同。
表现出的性质相同。A. |
B. |
C.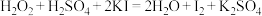 |
D.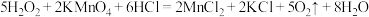 |
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】金属元素锡(Sn)和碳元素位于同一主族,主要化合价为+2和+4。某同学通过下列方法测定金属锡样品的纯度:(假定杂质不参加反应)
(1)将试样溶于盐酸中,反应的化学方程式为:______________________ 。
(2)加入过量的FeCl3溶液,反应的化学方程式为:______________________ 。
(3)用已知浓度的K2Cr2O7酸性溶液滴定生成的Fe2+.反应的离子方程式为:______________
(4)现有金属锡样品1.142g,经上述各步反应后,共用去0.100mol/L的K2Cr2O7溶液16.00ml. 则试样中锡的质量分数_____________________ 。
(5)步骤(4)中如果取用16.00ml的K2Cr2O7溶液则应用____________ (填仪器名称)。该同学在配制0.100mol/L 的K2Cr2O7溶液的试验中,若其他步骤都正确,但定容时俯视刻度线则所得溶液的浓度____________ (填偏高,偏低,或无影响)。
(1)将试样溶于盐酸中,反应的化学方程式为:
(2)加入过量的FeCl3溶液,反应的化学方程式为:
(3)用已知浓度的K2Cr2O7酸性溶液滴定生成的Fe2+.反应的离子方程式为:
(4)现有金属锡样品1.142g,经上述各步反应后,共用去0.100mol/L的K2Cr2O7溶液16.00ml. 则试样中锡的质量分数
(5)步骤(4)中如果取用16.00ml的K2Cr2O7溶液则应用
您最近半年使用:0次
【推荐1】人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力。
(1)反应过程中Fe2+发生___ 反应,说明亚硝酸钠具有___ 性;误食亚硝酸钠中毒,可服维生素C缓解,通过发生氧化还原反应解毒,说明维生素C具有___ 性。
(2)FeCl2易在酸性溶液(含HCl)中与H2O2溶液反应生成FeCl3,该反应的化学反应方程式为:___ ,发生反应的H2O2分子与转移的电子数之比为___ 。
(3)Fe3+对H2O2的分解也有催化作用,若分别用高锰酸钾和H2O2制得等质量氧气,反应过程中转移的电子数之比为___ 。
(1)反应过程中Fe2+发生
(2)FeCl2易在酸性溶液(含HCl)中与H2O2溶液反应生成FeCl3,该反应的化学反应方程式为:
(3)Fe3+对H2O2的分解也有催化作用,若分别用高锰酸钾和H2O2制得等质量氧气,反应过程中转移的电子数之比为
您最近半年使用:0次
【推荐2】为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应:2NO+2CO N2+2CO2。
N2+2CO2。
(1)作还原剂的物质是_______ 。氮元素的化合价_______ (填“升高”或“降低”)。
(2)若反应中消耗了2molNO,则生成N2的物质的量为_______ mol,转移电子的物质的量为_______ mol。
 N2+2CO2。
N2+2CO2。(1)作还原剂的物质是
(2)若反应中消耗了2molNO,则生成N2的物质的量为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】Ⅰ、下表是某地市场上销售的一种“加碘盐”包装上的部分文字说明。
回答下列问题:
(1)结合物质分类中的树状分类法的有关知识,根据物质的组成对物质进行分类。在下列五种___________ (填“混合物”“化合物”“盐”或“氧化物”)中与碘酸钾( )属于同类物质的是
)属于同类物质的是___________ (填序号)。③和④反应生成碘酸钾,请写出化学反应方程式___________ 。
① ②
② ③
③ ④
④ ⑤
⑤
(2)推测碘酸钾( )的物理性质:碘酸钾(
)的物理性质:碘酸钾( )
)___________ (填“能”或“不能”)溶于水;化学性质:碘酸钾( )在受热时
)在受热时___________ (填“易分解”或“不易分解”)。
Ⅱ、
(3) 属于非强酸形成的酸式盐,已知
属于非强酸形成的酸式盐,已知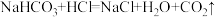 、
、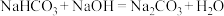 ,将上述两个化学反应方程式改写成离子方程式
,将上述两个化学反应方程式改写成离子方程式___________ 、___________ 。
Ⅲ、
(4)化学反应方程式 中还原剂是
中还原剂是___________ ,氧化剂和还原剂的质量比为___________ ,若反应中生成的 个数为12,则反应中转移的电子数为
个数为12,则反应中转移的电子数为___________ 。
Ⅳ、
(5)针对以下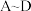 四个涉及
四个涉及 的反应填空:
的反应填空:
A.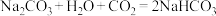 B.
B. C.
C.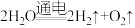 D.
D.
 仅作氧化剂的反应是
仅作氧化剂的反应是___________ (填序号,下同), 仅作还原剂的反应是
仅作还原剂的反应是___________ , 既作氧化剂又作还原剂的反应是
既作氧化剂又作还原剂的反应是___________ , 既不作氧化剂又不作还原剂的反应是
既不作氧化剂又不作还原剂的反应是___________ 。
回答下列问题:
| 配料表 | 精制海盐、碘酸钾( ) ) |
| 含碘量 | 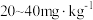 |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时待食品熟后加入碘盐 |
 )属于同类物质的是
)属于同类物质的是①
 ②
② ③
③ ④
④ ⑤
⑤
(2)推测碘酸钾(
 )的物理性质:碘酸钾(
)的物理性质:碘酸钾( )
) )在受热时
)在受热时Ⅱ、
(3)
 属于非强酸形成的酸式盐,已知
属于非强酸形成的酸式盐,已知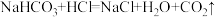 、
、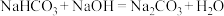 ,将上述两个化学反应方程式改写成离子方程式
,将上述两个化学反应方程式改写成离子方程式Ⅲ、
(4)化学反应方程式
 中还原剂是
中还原剂是 个数为12,则反应中转移的电子数为
个数为12,则反应中转移的电子数为Ⅳ、
(5)针对以下
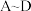 四个涉及
四个涉及 的反应填空:
的反应填空:A.
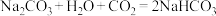 B.
B. C.
C.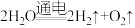 D.
D.
 仅作氧化剂的反应是
仅作氧化剂的反应是 仅作还原剂的反应是
仅作还原剂的反应是 既作氧化剂又作还原剂的反应是
既作氧化剂又作还原剂的反应是 既不作氧化剂又不作还原剂的反应是
既不作氧化剂又不作还原剂的反应是
您最近半年使用:0次



