已知A、B、C、D、E都是短周期的主族元素,原子序数依次增大,其中A是空气中含量最多的元素,C是短周期中原子半径最大的元素,C与B可形成C2B和C2B2两种物质,E是地壳中含量最多的金属元素。请回答下列问题:
(1)①A在元素周期表中的位置_______ 。
②上述元素的最高价氧化物对应的水化物中碱性最强的是_______ (填化学式)。
③写出C2B2的电子式_______ 。
(2)C、D、E三种元素对应的简单离子的半径由大到小的顺序是_______ (填离子符号)。
(3)写出单质E与 溶液反应的离子方程式
溶液反应的离子方程式_______ 。
(1)①A在元素周期表中的位置
②上述元素的最高价氧化物对应的水化物中碱性最强的是
③写出C2B2的电子式
(2)C、D、E三种元素对应的简单离子的半径由大到小的顺序是
(3)写出单质E与
 溶液反应的离子方程式
溶液反应的离子方程式
20-21高一上·广东梅州·期末 查看更多[3]
(已下线)第1章 物质结构 元素周期律(基础过关卷)-2020-2021学年高一化学必修2章末集训必刷卷(人教版)(已下线)专题07 物质结构与元素周期律-备战2021届高考化学二轮复习题型专练广东省梅州市2020-2021学年高一上学期期末考试化学试题
更新时间:2021-01-31 19:44:23
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】U、W、X、Y、Z都是短周期元素,且原子序数依次增大。其中U与W可形成三角锥形分子A,U与X可形成常温下呈液态的分子B,A、B均为10电子分子;Y元素原子的K层电子数与M层电子数相同;Z元素的单质、氧化物均为原子晶体。请回答下列问题:
(1)Z元素在周期表中的位置_______________ 。W、X、Y、Z四种元素的原子半径由小到大的顺序是___________________ (用元素符号表示)。
(2)用电子式表示U与X形成的18电子化合物的形成过程____________________ 。
(3)ZX2与NaOH溶液反应的离子方程式___________________ 。
(4)一定量的Y单质在足量二氧化碳中充分燃烧的化学方程式是______________ ,将生成的全部固体与足量的热浓硝酸混合,充分反应后,产物中二氧化碳和二氧化氮共aL(标准状况),则 Y 单质的质量是______________________ g(用含a的代数式表示)。
(1)Z元素在周期表中的位置
(2)用电子式表示U与X形成的18电子化合物的形成过程
(3)ZX2与NaOH溶液反应的离子方程式
(4)一定量的Y单质在足量二氧化碳中充分燃烧的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空。
(1)前20号元素中气态氢化物最稳定的是:_____ (填化学式)。
(2)前20号元素中最高价氧化物对应水化物碱性最强的碱为:_____ (填写名称)。
(3)第Ⅵ A族元素所形成的氢化物中沸点最高的是:____ (填化学式)。
(4)短周期主族元素中原子半径最大的元素是:_____ (填写名称)。
(5)Fe在元素周期表中位置为:______ 。
(6)以下晶体,存在分子间作用力的共价化合物是_______ (填序号)。
①Ne晶体 ②NH4Cl晶体 ③CaCl2晶体 ④干冰 ⑤水晶
(7)下列能说明氯元素原子得电子能力比硫元素原子得电子能力强的是_______ (填序号)。
① HCl的溶解度比H2S的大
② HCl的酸性比H2S的强
③ HCl的稳定性比H2S的强
④ Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
⑤ HClO4的酸性比H2SO4的强
⑥ Cl2能与H2S反应生成S
(1)前20号元素中气态氢化物最稳定的是:
(2)前20号元素中最高价氧化物对应水化物碱性最强的碱为:
(3)第Ⅵ A族元素所形成的氢化物中沸点最高的是:
(4)短周期主族元素中原子半径最大的元素是:
(5)Fe在元素周期表中位置为:
(6)以下晶体,存在分子间作用力的共价化合物是
①Ne晶体 ②NH4Cl晶体 ③CaCl2晶体 ④干冰 ⑤水晶
(7)下列能说明氯元素原子得电子能力比硫元素原子得电子能力强的是
① HCl的溶解度比H2S的大
② HCl的酸性比H2S的强
③ HCl的稳定性比H2S的强
④ Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
⑤ HClO4的酸性比H2SO4的强
⑥ Cl2能与H2S反应生成S
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,回答下列问题:
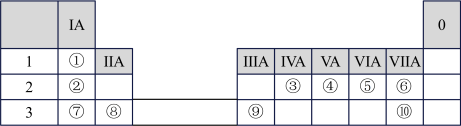
(1)自然界中,组成物质最多的元素在周期表中的位置是___________ 。上述元素中最高价氧化物对应的水化物碱性最强的是___________ (填化学式)。
(2)写出由①④⑩三种元素形成的一种盐的电子式___________ 。⑤⑦形成A2B2型化合物中所含的化学键类型为___________ 。
(3)⑥⑦⑨的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(4)根据对角线元素性质相似规则,写出②的最高价氧化物对应的水化物与稀硫酸反应的离子方程式:___________ 。
(5)①与④或⑤形成的两种10电子离子,在加热条件下能发生反应生成另两种10电子分子,写出对应的离子方程式:___________ 。
(6)⑥元素原子得电子能力强于⑩,请用原子结构知识解释其原因:___________ 。

(1)自然界中,组成物质最多的元素在周期表中的位置是
(2)写出由①④⑩三种元素形成的一种盐的电子式
(3)⑥⑦⑨的简单离子半径由大到小的顺序为
(4)根据对角线元素性质相似规则,写出②的最高价氧化物对应的水化物与稀硫酸反应的离子方程式:
(5)①与④或⑤形成的两种10电子离子,在加热条件下能发生反应生成另两种10电子分子,写出对应的离子方程式:
(6)⑥元素原子得电子能力强于⑩,请用原子结构知识解释其原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某粒子的结构示意图为:

试回答:
(1)当x-y=10时,该粒子为________ (填“原子”或“阳离子”“阴离子”)。
(2)当y=8时,该粒子可能是(写4种,写化学式):_______ 、________ 、_______ 、_______ 。
(3)比较当y=4时的元素氢化物与甲烷的稳定性______________ (填氢化物的化学式)。
(4)比较y=5、y=6、y=7的元素最高价氧化物对应水化物酸性强弱(写对应酸的化学式)________________________________ 。

试回答:
(1)当x-y=10时,该粒子为
(2)当y=8时,该粒子可能是(写4种,写化学式):
(3)比较当y=4时的元素氢化物与甲烷的稳定性
(4)比较y=5、y=6、y=7的元素最高价氧化物对应水化物酸性强弱(写对应酸的化学式)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和。则X、Y、Z、W分别为___________ (填元素符号,下同)。
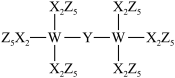
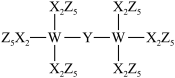
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子的最外层电子数与次外电子数之比为3∶4;N-与Ar原子电子层结构相同;X是短周期主族元素中原子半径最小的;Z是短周期主族元素中原子半径最大的;化合物XN常温下为气体。据此回答:
(1)N的最高价氧化物对应水化物的化学式是_______ 。
(2)Z与M形成的化合物水溶液显碱性,其原因是_______ (用离子方程式表示)。
(3)X与Y、X与M均可形成18电子分子,这两种分子在水溶液中反应可观察到的现象是_______ ,反应的化学方程式是_______ 。
(4)由X、Y、Z、M四种元素组成一种强酸的酸式盐,写出Ba(OH)2溶液中逐滴加入该盐溶液至中性的离子方程式_______ 。
(5)Y、Z、N形成的化合物的水溶液中离子浓度的大小顺序是_______ 。
(6)如图所示:
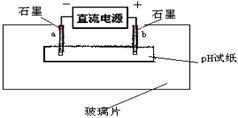
取一张用ZN溶液浸湿的pH试纸平铺在玻璃片上,取两根石墨棒做电极,接通直流电源。一段时间后,a电极处的pH试纸上可观察到的现象是_______ 。
(1)N的最高价氧化物对应水化物的化学式是
(2)Z与M形成的化合物水溶液显碱性,其原因是
(3)X与Y、X与M均可形成18电子分子,这两种分子在水溶液中反应可观察到的现象是
(4)由X、Y、Z、M四种元素组成一种强酸的酸式盐,写出Ba(OH)2溶液中逐滴加入该盐溶液至中性的离子方程式
(5)Y、Z、N形成的化合物的水溶液中离子浓度的大小顺序是
(6)如图所示:

取一张用ZN溶液浸湿的pH试纸平铺在玻璃片上,取两根石墨棒做电极,接通直流电源。一段时间后,a电极处的pH试纸上可观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】A、B、C、D四种元素处于同一周期,在同族元素中,A的气态氢化物的沸点最高,B的最高价氧化物对应的水化物的酸性在同周期中是最强的,C的电负性介于A、B之间,D与B相邻。
(1)C原子的价电子排布式为_____________ 。
(2)A、B、C三种元素原子的第一电离能由大到小的顺序是(写元素符号)_____________ 。
(3)B的单质分子中存在_____________ 个 键。
键。
(4)D和B形成一种超硬、耐磨、耐高温的新型化合物,该化合物属于_____________ 晶体,其硬度比金刚石_____________ (填“大”或“小”)。
(5)A的气态氢化物的沸点在同族中最高的原因是_____________ 。
(1)C原子的价电子排布式为
(2)A、B、C三种元素原子的第一电离能由大到小的顺序是(写元素符号)
(3)B的单质分子中存在
 键。
键。(4)D和B形成一种超硬、耐磨、耐高温的新型化合物,该化合物属于
(5)A的气态氢化物的沸点在同族中最高的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子,是产生温室效应的主要气体。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。人体缺E元素会得软骨病,D与E位于同主族。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C非金属性由强到弱的顺序为
(2)B的氢化物的分子式是
(3)写出化合物AC2的电子式:
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据相应信息回答有关问题。
I.物质结构和规律推断
如图为周期表中短周期的一部分,已知A是地壳中含量最多的元素。
(1)比较A、C的原子半径大小_______ (用原子符号表示)。
(2)比较C、D的简单氢化物的稳定性_______ (用化学式表示)。
II.实验操作和现象分析
(3)配制100ml0.1mol/L的NaOH溶液时,若仰视定容,则所配溶液的物质的量浓度_______ (填“偏大”、“偏小”或“不变")。
(4)将适量Ba(OH)2•8H2O晶体与NH4Cl晶体放入烧杯中,用玻璃棒快速搅拌,试着拿起烧杯观察,晶体变成糊状,此外还可观察到_______ 等现象。
III物质性质和成分探究
(5)将二氧化硫气体通入到品红溶液中,溶液褪色,体现了二氧化硫的_______ 性。
(6)在实验室,浓硝酸保存在棕色试剂瓶中,因浓硝酸见光或受热易分解,产生有刺激性气味的红棕色气体,该气体为_______ (用化学式表示)。
I.物质结构和规律推断
如图为周期表中短周期的一部分,已知A是地壳中含量最多的元素。
| A | ||
| B | C | D |
(1)比较A、C的原子半径大小
(2)比较C、D的简单氢化物的稳定性
II.实验操作和现象分析
(3)配制100ml0.1mol/L的NaOH溶液时,若仰视定容,则所配溶液的物质的量浓度
(4)将适量Ba(OH)2•8H2O晶体与NH4Cl晶体放入烧杯中,用玻璃棒快速搅拌,试着拿起烧杯观察,晶体变成糊状,此外还可观察到
III物质性质和成分探究
(5)将二氧化硫气体通入到品红溶液中,溶液褪色,体现了二氧化硫的
(6)在实验室,浓硝酸保存在棕色试剂瓶中,因浓硝酸见光或受热易分解,产生有刺激性气味的红棕色气体,该气体为
您最近一年使用:0次



