钒性能优良,用途广泛,有金属“维生素”之称。完成下列填空:
(1)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化学方程式是____ 。
(2)向上述所得溶液中加入KClO3溶液,完善并配平反应的离子方程式______ 。
ClO + VO2++ = Cl-+ VO
+ VO2++ = Cl-+ VO +
+
(3) V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应被吸收,则 、Cl-、VO2+还原性由大到小的顺序是
、Cl-、VO2+还原性由大到小的顺序是____ 。
(4)在20.00 mL 0.1 mol.L-1 溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是
溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是 ___ 。
a.VO2+ b. c. V2+ d.V
c. V2+ d.V
(1)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化学方程式是
(2)向上述所得溶液中加入KClO3溶液,完善并配平反应的离子方程式
ClO
 + VO2++ = Cl-+ VO
+ VO2++ = Cl-+ VO +
+ (3) V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应被吸收,则
 、Cl-、VO2+还原性由大到小的顺序是
、Cl-、VO2+还原性由大到小的顺序是(4)在20.00 mL 0.1 mol.L-1
 溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是
溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是 a.VO2+ b.
 c. V2+ d.V
c. V2+ d.V
2021·安徽合肥·一模 查看更多[4]
山东省泰安市宁阳县第四中学2023-2024学年高三上学期10月月考化学试题山东省泰安市宁阳县第四中学2022-2023学年高三上学期10月月考化学试题(等级考)(已下线)热点10 氧化还原反应与电极反应-2021年高考化学【热点·重点·难点】专练(新高考)安徽省合肥市2021年高三第一次教学质量检测化学试题
更新时间:2021-01-31 22:01:53
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】为了制备氯气,某同学查阅资料发现实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+ 2H2O。
MnCl2+Cl2↑+ 2H2O。
(1)请用双线桥法对该反应进行标注________________ 。
(2)写出该反应的离子方程式________________ 。
(3)该反应中,氧化剂和还原剂之比是________________ 。
 MnCl2+Cl2↑+ 2H2O。
MnCl2+Cl2↑+ 2H2O。(1)请用双线桥法对该反应进行标注
(2)写出该反应的离子方程式
(3)该反应中,氧化剂和还原剂之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】海洋的水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和 用以生产
用以生产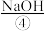 、
、 、
、 、
、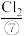 、
、 等,苦卤经过氯气氧化、热空气吹出、
等,苦卤经过氯气氧化、热空气吹出、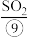 吸收等一系列操作可获得Br2。电解熔融氯化钠可冶炼
吸收等一系列操作可获得Br2。电解熔融氯化钠可冶炼 。海底埋藏大量可燃冰资源,
。海底埋藏大量可燃冰资源, 是一种清洁能源。
是一种清洁能源。
(1)上述标有序号的物质中属于电解质的是_______ (填序号,下同),属于非电解质的是_______ 。
(2)写出⑤溶于水的电离方程式_______ 。
(3)将⑧与④混合,写出离子反应方程式_______ 。
(4)将少量⑨通入④的溶液中,写出离子反应方程式_______ 。
(5)将⑤与④的溶液混合,写出离子反应方程式_______ 。
 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和 用以生产
用以生产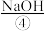 、
、 、
、 、
、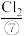 、
、 等,苦卤经过氯气氧化、热空气吹出、
等,苦卤经过氯气氧化、热空气吹出、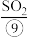 吸收等一系列操作可获得Br2。电解熔融氯化钠可冶炼
吸收等一系列操作可获得Br2。电解熔融氯化钠可冶炼 。海底埋藏大量可燃冰资源,
。海底埋藏大量可燃冰资源, 是一种清洁能源。
是一种清洁能源。(1)上述标有序号的物质中属于电解质的是
(2)写出⑤溶于水的电离方程式
(3)将⑧与④混合,写出离子反应方程式
(4)将少量⑨通入④的溶液中,写出离子反应方程式
(5)将⑤与④的溶液混合,写出离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求回答问题:
(1)将已配制好的饱和三氯化铁溶液滴入沸水中并煮沸一段时间,可得到红褐色液体,该反应的离子方程式为:___________
(2)实验室用氨水和硫酸铝溶液制取氢氧化铝,离子方程式为___________
(3)过氧化钠作为供氧剂时发生的化学反应(化学方程式):___________
(4)请用双线桥法标注以下氧化还原反应,标明电子转移数目,3Cl2+6KOH 5KCl+KClO3+3H2O
5KCl+KClO3+3H2O___________ ,氧化产物:还原产物=___________ (物质的量之比)。
(5)请用单线桥法标注以下氧化还原反应,标明电子转移数目:2 +5H2O2+6H+=2Mn2++5O2↑+5H2O
+5H2O2+6H+=2Mn2++5O2↑+5H2O___________ ,还原剂是___________ 。
(1)将已配制好的饱和三氯化铁溶液滴入沸水中并煮沸一段时间,可得到红褐色液体,该反应的离子方程式为:
(2)实验室用氨水和硫酸铝溶液制取氢氧化铝,离子方程式为
(3)过氧化钠作为供氧剂时发生的化学反应(化学方程式):
(4)请用双线桥法标注以下氧化还原反应,标明电子转移数目,3Cl2+6KOH
 5KCl+KClO3+3H2O
5KCl+KClO3+3H2O(5)请用单线桥法标注以下氧化还原反应,标明电子转移数目:2
 +5H2O2+6H+=2Mn2++5O2↑+5H2O
+5H2O2+6H+=2Mn2++5O2↑+5H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某一反应体系中有反应物和生成物共八种物质:KMnO4、SO2、CuS、H2SO4、CuSO4、K2SO4、MnSO4、H2O。反应中氧化过程如下:CuS→SO2。
(1)该反应中被还原的元素是_______ ,CuS发生氧化反应的实质是_______ 。
(2)若反应过程中转移了3mol电子,则参加反应的CuS的物质的量为_______ mol。
(3)写出并配平该反应的化学方程式_______ 。
(4)当KMnO4过量时,KMnO4会继续与SO2发生加下反应:2KMnO4+5SO2+2H2O→2H2SO4+K2SO4+2MnSO4。标出上述反应的电子转移数目和方向:_______ 该反应中氧化产物与还原产物的物质的量之比为_______ 。
(1)该反应中被还原的元素是
(2)若反应过程中转移了3mol电子,则参加反应的CuS的物质的量为
(3)写出并配平该反应的化学方程式
(4)当KMnO4过量时,KMnO4会继续与SO2发生加下反应:2KMnO4+5SO2+2H2O→2H2SO4+K2SO4+2MnSO4。标出上述反应的电子转移数目和方向:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知溶液中,还原性为HSO3->I-,氧化性为IO3->I2>SO42-。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系如图所示,请回答下列问题

下列问题:
(1)a点处的氧化产物是_________ (填化学式,下同),还原产物是_______ ,a点对应的离子方程式为_____ 。
(2)当n(I2)达到最大值时,n(IO3-)对应的最小值为____ mol,此时反应的离子方程式是_____________ 。
(3)当溶液中的I-为0.4mol时,加入的KIO3为______ mol。
(4)若向100mL 1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为____________ 。

下列问题:
(1)a点处的氧化产物是
(2)当n(I2)达到最大值时,n(IO3-)对应的最小值为
(3)当溶液中的I-为0.4mol时,加入的KIO3为
(4)若向100mL 1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】阅读下面科普信息,回答问题:
一个体重50kg的健康人含铁2 g,这2g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)在Fe+4HNO3(稀)===Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了______ 性,则56g Fe参加反应时,被还原的HNO3为____ g。
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食中毒的事件,其原因是NaNO2外观和食盐相似,又有咸味,却可以把人体内的Fe2+转化为Fe3+而失去了与O2结合的能力。(已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。)根据上述反应,可判断NaNO2具有__________ 性。鉴别NaNO2和NaCl,可选用的物质有:①水 ②碘化钾淀粉试纸 ③淀粉 ④白酒 ⑤食醋,你认为必须选用的物质有______ (填序号)。
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是______ 。
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)请配平以下化学方程式______ Al+______ NaNO3+______ NaOH=______ NaAlO2+______ N2↑+______ H2O;若反应过程中转移5mol 电子,则生成标准状况下N2的体积为______ 。
一个体重50kg的健康人含铁2 g,这2g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)在Fe+4HNO3(稀)===Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食中毒的事件,其原因是NaNO2外观和食盐相似,又有咸味,却可以把人体内的Fe2+转化为Fe3+而失去了与O2结合的能力。(已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。)根据上述反应,可判断NaNO2具有
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)请配平以下化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某溶液中含有 、Na+、
、Na+、 、
、 、
、 、
、 、Cl-、K+等八种离子,向其中加入Na2O2粉末,则:
、Cl-、K+等八种离子,向其中加入Na2O2粉末,则:
(1)离子浓度保持不变的是___________ ;
(2)离子浓度减小的是___________ ;
(3)离子浓度增大的是___________ ;
(4)其中发生的非氧化还原反应有___________ (用离子方程式表示);
(5)发生的氧化还原反应的有___________ (用离子方程式表示);。
 、Na+、
、Na+、 、
、 、
、 、
、 、Cl-、K+等八种离子,向其中加入Na2O2粉末,则:
、Cl-、K+等八种离子,向其中加入Na2O2粉末,则:(1)离子浓度保持不变的是
(2)离子浓度减小的是
(3)离子浓度增大的是
(4)其中发生的非氧化还原反应有
(5)发生的氧化还原反应的有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某中学生取纯净的Na2SO3·7H2O50.00g,经600℃以上的强热至恒重,分析及计算表明,恒重后的样品质量相当于无水亚硫酸钠的计算值,而且各元素的组成也符合计算值,但将它溶于水,却发现溶液的碱性大大高于期望值。经过仔细思考,这位同学解释了这种反常现象,并设计了一组实验,验证了自己的解释是正确的。
(1)他对反常现象的解释是:_______ (请用化学方程式表达)
(2)他设计的验证实验是:_______ (请用化学方程式表达)
(1)他对反常现象的解释是:
(2)他设计的验证实验是:
您最近一年使用:0次



