下表是海水晒盐时,在浓缩过程中析出的盐的种类和质量(每升海水析出的各种盐的质量,单位为克)。
试回答下列问题:
(1)海水中含量较高的是氯元素、钠元素和镁元素,但从表中数据可以看出,海水晒盐时先析出的是CaSO4,其原因可能是_______ 。
(2)综合成本等因素,通常海水晒盐时,在海水密度为1.21 g·mL-1~1.22 g·mL-1之间效益最佳,此时得到的粗盐中含有杂质,含有杂质的粗盐不能直接用作化工原料,需要进行精制。精制时,加入的试剂和进行的操作为①NaOH溶液、②BaCl2溶液、③Na2CO3液、④稀盐酸、⑤过滤,⑥蒸发结晶。则加入试剂和进行的操作的顺序为_______ (填标号)。
(3)经过精制的食盐在化工上有着广泛的用途。电解饱和食盐水可制得氯气和氢氧化钠,其反应的化学方程式为2NaCl+2H2O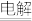 Cl2↑+H2↑+2NaOH,该反应中氧化产物与还原产物的物质的量之比为
Cl2↑+H2↑+2NaOH,该反应中氧化产物与还原产物的物质的量之比为_____ ,若将收集到的氯气通入石灰乳中,可制得漂白粉(主要成分为次氯酸钙),则工业上制漂白粉的化学方程式为_______ 。
(4)从海水中还可以提取镁、溴等。利用电解饱和食盐水得到的氯气作海水提取溴(在海水中主要以Br-形式存在)的氧化剂,则氯气作氧化剂得到溴单质反应的离子方程式为_____ 。
盐的种类 盐的质量(g) 海水的密度(g·mL-1) | CaSO4 | NaCl | MgCl2 | MgSO4 | NaBr |
1.13 | 0.56 | _______ | _______ | _______ | _______ |
1.20 | 0.91 | _______ | _______ | _______ | _______ |
1.21 | 0.05 | 3.26 | 0.004 | 0.008 | _______ |
1.22 | 0.015 | 9.65 | 0.01 | 0.04 | _______ |
1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
1.31 | _______ | 1.40 | 0.54 | 0.03 | 0.05 |
(1)海水中含量较高的是氯元素、钠元素和镁元素,但从表中数据可以看出,海水晒盐时先析出的是CaSO4,其原因可能是
(2)综合成本等因素,通常海水晒盐时,在海水密度为1.21 g·mL-1~1.22 g·mL-1之间效益最佳,此时得到的粗盐中含有杂质,含有杂质的粗盐不能直接用作化工原料,需要进行精制。精制时,加入的试剂和进行的操作为①NaOH溶液、②BaCl2溶液、③Na2CO3液、④稀盐酸、⑤过滤,⑥蒸发结晶。则加入试剂和进行的操作的顺序为
(3)经过精制的食盐在化工上有着广泛的用途。电解饱和食盐水可制得氯气和氢氧化钠,其反应的化学方程式为2NaCl+2H2O
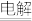 Cl2↑+H2↑+2NaOH,该反应中氧化产物与还原产物的物质的量之比为
Cl2↑+H2↑+2NaOH,该反应中氧化产物与还原产物的物质的量之比为(4)从海水中还可以提取镁、溴等。利用电解饱和食盐水得到的氯气作海水提取溴(在海水中主要以Br-形式存在)的氧化剂,则氯气作氧化剂得到溴单质反应的离子方程式为
更新时间:2021-02-02 20:42:51
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。
(1)工业上将氯气溶于一定浓度的氢氧化钠溶液可制得“84消毒液”,用电子式表示“84消毒液”的有效成分是__________ 。
(2)二氧化氯(ClO2)是一种黄绿色易溶于水的气体,也可用于自来水的杀菌消毒。工业上常用NaClO3和Na2SO3溶液混合并加入稀H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为______________ 。
(1)工业上将氯气溶于一定浓度的氢氧化钠溶液可制得“84消毒液”,用电子式表示“84消毒液”的有效成分是
(2)二氧化氯(ClO2)是一种黄绿色易溶于水的气体,也可用于自来水的杀菌消毒。工业上常用NaClO3和Na2SO3溶液混合并加入稀H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)化学与生产生活联系密切,请书写对应的化学方程式:
①漂白粉中的 能与空气中的
能与空气中的 和水蒸气发生反应:
和水蒸气发生反应:_________________________ 。
②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:__________________________ 。
③常温下,将氯气通入氢氧化钠溶液中,可以得到一种漂白液:__________________________ 。
(2)海水开发利用的部分过程如图所示:
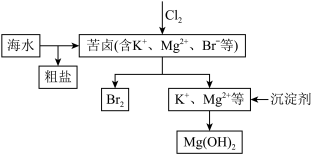
④向苦卤中通入氯气,发生反应的离子方程式是_____________________________________
⑤工业生产中常选用石灰乳作为沉淀剂,相关反应的离子方程式是______________________
⑥富集溴一般先用空气和水蒸气吹出单质溴,再用 将其还原吸收,相关反应的化学方程式是
将其还原吸收,相关反应的化学方程式是_______ 。
(1)化学与生产生活联系密切,请书写对应的化学方程式:
①漂白粉中的
 能与空气中的
能与空气中的 和水蒸气发生反应:
和水蒸气发生反应:②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:
③常温下,将氯气通入氢氧化钠溶液中,可以得到一种漂白液:
(2)海水开发利用的部分过程如图所示:

④向苦卤中通入氯气,发生反应的离子方程式是
⑤工业生产中常选用石灰乳作为沉淀剂,相关反应的离子方程式是
⑥富集溴一般先用空气和水蒸气吹出单质溴,再用
 将其还原吸收,相关反应的化学方程式是
将其还原吸收,相关反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.NaClO是“84”消毒液的有效成分。请回答下列问题:
(1)NaClO中Cl元素的化合价是_______ 。
(2)浸泡衣物时加入“84”消毒液,在空气中放置一段时间后漂白效果更好,结合离子方程式解释原因:_______ 。(已知酸性: )
)
(3)若将“84”消毒液与洁厕灵(主要成分是HCl)混合使用,会产生黄绿色的有毒气体,其反应的离子方程式是_______ 。
Ⅱ. 是一种有毒气体,如果泄漏会造成严重的危害。
是一种有毒气体,如果泄漏会造成严重的危害。
(4)已知 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。该反应中被氧化和未被氧化的
是否泄漏。该反应中被氧化和未被氧化的 分子的个数比为
分子的个数比为_______ 。
(5)喷射石灰乳等碱性物质可以减轻少量 泄漏造成的危害。
泄漏造成的危害。 和石灰乳反应的化学方程式是
和石灰乳反应的化学方程式是_______ 。
(1)NaClO中Cl元素的化合价是
(2)浸泡衣物时加入“84”消毒液,在空气中放置一段时间后漂白效果更好,结合离子方程式解释原因:
 )
)(3)若将“84”消毒液与洁厕灵(主要成分是HCl)混合使用,会产生黄绿色的有毒气体,其反应的离子方程式是
Ⅱ.
 是一种有毒气体,如果泄漏会造成严重的危害。
是一种有毒气体,如果泄漏会造成严重的危害。(4)已知
 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。该反应中被氧化和未被氧化的
是否泄漏。该反应中被氧化和未被氧化的 分子的个数比为
分子的个数比为(5)喷射石灰乳等碱性物质可以减轻少量
 泄漏造成的危害。
泄漏造成的危害。 和石灰乳反应的化学方程式是
和石灰乳反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】海洋化学资源的综合利用对人类的发展意义重大。
(1)经海水晒盐获得的粗盐水中含有Ca2+、Mg2+、SO 三种杂质离子,为了除去上述三种杂质离子,需加入四种试剂:①Na2CO3、②BaCl2、③NaOH、④稀盐酸。①四种试剂的加入次序正确的是
三种杂质离子,为了除去上述三种杂质离子,需加入四种试剂:①Na2CO3、②BaCl2、③NaOH、④稀盐酸。①四种试剂的加入次序正确的是___________ (填字母)。
a.④①②③ b.②①③④ c.③①②④ d.②③①④
②加入稀盐酸的目的是___________ (用离子方程式表示)。
(2)利用氧化还原反应原理,将Cl2通入提取食盐后的母液中,将溶液中的溴离子转化为溴单质,再鼓入热空气,使溴单质从溶液中分离出来。
①鼓入热空气将溴单质从溶液中分离出来的原理是___________ 。
②将溴离子转化为溴单质的离子反应方程式为___________ 。
(1)经海水晒盐获得的粗盐水中含有Ca2+、Mg2+、SO
 三种杂质离子,为了除去上述三种杂质离子,需加入四种试剂:①Na2CO3、②BaCl2、③NaOH、④稀盐酸。①四种试剂的加入次序正确的是
三种杂质离子,为了除去上述三种杂质离子,需加入四种试剂:①Na2CO3、②BaCl2、③NaOH、④稀盐酸。①四种试剂的加入次序正确的是a.④①②③ b.②①③④ c.③①②④ d.②③①④
②加入稀盐酸的目的是
(2)利用氧化还原反应原理,将Cl2通入提取食盐后的母液中,将溶液中的溴离子转化为溴单质,再鼓入热空气,使溴单质从溶液中分离出来。
①鼓入热空气将溴单质从溶液中分离出来的原理是
②将溴离子转化为溴单质的离子反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】必修Ⅰ第二章带领我们认识了海水中重要元素-钠和氯,同时引入了一个新的物理量——物质的量,帮助我们建立宏观物质和微观微粒之间的联系。以下是小明和李华两位同学学习第二章后相互赠送的化学礼物——亲自命制的习题。作为他们共同的好朋友,请你也收下并完成这两份礼物,陪伴他们共同成长与进步。
Ⅰ.小明送出的礼物(节选):
(1)钠长期置于空气中,最后形成的物质是_______ ,该物质与足量盐酸反应的离子方程式为_______ ,为除去该反应生成的气体中混有的HCl,应选用试剂_______ 。
(2)加热法除去碳酸钠固体中少量的碳酸氢钠反应化学方程式为_______ 。
Ⅱ.李华送出的礼物(节选):
(3)除去氯气中的HCl选用试剂_______ 。
(4)漂白粉的制备化学方程式_______ 。
(5)56g Fe与足量的氯气完全反应转移_______ 个电子数。
(6)相同质量的CO和CO2所含的氧原子个数之比是_______ 。
Ⅰ.小明送出的礼物(节选):
(1)钠长期置于空气中,最后形成的物质是
(2)加热法除去碳酸钠固体中少量的碳酸氢钠反应化学方程式为
Ⅱ.李华送出的礼物(节选):
(3)除去氯气中的HCl选用试剂
(4)漂白粉的制备化学方程式
(5)56g Fe与足量的氯气完全反应转移
(6)相同质量的CO和CO2所含的氧原子个数之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】填空。
(1)配制240mL、0.5mol/L的NaOH溶液,选用容量瓶的规格是___________ ,定容时向容量瓶中加蒸馏水超过刻度线,其结果___________ (填”偏大”、"偏小”、或“不变”)。
(2)从石油中分离出汽油、煤油和柴油等,所采用的方法是___________ (填“干馏”或“分馏”),属于___________ 变化(填“物理”或“化学”)。
(3)除去二氧化碳气体中的氯化氢杂质,选用的试剂是___________ (填“NaOH溶液”或“饱和NaHCO3溶液”)。
(4)如图是实验室制取氨气的装置,回答下列问题:

①写出该反应的化学方程式___________ 。
②收集氨气的方法是___________ 。
③验证氨气是否收集满的方法是___________ (写一种)。
(1)配制240mL、0.5mol/L的NaOH溶液,选用容量瓶的规格是
(2)从石油中分离出汽油、煤油和柴油等,所采用的方法是
(3)除去二氧化碳气体中的氯化氢杂质,选用的试剂是
(4)如图是实验室制取氨气的装置,回答下列问题:

①写出该反应的化学方程式
②收集氨气的方法是
③验证氨气是否收集满的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】从海水中可以获得淡水、食盐并可提取镁和溴等物质。
(1)海水淡化的方法主要有_____ (填一种);
(2)下列物质不需要经过化学变化就能从海水中获得的物质是______ (填序号);
(3)从海水中提取溴和镁的流程如下:

① 写出下列步骤的离子方程式或化学方程式
步骤I的化学方程式:_________________________________________________ ;
步骤III的离子方程式:________________________________________________ ;
步骤IV的化学方程式:________________________________________________ 。
②操作A是_________________ ,操作B是____________________ ,从步骤II得到的溶液中提取
溴还需要进行的操作有:萃取、_________ 、蒸馏。
(1)海水淡化的方法主要有
(2)下列物质不需要经过化学变化就能从海水中获得的物质是
| A.液溴 | B.食盐 | C.氢气 | D.淡水 |

① 写出下列步骤的离子方程式或化学方程式
步骤I的化学方程式:
步骤III的离子方程式:
步骤IV的化学方程式:
②操作A是
溴还需要进行的操作有:萃取、
您最近一年使用:0次
【推荐2】溴和碘的化合物在生产和生活中有广泛的用途.
(1)市场销售的某种食用精制盐中含碘酸钾。
①碘酸钾与碘化钾在酸性条件下发生如下反应,配平该反应的化学方程式:
( )  +
+( ) KI+( ) 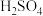 =
=( )  +
+( )  +
+( )
②上述反应生成的I2可用四氯化碳检验,现象为________________________ 。
向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
Na2SO3稀溶液与I2反应的离子方程式是________________________ 。
(2)海水提溴过程中溴元素的变化如下:

①过程I,海水显碱性,调其pH<3.5后,再通入氯气,调节海水pH可提高C12的利用率,用平衡原理解释其原因是_______________________ 。
②过程II,用热空气将溴赶出,再用浓Na2CO3溶液吸收。完成并配平下列方程式。
( ) 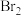 +
+( ) 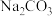 =
=( )  +
+( )  +
+( )
③过程III,用硫酸酸化可得Br2和Na2SO4的混合溶液。相同条件下,若用盐酸酸化,则所得溴的质量减少,原因是_________________________ 。
④NaBrO3是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入NaBrO3溶液,当加入 2.6molNaBrO3时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:

则原溶液中NaI的物质的量为_________ mol.
(1)市场销售的某种食用精制盐中含碘酸钾。
①碘酸钾与碘化钾在酸性条件下发生如下反应,配平该反应的化学方程式:
 +
+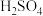 =
= +
+ +
+②上述反应生成的I2可用四氯化碳检验,现象为
向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
Na2SO3稀溶液与I2反应的离子方程式是
(2)海水提溴过程中溴元素的变化如下:

①过程I,海水显碱性,调其pH<3.5后,再通入氯气,调节海水pH可提高C12的利用率,用平衡原理解释其原因是
②过程II,用热空气将溴赶出,再用浓Na2CO3溶液吸收。完成并配平下列方程式。
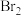 +
+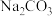 =
= +
+ +
+③过程III,用硫酸酸化可得Br2和Na2SO4的混合溶液。相同条件下,若用盐酸酸化,则所得溴的质量减少,原因是
④NaBrO3是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入NaBrO3溶液,当加入 2.6molNaBrO3时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:

则原溶液中NaI的物质的量为
您最近一年使用:0次

 的熔点为712℃。
的熔点为712℃。

