Ⅰ.NaClO是“84”消毒液的有效成分。请回答下列问题:
(1)NaClO中Cl元素的化合价是_______ 。
(2)浸泡衣物时加入“84”消毒液,在空气中放置一段时间后漂白效果更好,结合离子方程式解释原因:_______ 。(已知酸性: )
)
(3)若将“84”消毒液与洁厕灵(主要成分是HCl)混合使用,会产生黄绿色的有毒气体,其反应的离子方程式是_______ 。
Ⅱ. 是一种有毒气体,如果泄漏会造成严重的危害。
是一种有毒气体,如果泄漏会造成严重的危害。
(4)已知 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。该反应中被氧化和未被氧化的
是否泄漏。该反应中被氧化和未被氧化的 分子的个数比为
分子的个数比为_______ 。
(5)喷射石灰乳等碱性物质可以减轻少量 泄漏造成的危害。
泄漏造成的危害。 和石灰乳反应的化学方程式是
和石灰乳反应的化学方程式是_______ 。
(1)NaClO中Cl元素的化合价是
(2)浸泡衣物时加入“84”消毒液,在空气中放置一段时间后漂白效果更好,结合离子方程式解释原因:
 )
)(3)若将“84”消毒液与洁厕灵(主要成分是HCl)混合使用,会产生黄绿色的有毒气体,其反应的离子方程式是
Ⅱ.
 是一种有毒气体,如果泄漏会造成严重的危害。
是一种有毒气体,如果泄漏会造成严重的危害。(4)已知
 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。该反应中被氧化和未被氧化的
是否泄漏。该反应中被氧化和未被氧化的 分子的个数比为
分子的个数比为(5)喷射石灰乳等碱性物质可以减轻少量
 泄漏造成的危害。
泄漏造成的危害。 和石灰乳反应的化学方程式是
和石灰乳反应的化学方程式是
更新时间:2022-10-31 13:54:40
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】锂离子电池广泛应用于日常电子产品中,也是电动汽车动力电池的首选.正极材料的选择决定了锂离子电池的性能.磷酸铁钾(LiFePO4)以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”。
(1)高温固相法是磷酸铁锂生产的主要方法。通常以铁盐、磷酸盐和锂盐为原料,按化学计量比充分混匀后,在惰性气氛的保护中先经过较低温预分解,再经高温焙烧,研磨粉碎制成。其反应原理如下:
Li2CO3+2FeC2O4•2H2O+2NH4H2PO4═2NH3↑+3CO2↑+______ +_______ +_______
①完成上述化学方程式.
②理论上,反应中每转移0.15mol电子,会生成LiFePO4______________ g;
③反应需在惰性气氛的保护中进行,其原因是______________ ;
(2)磷酸亚铁锂电池装置如图所示,其中正极材料橄榄石型LiFePO4通过粘合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。

电池工作时的总反应为:LiFePO4+6C Li1-xFePO4+LixC6,则放电时,正极的电极反应式为
Li1-xFePO4+LixC6,则放电时,正极的电极反应式为______________ 。充电时,Li+迁移方向为______________ (填“由左向右”或“由右向左”),图中聚合物隔膜应为______________ (填“阳”或“阴”)离子交换膜。
(3)用该电池电解精炼铜。若用放电的电流强度I=2.0A的电池工作10分钟,电解精炼铜得到铜0.32g,则电流利用效率为______________ (保留小数点后一位)。(已知:法拉第常数F=96500C/mol,电流利用效率=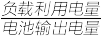 100%)
100%)
(4)废旧磷酸亚铁锂电池的正极材料中的LiFePO4难溶于水,可用H2SO4和H2O2的混合溶液浸取,发生反应的离子方程式为______________ 。
(1)高温固相法是磷酸铁锂生产的主要方法。通常以铁盐、磷酸盐和锂盐为原料,按化学计量比充分混匀后,在惰性气氛的保护中先经过较低温预分解,再经高温焙烧,研磨粉碎制成。其反应原理如下:
Li2CO3+2FeC2O4•2H2O+2NH4H2PO4═2NH3↑+3CO2↑+
①完成上述化学方程式.
②理论上,反应中每转移0.15mol电子,会生成LiFePO4
③反应需在惰性气氛的保护中进行,其原因是
(2)磷酸亚铁锂电池装置如图所示,其中正极材料橄榄石型LiFePO4通过粘合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。

电池工作时的总反应为:LiFePO4+6C
 Li1-xFePO4+LixC6,则放电时,正极的电极反应式为
Li1-xFePO4+LixC6,则放电时,正极的电极反应式为(3)用该电池电解精炼铜。若用放电的电流强度I=2.0A的电池工作10分钟,电解精炼铜得到铜0.32g,则电流利用效率为
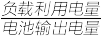 100%)
100%)(4)废旧磷酸亚铁锂电池的正极材料中的LiFePO4难溶于水,可用H2SO4和H2O2的混合溶液浸取,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】亚硫酰氯(SOCl2)在农药、医药、染料等生产中有重要应用,是一种无色或淡黄色液体,易挥发,遇水极易反应生成两种酸性气体。回答下列问题:
(1)根据价电子对互斥理论,亚硫酰氯空间构型为_______ ,其构成元素电负性由大到小的顺序为_______ 。
(2)实验室可通过将二氧化硫和氯气通入一氯化硫(S2Cl2)中反应制取亚硫酰氯。
①一氯化硫的电子式为_______ ;
②该反应中还原剂与氧化剂的物质的量之比为_______ ;
③向Ba(OH)2溶液中滴加少量亚硫酰氯,有白色沉淀生成,发生反应的离子方程式为_______ 。
(3)MgCl2·6H2O、AlCl3·6H2O、FeCl2·4H2O等结晶水合氯化物在空气中受热脱水易发生水解反应,常用亚硫酰氯作脱水剂以制取无水氯化物。
①在加热条件下,亚硫酰氯与MgCl2·6H2O反应的化学方程式为_______ 。
②MgCl2·6H2O在空气中受热脱水过程中,热重分析测得剩余固体质量占初始固体质量的百分含量随温度变化的曲线如图所示。
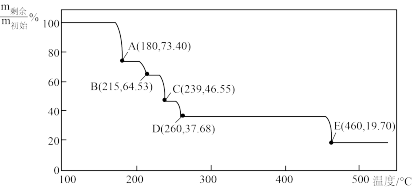
试判断A点固体的化学式为_______ ;460℃时发生反应的化学方程式为_______ 。
(1)根据价电子对互斥理论,亚硫酰氯空间构型为
(2)实验室可通过将二氧化硫和氯气通入一氯化硫(S2Cl2)中反应制取亚硫酰氯。
①一氯化硫的电子式为
②该反应中还原剂与氧化剂的物质的量之比为
③向Ba(OH)2溶液中滴加少量亚硫酰氯,有白色沉淀生成,发生反应的离子方程式为
(3)MgCl2·6H2O、AlCl3·6H2O、FeCl2·4H2O等结晶水合氯化物在空气中受热脱水易发生水解反应,常用亚硫酰氯作脱水剂以制取无水氯化物。
①在加热条件下,亚硫酰氯与MgCl2·6H2O反应的化学方程式为
②MgCl2·6H2O在空气中受热脱水过程中,热重分析测得剩余固体质量占初始固体质量的百分含量随温度变化的曲线如图所示。

试判断A点固体的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】有下列6种物质: 、
、 、
、 、
、 、
、 、
、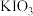 组成一个氧化还原反应,请回答下列问题
组成一个氧化还原反应,请回答下列问题
(1)将这6种物质分别填入下面对应的横线上,组成化学方程式并配平:___________ ___________
(2)反应物中发生氧化反应的物质是___________  填化学式
填化学式 ,被还原的元素是
,被还原的元素是___________ ;
(3)反应中1mol氧化剂___________  填“得到”或“失去”
填“得到”或“失去”
___________ mol电子;
(4)生应物中还原产物是___________  填化学式
填化学式 。
。
 、
、 、
、 、
、 、
、 、
、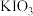 组成一个氧化还原反应,请回答下列问题
组成一个氧化还原反应,请回答下列问题(1)将这6种物质分别填入下面对应的横线上,组成化学方程式并配平:

(2)反应物中发生氧化反应的物质是
 填化学式
填化学式 ,被还原的元素是
,被还原的元素是(3)反应中1mol氧化剂
 填“得到”或“失去”
填“得到”或“失去”
(4)生应物中还原产物是
 填化学式
填化学式 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】亚硝酸钠(化学式为 NaNO2)是一种常用的防腐剂,回答下列问题:
(1)NaNO2 中 N 元素的化合价为_________ .
(2)亚硝酸钠在 320°C 时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。该反应的化学方程式_________________ 。
(3)我国规定火腿肠中亚硝酸钠添加标准为每千克食品含量不超过 150 毫克,以此计算,200g 15%的亚硝酸钠溶液至少可用于生产火腿肠______ 千克。
(4)在酸性条件下,NaNO2与按物质的量 1:1 恰好完全反应,且I-被氧化为 I2时,产物中含氮的物质为________ (填化学式)。
(5)工业废水中的 NaNO2 可用铝粉除去,已知此体系中包含 AI、NaAlO2、NaNO2、NaOH、NH3、H2O 六种物质。该反应的化学方程式为____________ 。
(6)某同学设计实验对工业产品中 NaNO2 的含量进行测定,你取固体样品 2g,完全溶解配制成溶液 100mL 取出 25mL 溶液用 0.100 mol/L 酸性 KMnO4 溶液进行滴定(杂质不与 KMnO4 反应),实验所得数据如下表所示:
该样品中亚硝酸钠的质量分数为_________ .(已知:5NO2-+2MnO4-+6H+ = 5NO3-+2Mn2++3H2O)
(1)NaNO2 中 N 元素的化合价为
(2)亚硝酸钠在 320°C 时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。该反应的化学方程式
(3)我国规定火腿肠中亚硝酸钠添加标准为每千克食品含量不超过 150 毫克,以此计算,200g 15%的亚硝酸钠溶液至少可用于生产火腿肠
(4)在酸性条件下,NaNO2与按物质的量 1:1 恰好完全反应,且I-被氧化为 I2时,产物中含氮的物质为
(5)工业废水中的 NaNO2 可用铝粉除去,已知此体系中包含 AI、NaAlO2、NaNO2、NaOH、NH3、H2O 六种物质。该反应的化学方程式为
(6)某同学设计实验对工业产品中 NaNO2 的含量进行测定,你取固体样品 2g,完全溶解配制成溶液 100mL 取出 25mL 溶液用 0.100 mol/L 酸性 KMnO4 溶液进行滴定(杂质不与 KMnO4 反应),实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗KMnO4溶液体积/mL | 20.70 | 20.02 | 20.00 | 19.98 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)消毒液中的有效成分是_______ ,制备 消毒液的反应的化学方程式为
消毒液的反应的化学方程式为_______ 。它的消毒原理是_______ (用化学方程式表示)。由以上反应证明 是弱酸,酸性比碳酸
是弱酸,酸性比碳酸_______ 。
(2)将 和
和 的混合物加入足量的水中充分反应后,生成标准状况下的气体
的混合物加入足量的水中充分反应后,生成标准状况下的气体 ,所得溶液的体积为
,所得溶液的体积为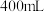 。试计算:
。试计算:
①原混合物中 的质量为
的质量为_______  。
。
②所得溶液的物质的量浓度为_______  。
。
(1)消毒液中的有效成分是
 消毒液的反应的化学方程式为
消毒液的反应的化学方程式为 是弱酸,酸性比碳酸
是弱酸,酸性比碳酸(2)将
 和
和 的混合物加入足量的水中充分反应后,生成标准状况下的气体
的混合物加入足量的水中充分反应后,生成标准状况下的气体 ,所得溶液的体积为
,所得溶液的体积为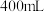 。试计算:
。试计算:①原混合物中
 的质量为
的质量为 。
。②所得溶液的物质的量浓度为
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)某化工厂用氯气与石灰乳生产漂白粉,该厂出厂产品说明书如图:
①漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式:___ ,____ 。
②某实验室研究员将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,收集到标准状况下448mL气体,则该漂白粉中所含有效成分的质量为___ (假设漂白粉中的其他成分不与硝酸反应)。
(2)将14gNa2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体1.12L,所得溶液的体积为400mL。试计算:原混合物中Na2O的质量为___ g,所得溶液中Na+的物质的量浓度为___ mol·L‑1。
(1)某化工厂用氯气与石灰乳生产漂白粉,该厂出厂产品说明书如图:
| 使用说明 【主要成分】次氯酸钙、氯化钙 【用途用量】取漂白粉2至3g,水1000g,配成溶液,将病人 用其浸泡5至10分钟。如需要,浓度可提高,时间可延长。 【注意事项】密封避光保存于阴凉干燥处,随配随用,有腐蚀性, 少与手接触。 |
①漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式:
②某实验室研究员将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,收集到标准状况下448mL气体,则该漂白粉中所含有效成分的质量为
(2)将14gNa2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体1.12L,所得溶液的体积为400mL。试计算:原混合物中Na2O的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某校高一化学研究性学习小组对氯气在日常生活中的用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等。
(1)氯气可以用于漂白、消毒的原因是氯气能与水反应,生成具有漂白、消毒作用的___________ (填名称),相关反应的离子方程式为___________ 。
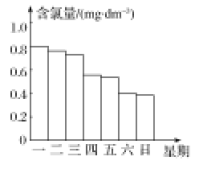
(2)在调查某室外大型游泳池夏季池水消毒情况时,该小组成员了解到,游泳池每周一上午8:00换水,然后通入氯气消毒,通常游泳池水中的含氯量(有效氯)控制在 时,效果最好。如图是该小组测定的某周每天19:00时游泳池水中的含氯量,则哪几天使用游泳池相对不太安全?
时,效果最好。如图是该小组测定的某周每天19:00时游泳池水中的含氯量,则哪几天使用游泳池相对不太安全?___________ 。
(3)根据下图判断,你认为哪几天的天气炎热、阳光强烈?___________ ,请写出可能的原因:___________ (用化学方程式表示)。
(4)小型游泳池通常使用漂白液(含 的溶液)而非氯气来消毒,试举出使用漂白液而非氯气消毒的理由:
的溶液)而非氯气来消毒,试举出使用漂白液而非氯气消毒的理由:___________ (写出一个即可);用化学方程式说明工业上生产漂白液的原理:___________ 。
(1)氯气可以用于漂白、消毒的原因是氯气能与水反应,生成具有漂白、消毒作用的
(2)在调查某室外大型游泳池夏季池水消毒情况时,该小组成员了解到,游泳池每周一上午8:00换水,然后通入氯气消毒,通常游泳池水中的含氯量(有效氯)控制在
 时,效果最好。如图是该小组测定的某周每天19:00时游泳池水中的含氯量,则哪几天使用游泳池相对不太安全?
时,效果最好。如图是该小组测定的某周每天19:00时游泳池水中的含氯量,则哪几天使用游泳池相对不太安全?(3)根据下图判断,你认为哪几天的天气炎热、阳光强烈?

(4)小型游泳池通常使用漂白液(含
 的溶液)而非氯气来消毒,试举出使用漂白液而非氯气消毒的理由:
的溶液)而非氯气来消毒,试举出使用漂白液而非氯气消毒的理由:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】“化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学反应方程式__ 。
(2)小苏打是食品加工业应用最广泛的疏松剂,请写出碳酸氢钠与氢氧化钠的离子方程式__ 。
(3)舍勒发现氯气的方法至今还是实验室中制取氯气的主要方法之一,请写出相应的离子方程式__ 。
(4)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①工业上利用氯气和氢氧化钙反应可制得漂白粉,漂白粉主要成分的化学式为__ ,制备漂白粉的离子方程式为__ 。
②将灼热的铜丝伸入盛有氯气的集气瓶中,反应现象为__ 。将反应后的产物溶于水配成饱和溶液,向溶液中加入一小块金属钠,反应的离子方程式为__ ,除了钠与水反应的现象其余可以观察到的现象是__ 。
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学反应方程式
(2)小苏打是食品加工业应用最广泛的疏松剂,请写出碳酸氢钠与氢氧化钠的离子方程式
(3)舍勒发现氯气的方法至今还是实验室中制取氯气的主要方法之一,请写出相应的离子方程式
(4)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①工业上利用氯气和氢氧化钙反应可制得漂白粉,漂白粉主要成分的化学式为
②将灼热的铜丝伸入盛有氯气的集气瓶中,反应现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ca(ClO)2、NaClO、FeCl3、Al2O3、Fe2O3、Mn2O7等都是重要的化合物。回答下列问题:
(1)属于酸性氧化物的是______ (填化学式),其相应的钾盐具有_____ (填“强氧化性”或“强还原性”),FeSO4溶液能使该钾盐的酸性溶液褪色,其原因为________ (用离子方程式解释)。
(2)属于“84"消毒液成分的是______ (填化学式),其在空气中易变质,产物之一为碳酸氢钠,写出发生该反应的离子方程式:_______ 。
(3)用覆铜板制作印刷电路板的原理是_______ (用离子方程式表示),检验“腐蚀液”中有无Fe3+的试剂为______ (填化学式)。
(4)将氯气通入冷的_____ (填物质名称)中可制得以Ca(ClO)2为有效成分的漂白粉,该过程中转移2mol电子时,消耗氧化剂与还原剂的质量之比为________ 。
(1)属于酸性氧化物的是
(2)属于“84"消毒液成分的是
(3)用覆铜板制作印刷电路板的原理是
(4)将氯气通入冷的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】新型冠状病毒蔓延期间,为做好自我保护,我们要减少外出,避免与表现出有呼吸道疾病症状的人密切接触,外出最重要的防护措施是佩戴符合要求的口罩。在生活中常见的口罩一般有棉布口罩、医用外科口罩、活性炭口罩和N95口罩。也可以在实验室进行制备84消毒液(有效成分是NaClO)。
(1)新型冠状病毒可以通过气溶胶传播,气溶胶属于分散系中的___________ (“溶液”、“胶体”、“悬浊液”)。
(2)佩戴口罩预防疾病的原理相当于化学实验中的_________ 操作。(“蒸发”、“过滤”“萃取”)
(3)生成N95口罩的主要原料是聚丙烯,它属于___________ (填“金属材料”或“合成材料”)
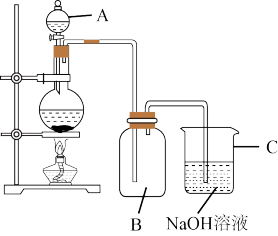
(4)如图是模拟84消毒液的装置,实验室先制备氯气,再通入氢氧化钠溶液,写出发生的化学反应方程式:__________________________ ,氧化剂是_________ ,氧化产物是_________ 。
(5)84消毒液和洁厕灵混合使用时会发生化学反应2HCl+NaClO=NaCl+H2O+X↑,使消毒液失效,杀菌消毒能力减弱,易发生生命危险,X为_________ 。
(1)新型冠状病毒可以通过气溶胶传播,气溶胶属于分散系中的
(2)佩戴口罩预防疾病的原理相当于化学实验中的
(3)生成N95口罩的主要原料是聚丙烯,它属于
(4)如图是模拟84消毒液的装置,实验室先制备氯气,再通入氢氧化钠溶液,写出发生的化学反应方程式:

(5)84消毒液和洁厕灵混合使用时会发生化学反应2HCl+NaClO=NaCl+H2O+X↑,使消毒液失效,杀菌消毒能力减弱,易发生生命危险,X为
您最近一年使用:0次



