新型冠状病毒蔓延期间,为做好自我保护,我们要减少外出,避免与表现出有呼吸道疾病症状的人密切接触,外出最重要的防护措施是佩戴符合要求的口罩。在生活中常见的口罩一般有棉布口罩、医用外科口罩、活性炭口罩和N95口罩。也可以在实验室进行制备84消毒液(有效成分是NaClO)。
(1)新型冠状病毒可以通过气溶胶传播,气溶胶属于分散系中的___________ (“溶液”、“胶体”、“悬浊液”)。
(2)佩戴口罩预防疾病的原理相当于化学实验中的_________ 操作。(“蒸发”、“过滤”“萃取”)
(3)生成N95口罩的主要原料是聚丙烯,它属于___________ (填“金属材料”或“合成材料”)
(4)如图是模拟84消毒液的装置,实验室先制备氯气,再通入氢氧化钠溶液,写出发生的化学反应方程式:__________________________ ,氧化剂是_________ ,氧化产物是_________ 。
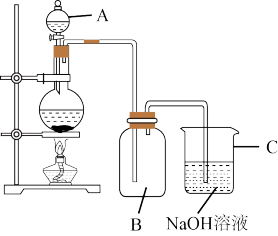
(5)84消毒液和洁厕灵混合使用时会发生化学反应2HCl+NaClO=NaCl+H2O+X↑,使消毒液失效,杀菌消毒能力减弱,易发生生命危险,X为_________ 。
(1)新型冠状病毒可以通过气溶胶传播,气溶胶属于分散系中的
(2)佩戴口罩预防疾病的原理相当于化学实验中的
(3)生成N95口罩的主要原料是聚丙烯,它属于
(4)如图是模拟84消毒液的装置,实验室先制备氯气,再通入氢氧化钠溶液,写出发生的化学反应方程式:

(5)84消毒液和洁厕灵混合使用时会发生化学反应2HCl+NaClO=NaCl+H2O+X↑,使消毒液失效,杀菌消毒能力减弱,易发生生命危险,X为
更新时间:2020-12-02 19:26:21
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】1774年,舍勒在研究软锰矿(主要成分是 )的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为Chlorine(中文命名“氯气”)。
)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为Chlorine(中文命名“氯气”)。
(1)实验室沿用舍勒的方法制取 的化学方程式为
的化学方程式为___________ 。
(2)实验室中用 溶液吸收尾气中的
溶液吸收尾气中的 的离子方程式为
的离子方程式为___________ ,配制 的
的 溶液
溶液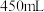 ,所需
,所需 固体的质量为
固体的质量为___________ 。
(3)用 可制备
可制备 溶液,将
溶液,将 溶液加入到滴有酚酞的
溶液加入到滴有酚酞的 溶液中,观察到溶液红色褪去。溶液褪色的原因可能是①
溶液中,观察到溶液红色褪去。溶液褪色的原因可能是① 被
被 中和,②
中和,②___________ 。设计实验探究溶液红色褪去的原因___________ 。
(4) 溶液不能长久存放的原因是
溶液不能长久存放的原因是___________ (用化学方程式表示),检验长久存放的 溶液中阴离子的实验操作及现象是
溶液中阴离子的实验操作及现象是___________ 。
 )的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为Chlorine(中文命名“氯气”)。
)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为Chlorine(中文命名“氯气”)。(1)实验室沿用舍勒的方法制取
 的化学方程式为
的化学方程式为(2)实验室中用
 溶液吸收尾气中的
溶液吸收尾气中的 的离子方程式为
的离子方程式为 的
的 溶液
溶液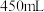 ,所需
,所需 固体的质量为
固体的质量为(3)用
 可制备
可制备 溶液,将
溶液,将 溶液加入到滴有酚酞的
溶液加入到滴有酚酞的 溶液中,观察到溶液红色褪去。溶液褪色的原因可能是①
溶液中,观察到溶液红色褪去。溶液褪色的原因可能是① 被
被 中和,②
中和,②(4)
 溶液不能长久存放的原因是
溶液不能长久存放的原因是 溶液中阴离子的实验操作及现象是
溶液中阴离子的实验操作及现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图在衬白纸的玻璃片中央放置适量的KMnO4颗粒,在周围分别滴加一滴含有酚酞的澄清石灰水、FeCl2溶液,然后在KMnO4晶体上滴加适量的浓盐酸,迅速盖好表面皿。提示:实验室中所用的少量氯气可以用下述原理制取:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,此反应在常温下即能进行。

(1)浓盐酸在反应中表现出来的性质是______ (填写编号),氧化剂与还原剂物质的量之比为______ ,氧化产物为______ 。
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(2)产生0.1 mol Cl2,则转移电子的物质的量为______ mol。
(3)a处反应的化学方程式是___________________________ ,工业上用此原理制取漂白粉。
(4)b处离子方程式是________________________ 。
(5)高锰酸钾标准溶液经常用来滴定测量物质的含量。用高锰酸钾法间接测定石灰石中CaCO3的含量的方法为: 称取试样0.1250g,用稀盐酸溶解后加入(NH4)2C2O4得CaC2O4沉淀。沉淀经过滤洗涤后溶于稀硫酸中。滴定生成的H2C2O4用去浓度为0.0 16mo/LKMnO4溶液25.00mL。
①写出CaC2O4沉淀溶解的离子方程式:___________________
②配平并完成下列高锰酸钾滴定草酸反应的离子方程式:____ MnO4-+___ H2C2O4+____ =___ Mn2++___ CO2↑+____
③石灰石中CaCO3的百分含量:_______

(1)浓盐酸在反应中表现出来的性质是
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(2)产生0.1 mol Cl2,则转移电子的物质的量为
(3)a处反应的化学方程式是
(4)b处离子方程式是
(5)高锰酸钾标准溶液经常用来滴定测量物质的含量。用高锰酸钾法间接测定石灰石中CaCO3的含量的方法为: 称取试样0.1250g,用稀盐酸溶解后加入(NH4)2C2O4得CaC2O4沉淀。沉淀经过滤洗涤后溶于稀硫酸中。滴定生成的H2C2O4用去浓度为0.0 16mo/LKMnO4溶液25.00mL。
①写出CaC2O4沉淀溶解的离子方程式:
②配平并完成下列高锰酸钾滴定草酸反应的离子方程式:
③石灰石中CaCO3的百分含量:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】NaCl是一种基础化工原料,通过电解饱和食盐水可以制得NaOH、H2、Cl2。完成下列填空:
(1)写出电解饱和食盐水的化学方程式_______ 。开始时_______ 极(阴、阳)碱性增强。
(2)新冠疫情期间需要大量消毒液,工业上生产消毒液是将氯气与烧碱溶液反应,完成该反应方程式_______ 。
(3)氯气压缩成为液氯属于_______ 变化(选填“物理”“化学”)。常用浓氨水来检查输氯管道是否泄漏,泄漏处会观察到大量的白烟(NH4Cl),其中一步反应是:2NH3+3Cl2→N2+6HCl,该反应也表明氯和氮的非金属性_______ > _______ 。写出产生白烟的化学方程式:_______ 。该白烟的成分溶于水,溶液呈_______ 性。(酸、碱或中性),用离子方程式解释原因_______ 。
(4)pH=2的醋酸和盐酸两溶液中,水的电离_______。
(5)取25 mLpH=2的醋酸溶液,加入等体积pH=12的NaOH溶液,反应后溶液中c(Na+)、c(CH3COO-)的大小关系为c(Na+)_______ c(CH3COO-)。
(1)写出电解饱和食盐水的化学方程式
(2)新冠疫情期间需要大量消毒液,工业上生产消毒液是将氯气与烧碱溶液反应,完成该反应方程式
(3)氯气压缩成为液氯属于
(4)pH=2的醋酸和盐酸两溶液中,水的电离_______。
| A.都被促进 | B.都被抑制 |
| C.甲中被促进,乙中被抑制 | D.甲中被抑制,乙中被促进 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)NaClO中Cl的化合价为_______ ,NaClO具有较强的_______ (填“氧化”或“还原”)性,是常用的消毒剂和漂白剂的有效成分。
(2)9.03×1023个CO2的物质的量是_______ ,在标准状况下的体积为_______ 。
(3)质量比为11:7:16的CO2、CO、O2,其物质的量之比为_______ ,所含氧原子数之比为_______ 。
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO ,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO
,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO )=
)=_______ 。
(5)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。工业生产漂白粉的化学方程式为_______ 。
(6)FeCl2溶液通入氯气的反应,用离子方程式表示_______ 。
(7)将烧至红热的铁丝伸到盛有氯气的集气瓶中,可观察到铁丝剧烈燃烧,产生棕黄色的烟,反应的化学方程式为_______ ,该反应中被还原的物质是_______ (填化学式)。
(1)NaClO中Cl的化合价为
(2)9.03×1023个CO2的物质的量是
(3)质量比为11:7:16的CO2、CO、O2,其物质的量之比为
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO
 ,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO
,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO )=
)=(5)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。工业生产漂白粉的化学方程式为
(6)FeCl2溶液通入氯气的反应,用离子方程式表示
(7)将烧至红热的铁丝伸到盛有氯气的集气瓶中,可观察到铁丝剧烈燃烧,产生棕黄色的烟,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】双氧水和84消毒液是生活中常用的两种消毒剂,了解物质的性质是科学合理使用化学品的基础和前提。请回答下列问题:
(1)某同学设计如下实验研究H2O2的性质
① 从理论上看H2O2既有氧化性又有还原性,具有还原性的原因是__________ 。
② 能证明H2O2具有还原性的实验是_____ (填序号)。可作为证据的实验现象是_____ (填字母序号)。
(2)84消毒液的有效成分为NaClO
① 将Cl2通入NaOH溶液中可制得84消毒液,化学反应方程式为__________ 。
② 84消毒液不能用于钢制器具的消毒,原因是NaClO具有_________ 性。
③ 84消毒液的溶液在浸泡餐具过程中,因吸收空气中CO2消毒杀菌能力增强,其中发生的化学反应符合规律:______ + ______ = ______ + _____ (填物质类别 )
(3)2016年巴西奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。
① 该反应说明氧化性:NaClO_______ H2O2的(填“>”或“<”)。
② 当有0.1mol O2生成时,转移电子_______ mol
(1)某同学设计如下实验研究H2O2的性质
| 序号 | 实验 | 实验现象 |
| ⅰ | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a. 溶液紫色褪去 b. 有大量气泡产生 |
| ⅱ | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c. 溶液变蓝 |
① 从理论上看H2O2既有氧化性又有还原性,具有还原性的原因是
② 能证明H2O2具有还原性的实验是
(2)84消毒液的有效成分为NaClO
① 将Cl2通入NaOH溶液中可制得84消毒液,化学反应方程式为
② 84消毒液不能用于钢制器具的消毒,原因是NaClO具有
③ 84消毒液的溶液在浸泡餐具过程中,因吸收空气中CO2消毒杀菌能力增强,其中发生的化学反应符合规律:
(3)2016年巴西奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。
① 该反应说明氧化性:NaClO
② 当有0.1mol O2生成时,转移电子
您最近一年使用:0次



